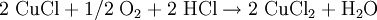- Wacker-Hoechst-Verfahren
-
Das Wacker-Verfahren (auch Wacker-Hoechst-Verfahren genannt) ist ein großtechnischer Prozess in der chemischen Industrie, bei dem eine katalytische Addition von molekularem Sauerstoff an Alkene erfolgt. Dieses von der Wacker Chemie AG (Deutschland) entwickelte Verfahren gehörte zu den ersten, die geeignet waren, auf die zukünftige Bedeutung von Alkenen hinzuweisen. Enorme Mengen an Aldehyden werden jährlich nach dieser Methode produziert.
Man sagte, dass „die Erfindung des Wacker-Verfahrens einen Triumph des gesunden Menschenverstandes“ darstellt.[1] Mit dieser Methode kann z. B. aus Ethen (C2H4) Acetaldehyd (CH3CHO) gewonnen werden. Acetaldehyd kann wiederum zur Essigsäure (CH3COOH) oxidiert werden.
Der Wacker-Prozess bzw. das Wacker-Verfahren führt genauso wie die ebenfalls großtechnisch durchgeführte Hydroformylierung zu Aldehyden, mit dem Unterschied, dass bei der Hydroformylierung eine Kettenverlängerung stattfindet und diese durch andere Übergangsmetalle katalysiert wird.
Der ablaufende Kreisprozess kann in folgende Gleichungen zusammengefasst werden:
Es gibt das einstufige und das zweistufige Verfahren. Beim einstufigen Verfahren wird in nur einem Reaktor die Oxidation des Ethens sowie die Regeneration des Katalysators durchgeführt. Die Regeneration muss mit reinem Sauerstoff erfolgen, außerdem muss das verwendete Ethen sehr rein sein. Um unterhalb der Explosionsgrenze zu bleiben, wird mit einem Überschuss an Ethen gearbeitet, dadurch sinkt die Ausbeute auf etwa 35 %. Nicht umgesetztes Ethen kann jedoch erneut in den Reaktor geführt werden.
Beim zweistufigem Verfahren sind die Oxidation des Ethens und die Regeneration des Katalysators räumlich getrennt. Es kann mit Luftsauerstoff regeneriert werden und auch die Ansprüche an die Reinheit des Ethens sind geringer. Allerdings sind die Investitionskosten in die Anlagen sowie der Energieverbrauch beim zweistufigem Verfahren deutlich höher, weshalb man, wenn die Versorgung mit reinem Sauerstoff gewährleistet ist, lieber das einstufige Verfahren anwendet.
Die Ausbeute liegt für beide Verfahren bei etwa 95 %.
Das Wacker-Hoechst-Verfahren verliert an Bedeutung, da nicht die Aldehyde sondern deren Folgeprodukte industriell die entscheidende Rolle spielen und diese (z. B. Essigsäure oder Essigsäureanhydrid) verstärkt über die Verwendung von Synthesegas hergestellt werden.
Inhaltsverzeichnis
Einzelnachweise
- ↑ G. W. Parshall: Homogeneous Catalysis, Wiley, New York 1980, S. 102
Weblinks
- 3D-Animation des Mechanismus der Reaktion
- Weiteres im Lernprogramm zur Komplexchemie -> Anwendungen -> Katalyse
Siehe auch
Literatur
- Huheey J.; Keiter E.; Keiter R.; Anorganische Chemie, 3. Auflage, de Gruyter, 2003, S. 837
- M.Baerns, A.Behr, A.Brehm, J.Gmehling, H.Hofmann, U.Onken, A.Renken; Technische Chemie, 1. Auflage, Wiley-VCH, 2006, S. 573
Wikimedia Foundation.


![\mathrm{[PdCl_4]^{2-} + C_2H_4 + H_2O \rightarrow CH_3CHO + Pd + 2 \ HCl +2 \ Cl^-}](/pictures/dewiki/50/20923857cba488975379055fb8e933e7.png)
![\mathrm{Pd + 2 \ CuCl_2 + 2 \ Cl^- \rightarrow [PdCl_4]^{2-} + 2 \ CuCl}](/pictures/dewiki/50/24aa4ca490ec5b67e53b6046f651798b.png)