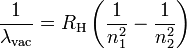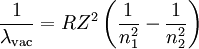- Wasserstoffspektrum
-
Die Rydberg-Formel (Rydberg-Ritz-Formel) wird in der Atomphysik benutzt, um das komplette Spektrum des Lichtes bei der Emission von Licht durch Wasserstoff zu bestimmen. Sie ist proportional zur Energie des Wasserstoffatoms in Abhängigkeit von den Hauptquantenzahlen. Diese Formel wurde später erweitert, um das Spektrum auch aller anderen Elemente zu bestimmen.
Die Formel wurde durch den schwedischen Physiker Janne Rydberg aufgestellt und am 5. November 1888 erstmals vorgestellt. Auch Walter Ritz arbeitete an der Formel.
Rydberg-Formel für Wasserstoff
Mit
- λvac ist die Wellenlänge des Lichtes, wenn dieses im Vakuum emittiert wird.
- RH ist die Rydberg-Konstante für Wasserstoff.
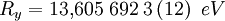 (dies ist die Rydbergenergie von Wasserstoff)
(dies ist die Rydbergenergie von Wasserstoff)- n1 und n2 sind die ganzzahligen Werte der Hauptquantenzahl mit n1 < n2.
Dabei ist
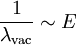
Dies leitet sich aus folgenden Formeln ab: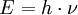 und
und 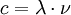 , also folgt:
, also folgt: 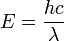
Mit n1 = 1 (Grundzustand) und
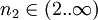 , erhält man eine Serie von Spektrallinien, die auch Lyman-Serie genannt wird. Der erste Übergang der Serie hat eine Wellenlänge von 121 nm, die Seriengrenze liegt bei 91 nm. Analog ergeben sich die anderen Serien:
, erhält man eine Serie von Spektrallinien, die auch Lyman-Serie genannt wird. Der erste Übergang der Serie hat eine Wellenlänge von 121 nm, die Seriengrenze liegt bei 91 nm. Analog ergeben sich die anderen Serien:n1 n2 Name Wellenlänge des Übergangs 1 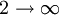
Lyman-Serie 121 nm 2 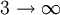
Balmer-Serie 656 nm 3 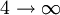
Paschen-Serie 1.874 nm 4 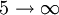
Brackett-Serie 4.051 nm 5 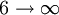
Pfund-Serie 7.456 nm 6 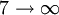
Humphrey-Serie 12.365 nm Rydberg-Formel für wasserstoffähnliche Atome
Die obige Formel lässt sich auch für wasserstoffähnliche Atome anderer chemischer Elemente erweitern.
mit
- λvac ist die Wellenlänge des Lichtes
emittiert im Vakuum.
- R ist die Rydberg-Konstante für das jeweilige Element;
- Z ist die Kernladung, d.h. die Anzahl der Protonen im Atomkern eines Elementes;
- n1 und n2 sind die ganzzahligen Werte der Hauptquantenzahl mit n1 < n2.
Diese Formel lässt sich nur auf Wasserstoff-ähnliche Elemente anwenden, d.h. auf Elemente, die nur ein Elektron in einer nicht abgeschlossenen Schale besitzen. Solche Elemente sind z.B. Lithium, Natrium und Kalium. Eine Verallgemeinerung auf die Lichtemission auch anderer Elemente führt zum Moseleyschen Gesetz. Außerdem werden in der Rydberg-Formel Korrekturen, die aufgrund von Drehimpulsen oder relativistischen Effekten verursacht werden, nicht berücksichtigt.
Wikimedia Foundation.