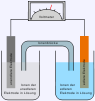
- Zink-Luft
-
Eine Zink-Luft-Batterie ist eine Primärzelle, deren Spannung von maximal 1,65 V aufgrund einer Zink-Sauerstoff-Reaktion entsteht. Meist wird die Spannung durch Reduzierung der Luftzufuhr auf 1,35 bzw. 1,4 V reduziert, um Kompatibilität zu nicht mehr hergestellten Quecksilberoxid-Zink-Batterien zu gewährleisten, wie sie beispielsweise in Hörgeräten (siehe auch Hörgerätebatterie) eingesetzt werden. Die Zink-Luft-Batterie wurde vor allem aufgrund des Rohstoffmangels nach dem Zweiten Weltkrieg entwickelt. Heute bietet sie in der Bauform als Knopfzelle durch besonders hohe Energiedichte und eine annähernd waagerechte Entladungskurve die optimale Stromversorgung für analoge und digitale Hörgeräte.
In der Zink-Luft-Batterie wird Zinkmetall mit Luftsauerstoff in einem alkalischen Elektrolyten zum Oxid oder Hydroxid oxidiert und die dabei freiwerdende Energie elektrochemisch genutzt. Es laufen die folgenden Reaktionen ab:
Entladung
Gleichung Anode 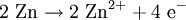
Oxidation / ElektronenabgabeKathode 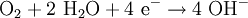
Reduktion / ElektronenaufnahmeGesamtreaktion 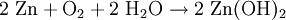
Redoxreaktion / ZellreaktionEine Wiederaufladbarkeit kann erreicht werden, wenn das umgesetzte Metall mechanisch ersetzt wird, womit eine Variante einer Brennstoffzelle mit festem Brennstoff vorliegt. Solche Systeme wurden um das Jahr 2000 auf ihre Eignung in Elektrofahrzeugen geprüft, haben sich jedoch nicht bewährt.
Eine elektrische Ladung ist nicht so aufwändig und wäre somit wesentlich benutzerfreundlicher. Ein Wiederaufladen der Zink-Elektrode ist in einem wässrigen alkalischen Elektrolyten möglich; es bilden sich dabei Dendriten, die zu Kurzschlüssen führen. Außerdem muss eine „bifunktionale“ Luftelektrode verwendet werden. Es handelt sich hierbei um eine poröse „Gasdiffusionselektrode“, die bifunktionell sein muss, d. h. zur Reduktion des Luftsauerstoffs und Oxidation des Entladungsprodukts (OH-) an der Dreiphasengrenze Festelektrode – Flüssigelektrolyt – Gasraum fähig sein muss.
Ladung
Gleichung Anode 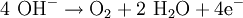
Oxidation / ElektronenabgabeKathode 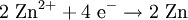
Reduktion / ElektronenaufnahmeGesamtreaktion 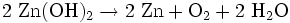
Redoxreaktion / ZellreaktionDie Poren der Gasdiffusionselektrode müssen mit einem Elektrolyten benetzt sein, um eine große Reaktionsfläche für den Sauerstoffumsatz an der Dreiphasengrenze anzubieten. Das „Herzstück“ der Gasdiffusionselektrode ist eine etwa 1 mm dünne Aktivschicht, die ein leitendes Trägermaterial aus feinteiligem Kohlenstoff aufweist, auf das elektrolytseitig ein Katalysator zur Beschleunigung der Sauerstoffreduktion und Hydroxidoxidation aufgebracht wird.
In Zink-Luft-Zellen sind etwa 400 bis 600 Lade-/Entladevorgänge erreichbar; die mittlere Entladespannung beträgt etwa 1,16 V.
Bei neuen Batterien ist die Eintrittsöffnung für den Luftsauerstoff meist mit einer Lasche versiegelt, sodass die Redoxreaktionen erst bei Entfernung dieses Siegels einsetzen. Daher zeichnen sich Zink-Luft-Batterien durch eine lange Lagerfähigkeit aus, müssen nach Entfernung des Siegels jedoch in der Regel innerhalb weniger Wochen aufgebraucht werden.
Primärzellen: Alkali-Mangan-Batterie | Daniell-Element | Leclanché-Element | Lithium-Batterie | Lithium-Eisensulfid-Batterie | Nickel-Oxyhydroxid-Batterie | Quecksilberoxid-Zink-Batterie | Silberoxid-Zink-Batterie | Zink-Braunstein-Zelle | Zinkchlorid-Batterie | Zink-Luft-Batterie
Sekundärzellen: Bleiakkumulator | Natrium-Schwefel-Akkumulator | Nickel-Cadmium-Akkumulator | Nickel-Eisen-Akkumulator | Nickel-Metallhydrid-Akkumulator | Nickel-Wasserstoff-Akkumulator | Lithium-Eisen-Phosphat-Akkumulator | Lithium-Ionen-Akkumulator | Lithium-Mangan-Akkumulator | Lithium-Polymer-Akkumulator | Lithium-Titanat-Akkumulator | Vanadium-Redox-Akkumulator
Ausführungen: Akkumulator | Batterie | Brennstoffzelle | Konzentrationselement | Redox-Flow-Zelle | Bestandteile: Halbzelle (Donator- und Akzeptorhalbzelle)
Wikimedia Foundation.