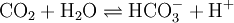- Carboanhydrase
-
Α-Carboanhydrasen —
Kofaktor Zink Bezeichner Gen-Name(n) CA1, CA2, CA3, CA4, CA5A, CA5B, CA6, CA7, CA9, CA12, CA13, CA14 Enzymklassifikation EC, Kategorie 4.2.1.1 Lyase Reaktionsart (De-)Hydratisierung Substrat Kohlendioxid + Wasser Produkte Hydrogencarbonat + Wasserstoffion Die α-Carboanhydrasen (α-CA) sind Enzyme, die die Hydratisierung von Kohlenstoffdioxid zu Kohlensäure (=Hydrogencarbonat) und umgekehrt katalysieren. Sie kommen in Tieren, Bakterien und Grünalgen vor. Kohlendioxid lässt sich im Körper leichter als Hydrogencarbonat transportieren, daher ist eine reversible Umwandlung sinnvoll. Außerdem wird über die Reaktion der pH-Wert des Blutplasmas und der Magensäure geregelt. Bei Tieren sind elf paraloge Isoformen des Enzyms bekannt, sowie vier weitere ohne Enzymaktivität.[1][2]
Die elf Isoformen werden nach Lokalisation unterteilt in:
- zytosolisch (CA-I, CA-II, CA-III, CA-VII, CA-XIII)
- mitochondriell (CA-VA, CA-VB)
- sekretiert (CA-VI)
- membran-assoziiert (CA-IV, CA-IX, CA-XII, CA-XIV)
Inhaltsverzeichnis
Katalysiertes Gleichgewicht
Kohlendioxid wird zu Kohlensäure hydratisiert und umgekehrt.
Die Carboanhydrase ist eines der schnellsten bekannten Enzyme: sie kann jeweils bis zu 106 Moleküle Kohlenstoffdioxid pro Sekunde hydratisieren und beschleunigt die natürliche Reaktion damit um das 107-fache. (Siehe auch: Wechselzahl.)
Aufbau
CA besteht aus einem Protein und enthält als Cofaktor ein Zinkion (Zn2+), welches die eigentliche katalytische Aktivität des Enzyms bedingt. (CA war übrigens nicht nur das erste bekannte Zinkenzym, sondern auch das erste Enzym überhaupt, von dem bekannt war, dass es ein Metall als Cofaktor benötigt.) Das aktive Zentrum besteht aus dem Zinkion, welches an drei Imidazolreste gebunden ist, die je von einer im Protein enthaltenen Aminosäure Histidin stammen. Die vierte Koordinationsstelle ist von einem Hydroxo-Liganden besetzt. Das Zink ist also tetrakoordiniert, der Koordinationspolyeder ist ein Tetraeder.
In seltenen Fällen ist Cadmium als Cofaktor im aktiven Zentrum des Enzyms gebunden. Dies ist zum Beispiel bei Thalassioria weissflogii der Fall.[3]
Funktionen im Organismus
Atmung
Bei der Atmung fällt Kohlendioxid (CO2) als Stoffwechselendprodukt an. Kohlendioxid wird ins Blut freigesetzt und muss zu den Lungen (bei komplexen Organismen) transportiert werden. Bei Pflanzen wird Kohlendioxid für die Photosynthese benötigt und dafür durch die Spaltöffnungen der Blätter aufgenommen. Dieses gelangt schließlich in die Thylakoide und wird im Zuge der Photosynthese zu Glucose umgesetzt. In wässrigen Lösungen, wie z. B. im Blut oder im Zytoplasma, reagiert CO2 indes mit Wasser zu Hydrogencarbonat. Obwohl diese Reaktionen auch ohne Katalysator spontan ablaufen, finden sich Carboanhydrasen in fast allen Organismen. Ob CO2 aufgenommen bzw. abgegeben wird, hängt vom pH-Wert des Zellplasmas ab. Im tierischen Organismus ist CA in Erythrozyten (roten Blutzellen) zu finden, wo sie am Kohlendioxidtransport beteiligt ist. Kohlendioxid diffundiert in den Kapillaren in die Erythrozyten, wird dort mit Wasser zu Kohlensäure umgesetzt und reagiert schließlich zu Hydrogencarbonationen und Protonen. Das Hydrogencarbonat wird im sogenannten „Chlorid-Shift“ gegen Chlorid aus dem Plasma ausgetauscht, um die Elektroneutralität zu wahren.
Nierenfunktion
CA ist unter Anderem entscheidend für die Regulation des Säure-Base-Haushaltes durch die Niere. Für diese Regulation ist wichtig, dass im Primärharn filtriertes Hydrogencarbonat zu etwa 90 Prozent rückresorbiert wird. Andernfalls entstünde eine Azidose. Ohne die CA würde die Hydrogencarbonat-Rückresorption aus dem Primärharn nicht funktionieren. Der Mechanismus: Aus den Tubuluszellen der Niere werden von intrazellulär nach extrazellulär (in das Lumen des Nierentubulus) Protonen (H+) im Austausch gegen Na+ ausgeschieden. Durch die Wirkung der CA reagiert filtriertes Hydrogencarbonat mit Protonen zu Kohlensäure, diese dann zu Wasser und Kohlendioxid. Das Kohlendioxid kann (im Unterschied zum Hydrogencarbonat) leicht durch die Zellmembran vom Tubuluslumen (Primärharn) in die Tubuluszelle gelangen. Dort katalysiert die intrazelluläre CA die umgekehrte Reaktion. Aus dem Kohlendioxid werden so in der Tubuluszelle Protonen und Hydrogencarbonat gebildet. Das Hydrogencarbonat wird aus der Zelle ins Blut abgegeben, das Proton steht erneut für die gleiche Reaktion zur Verfügung. Gehemmt werden kann die Carboanhydrase durch das Medikament Acetazolamid. Die Hemmung führt zu Bicarbonatverlust über den Harn und somit zu einer Azidose. Dies kann zur Behandlung von metabolischen Alkalosen eingesetzt werden.
Magenfunktion
Sie ist das Schlüsselenzym für die Produktion der Magensäure. Die Carboanhydrase befindet sich in den Belegzellen (Parietalzellen) des Magenepithels. Protonen werden an der apikalen Membran der Epithelzelle durch eine Protonen-Kalium-ATPase (V-ATPase) in das Magenlumen transportiert. Dabei wird Kalium im Austausch in die Zelle transportiert. In der Zelle stellt die CA Protonen und Bicarbonat aus Wasser und Kohlendioxid her. An der basolateralen Membran wird Bicarbonat daraufhin im Austausch gegen Chlorid aus der Zelle in das Blutgefäßsystem gebracht. Das Chlorid gelangt an der apikalen Membran durch einen Chloridkanal in das Magenlumen und bildet dort mit den Protonen die Magensäure.
Die V-ATPase und Carboanhydrase in den Belegzellen des Magens wird durch Protonenpumpenhemmer wie z. B. Omeprazol oder Pantoprazol gehemmt.[4]
CA-IV
Im Ziliarkörper des Auges ist die Carboanhydrase CA-IV an der Produktion des Kammerwassers beteiligt. Hemmung durch Azetazolamid kann eine übermäßige Produktion (relativ im Vergleich zum Abtransport aus dem Auge) des Kammerwassers reduzieren und so helfen, einen überhöhten Augeninnendruck Glaukom zu reduzieren. Mutationen am CA4-Gen können zu einer Form der Retinitis pigmentosa (RP17) führen.
Weitere Funktionen
In der Bauchspeicheldrüse dient die Carboanhydrase der Hydrogencarbonat-Sekretion
Die heute nur noch selten verwendeten Sulfonamide hemmen ebenfalls die Carboanhydrase.
Bei Süßwasserfischen ermöglicht die Carboanhydrase in darauf spezialisierten Zellen des Kiemenepithels die Salzresorption und dient damit der Osmoregulation.
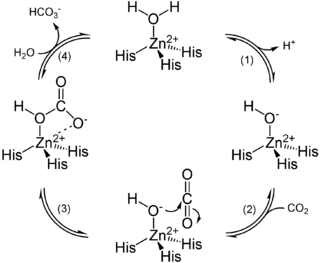
Reaktionsmechanismus der Carboanhydrase
- An das Zink(II) Ion, welches an die drei Stickstoffdonorzentren des Imidazolringes der drei Histidin-Aminosäuren koordiniert ist, kann sich ein Molekül Wasser anlagern. Infolge der Koordination an das Zinkion wird der pKs Wert des Wassermoleküls gesenkt – so weit, dass auch bei dem physiologischem pH Wert, wie er in der Umgebung der Carboanhydrase zu finden ist, ein Proton abgespalten werden kann (1).
- Dabei ist die am Sauerstoff zurückbleibende negative Ladung mesomeristabilisiert, da sie auf das Zink(II)ion übertragen werden kann.
- In einem nächsten Schritt (2) lagert sich ein Molekül Kohlenstoffdioxid im aktiven Zentrum des Enzyms so an, dass es mit dem Hydroxidion reagieren kann.
- Die freien Elektronenpaare am Sauerstoff der OH-Gruppe greifen nukleophil das Kohlendioxidmolekül an, so dass ein Hydrogencarbonation entsteht (3)
- Schließlich kann ein Wassermolekül an das aktive Zentrum gebunden werden, so dass das Hydrogenkarbonation freigesetzt wird (4).
Durch diese Regenerierung des aktiven Zentrums kann ein neuer Zyklus beginnen.
Literatur
- Berg/Tymoczko/Stryer: Biochemie. 5. Auflage. Spektrum Akademischer Verlag, Heidelberg 2003, ISBN 3827413036
Einzelnachweise
- ↑ PROSITE-Eintrag
- ↑ Interpro: Carboanhydrasen
- ↑ Lane TW, Morel FM: A biological function for cadmium in marine diatoms. In: Proc. Natl. Acad. Sci. U.S.A.. 97, Nr. 9, April 2000, S. 4627–31. doi:10.1073/pnas.090091397. PMID 10781068
- ↑ Puscas I, Coltau M, Baican M, Domuta G: Omeprazole has a dual mechanism of action: it inhibits both H(+)K(+)ATPase and gastric mucosa carbonic anhydrase enzyme in humans (in vitro and in vivo experiments). In: J. Pharmacol. Exp. Ther.. 290, Nr. 2, August 1999, S. 530–4. PMID 10411559
Weblinks
- Jennifer McDowall/Interpro: Protein Of The Month: Carbonic Anhydrase. (engl.)
Wikimedia Foundation.