- Cytochrom c Oxidase
-
Cytochrom-c-Oxidase, Untereinheiten 1-3 (mitochondrial) Schematische Darstellung der Cytochrom-c-Oxidase (UE I-IV) Größe 513,227,261 Aminosäuren (UE 1,2,3) Bezeichner Gen-Namen MT-CO1; MT-CO2; MT-CO3 Externe IDs CAS-Nummer: 9001-16-5 Transporter-Klassifikation TCDB 3.D.4.7.1 Bezeichnung protonenübertragende COX Enzymklassifikation EC, Kategorie 1.9.3.1 Oxidoreduktase Reaktionsart Redoxreaktion Substrat 4 Cytochrom c (reduziert) + O2 + 4 H+ Produkte 4 Cytochrom c (oxidiert) + 2 H2O Das Enzym Cytochrom-c-Oxidase (COX), genauer Cytochrom c : Sauerstoff Oxidoreduktase (systematischer Name), Cytochrom-aa3-Komplex oder auch Komplex IV der mitochondrialen Atmungskette genannt, ist eine Oxidoreduktase. Das Enzym katalysiert in einer gekoppelten Reaktion die Oxidation von Cytochrom c mit der Reduktion von Sauerstoff zu Wasser und dem Transport von Protonen über eine biologische Membran.
Inhaltsverzeichnis
Die Enzymfamilie der Häm-Kupfer-Oxidasen
Die Cytochrom-c-Oxidase gehört zur Superfamilie der Häm-Kupfer-Oxidasen, die bei allen aerob atmenden Organismen den terminalen Elektronenakzeptor der Atmungskette darstellen. Sie sind für nahezu sämtlichen Sauerstoffverbrauch der atmenden Organismen verantwortlich. Die Oxidasen sind bei Eukaryonten in der inneren Mitochondrienmembran, bei Prokaryonten in der inneren Zellmembran eingelagert. Varianten der Cytochrom-c-Oxidase kommen in der Zellmembran aerober Bakterien vor. Diese enthalten zum Teil modifizierte Kofaktoren (Häm-Varianten), oder verwenden andere Elektronendonoren als Cytochrom c (Chinol-Oxidasen z. B. in Escherichia coli). Sie besitzen sämtlich große strukturelle und funktionelle Homologie und enthalten im aktiven Zentrum eine Häm-Gruppe und ein Kupfer-Ion.
Struktur
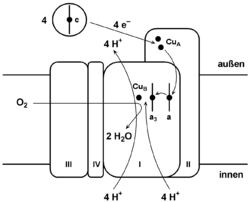
Der mitochondriale Enzymkomplex in Säugetieren besteht aus 13 Untereinheiten, von denen die Untereinheiten I–III mitochondrial und die weiteren Untereinheiten IV–XIII vom Nukleus kodiert sind. Die Untereinheit I besitzt die drei redoxaktive Metallzentren Häm a, Häm a3 und CuB. Häm a3 und CuB bilden zusammen das katalytisch aktive Zentrum, an dem Sauerstoff gebunden und zu Wasser reduziert wird. Die Untereinheit II besitzt das redoxaktive Metallzentrum CuA, das Elektronen vom Cytochrom c aufnimmt, die dann zum Häm a und weiter zum Häm a3 transferiert werden.
Funktion
Die Funktion der Cytochrom-c-Oxidase besteht aus der
- Reduktion von Sauerstoff zu Wasser (biologische Knallgasreaktion) mittels Elektronen vom Cytochrom c und dem
- Transport von Protonen (Protonenpumpe) über die biologische Membran.
Während des katalytischen Zyklus der Cytochrom-c-Oxidase wird ein Molekül Sauerstoff (O2) zu zwei Molekülen Wasser (H2O) reduziert. Als Reduktionsmittel werden vier Elektronen (e−) von vier Molekülen Cytochrom c sowie Protonen (H+) für die Wasserbildung aus dem Innenraum des Mitochondriums (Matrix) gebraucht. Die bei der Reduktion von Sauerstoff zu Wasser freigesetzte Energie wird zum Aufbau eines Protonengradienten über die innere Mitochondrienmembran genutzt. Pro Reaktionszyklus werden vier Protonen aus dem Innenraum des Mitochondriums in den Intermembranraum transportiert.
Das komplexe Zusammenspiel der ablaufenden Sauerstoffchemie, der Elektronentransferreaktionen, sowie den Protonenaufnahme- und Pumpschritten und deren genauen zeitlichen Abfolgen konnten bisher noch nicht detailliert aufgeklärt werden. Ein einfaches Bild des Reaktionszyklus sieht wie folgt aus: Geht man vom vollständig oxidierten Zustand der Cytochrom-c-Oxidase aus, werden nacheinander 2 Elektronen über das CuA und das Häm a in das katalytisch aktive Häm-a3/CuB-Zentrum transferiert. Im um 2 Elektronen reduzierten Zustand bindet das Häm a3 den Sauerstoff, dieser wird konzertiert mit 4 Elektronen reduziert. Die zwei gebildeten Sauerstoffionen binden als Oxo-Gruppe (=O2−) an das Häm a3 und das CuB. Durch die Aufnahme von 2 weiteren Elektronen und die Abspaltung von 2 Wassermolekülen relaxiert das Enzym wieder zum Ausgangszustand. Protonenaufnahme von der Innenseite der Membran und Protonenpumpschritte über die Membran hinweg findet mit jedem der 4 Elektronentransferreaktionen pro Zyklus vom reduzierten Cytochrom c zum Reaktionszentrum der Cytochrom-c-Oxidase statt. Die Ausbildung eines Protonengradienten über die Membran durch die Protonenpumpaktivität der Oxidase wird zusätzlich dadurch verstärkt, dass die vier für die Wasserbildung erforderlichen Protonen nur von der Innenseite der Membran aufgenommen werden.
Reaktionsgleichung:
- 4 Cyt c (FeII) + O2 + 8 H+innen → 4 Cyt c (FeIII) + 2 H2O + 4 H+außen
Inhibitoren
Cyanide, Kohlenmonoxid, Schwefelwasserstoffe und Azide sind Inhibitoren der Cytochrom-c-Oxidase. Sie blockieren irreversibel die Bindungsstelle für Sauerstoff im aktiven Zentrum.
Nachweis
Zum Nachweis des Enzyms Cytochrom-c-Oxidase in Zellen wird der Oxidase-Test verwendet.
Alternative Bezeichnungen
- Cytochrom c : O2 Oxidoreduktase
- Cytochrom-Oxidase (Zytochromoxidase)
- Komplex IV der Atmungskette
- Cytochrom-aa3-Komplex nach David Keilin
- Atmungsferment nach Otto Heinrich Warburg (Nobelpreis für die Entdeckung)
- Indophenol-Oxidase nach Paul Ehrlich
Siehe auch
Bekannte 3D-Kristallstrukturen der Cytochrom-c-Oxidase:
- das mitochondriale Enzym aus Rinderherz: PDB 2OCC
- das bakterielle Enzym aus Paracoccus denitrificans: PDB 1QLE Orientierung in der Membran
- das bakterielle Enzym aus Rhodobacter sphaeroides: PDB 1M56
- das bakterielle Enzym aus Thermus thermophilus: PDB 1EHK
bzw. der Chinol-Oxidase:
- das bakterielle Enzym aus Escherichia coli: PDB 1FFT
Weitere Enzymkomplexe der Atmungskette:
- Komplex I auch NADH-Dehydrogenase
- Komplex II auch Succinat-Dehydrogenase
- Komplex III auch Cytochrom-c-Reduktase
- Komplex V auch ATP-Synthase
Literatur
- Warburg, O. (1924): Über Eisen, den sauerstoffübertragenden Bestandteil des Atmungsfermentes. In: Biochemische Zeitschrift. Bd. 152, S. 479–494.
- David Keilin (1925): On cytochrome, a respiratory pigment, common to animals, yeast, and higher plants. In: Proc. Royal Soc. London. Series B. Bd. 98, S. 312–339. JSTOR
- Iwata, S. et al. (1995): Structure at 2.8 A resolution of cytochrome c oxidase from Paracoccus denitrificans. In: Nature. Bd. 376, S. 660–669. PMID 95379947 Volltext (PDF)
- Tsukihara, T. et al. (1996): The whole structure of the 13-subunit oxidized cytochrome c oxidase at 2.8 A. In: Science. Bd. 272, S. 1136–1144. PMID 96216288
Wikimedia Foundation.