- Cytochrom C
-
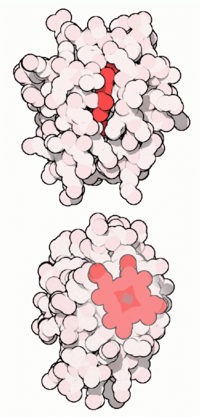
Kalottenmodell des Cytochrom c mit Häm-Gruppe (rot) und Eisen-Ion (grau)
Cytochrom c ist ein kleines Protein mit etwa 100 Aminosäuren aus der Familie der Cytochrome, das in den Mitochondrien („Kraftwerke der Zelle“) bei der oxidativen Phosphorylierung (Energiegewinnung) eine entscheidende Rolle als Elektronencarrier (Elektronentransporter) spielt.
Inhaltsverzeichnis
Struktur
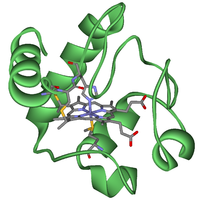
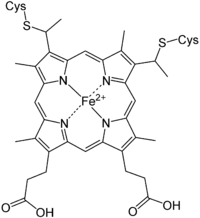
Die Primärstruktur des humanen Cytochrom c besteht aus 104 Aminosäuren.[1] Das Cytochrom c besitzt als prosthetische Gruppe ein Häm c, das über zwei Thioether-Brücken an zwei Cystein-Reste im Protein gebunden ist. Das zentrale Eisen-(II)-Ion (Fe2+) ist oktaedrisch komplexiert über koordinative Bindungen zu den vier Stickstoff-Atomen (äquatorial) der Pyrrole im Porphyrin und axial zu einem Stickstoff-Atom eines Histidin-Restes und zu einem Schwefel-Atom eines Methionin-Restes im Protein.
Die Häm-Gruppe ist außerdem für die rote Farbe des Cytochrom c verantwortlich.
Funktion
Das Enzym Cytochrom-c-Reduktase (Komplex III der Atmungskette) oxidiert über den Q-Zyklus ein Molekül Coenzym Q (CoQ) und reduziert dabei zwei Moleküle Cytochrom c. Das Enzym Cytochrom-c-Oxidase (Komplex IV der Atmungskette) oxidiert vier Moleküle Cytochrom c und reduziert dabei ein Molekül Sauerstoff zu zwei Molekülen Wasser.
Bei Beschädigung der Mitochondrien wird Cytochrom c ins Zytosol abgegeben, wo es über eine Signalkaskade den programmierten Zelltod (Apoptose) auslöst.
Da Cytochrom c in praktisch allen Lebewesen vorkommt und sich seine Primärstruktur zwischen ähnlichen Arten nur in wenigen Aminosäuren unterscheidet, ist es ein wichtiges Mittel zur taxonomischen Einteilung der Lebewesen und ein Indiz für die evolutionäre Entwicklung der Arten.
Siehe auch
Enzymkomplexe der Atmungskette:
- Komplex I, auch NADH-Dehydrogenase
- Komplex II, auch Succinat-Dehydrogenase
- Komplex III, auch Cytochrom-c-Reduktase
- Komplex IV, auch Cytochrom-c-Oxidase
- Komplex V, auch ATP-Synthase
Einzelnachweise
Literatur
- I. Bertini et al. (2006): Cytochrome c: occurrence and functions. In: Chemical Reviews. Bd. 106, S. 90-115. PMID 16402772.
Wikimedia Foundation.