- Eiweißmangel
-
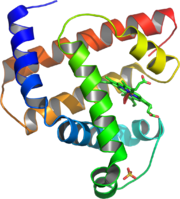 Eine Darstellung der 3D-Struktur von Myoglobin mit farbigen α-Helices. Dies war das erste Protein, dessen Struktur mit Hilfe der Kristallstrukturanalyse aufgeklärt wurde.
Eine Darstellung der 3D-Struktur von Myoglobin mit farbigen α-Helices. Dies war das erste Protein, dessen Struktur mit Hilfe der Kristallstrukturanalyse aufgeklärt wurde.Proteine, umgangssprachlich auch Eiweiße genannt, sind aus Aminosäuren aufgebaute Makromoleküle. Proteine gehören zu den Grundbausteinen aller Zellen. Sie verleihen der Zelle nicht nur Struktur, sondern sind die molekularen „Maschinen“, die Stoffe transportieren, Ionen pumpen, chemische Reaktionen katalysieren und Signalstoffe erkennen. Die Gesamtheit aller Proteine in einem Lebewesen, einem Gewebe, einer Zelle oder einem Zellkompartiment, unter exakt definierten Bedingungen und zu einem bestimmten Zeitpunkt, wird als Proteom bezeichnet.
Bausteine der Proteine sind bestimmte als proteinogen, also proteinaufbauend, bezeichnete Aminosäuren, die durch Peptidbindungen zu Ketten verbunden sind. Beim Menschen handelt es sich um 21 verschiedene Aminosäuren - die 20 seit langem bekannten sowie Selenocystein. Die Aminosäureketten können eine Länge von bis zu mehreren tausend Aminosäuren haben, wobei man Aminosäureketten mit einer Länge von unter ca. 100 Aminosäuren als Peptide bezeichnet und erst ab einer größeren Kettenlänge von Proteinen spricht. Die molekulare Größe eines Proteins wird in der Regel in Kilo-Dalton (kDa) angegeben. Titin, das mit ca. 3600 kDa größte bekannte menschliche Protein, besteht aus über 30.000 Aminosäuren und beinhaltet 320 Proteindomänen.
Die Aminosäureabfolge eines Proteins - und damit sein Aufbau - ist in dem jeweiligen Gen kodiert.
Das Wort Protein wurde 1838 von Jöns Jakob Berzelius von dem griechischen Wort πρωτευω (proteuo, „ich nehme den ersten Platz ein“, von πρωτος, protos, „erstes“, „wichtigstes“) abgeleitet. Dies soll die Bedeutung der Proteine für das Leben unterstreichen.
Inhaltsverzeichnis
Bedeutung für den Organismus
Proteine können im Organismus folgende, sehr unterschiedliche Funktionen haben:
- Verschiedene Keratinstrukturen dienen dem Schutz und der Verteidigung von höheren Lebewesen: Haare/Wolle, Hörner, Nägel/Klauen, Schnäbel, Schuppen und Federn.
- Kollagene, die bis zu 1/3 des gesamten Körperproteins ausmachen können, sind Strukturproteine der Haut, des Bindegewebes und der Knochen. Als Strukturproteine bestimmen sie den Aufbau der Zelle und damit letztlich die Beschaffenheit der Gewebe und des gesamten Körperbaus.
- In den Muskeln verändern Myosine und Aktine ihre Form und sorgen dadurch für Muskelkontraktion und damit für Bewegung.
- Enzyme übernehmen Biokatalysefunktionen, d.h. sie ermöglichen und kontrollieren sehr spezifische (bio)chemische Reaktionen in Lebewesen.
- Als Ionenkanäle regulieren sie die Ionenkonzentration in der Zelle, und damit deren osmotische Homöostase sowie die Erregbarkeit von Nerven und Muskeln.
- Als Transportproteine übernehmen sie den Transport körperwichtiger Substanzen wie z. B. Hämoglobin, das im Blut für den Sauerstofftransport zuständig ist, oder Transferrin, das Eisen im Blut transportiert.
- In Zellmembranen befinden sich Membranrezeptoren - meist Komplexe aus mehreren Proteinen (auch Multiproteinkomplexe genannt), die Substanzen außerhalb der Zelle erkennen und binden. Dadurch ergibt sich eine Konformationsänderung, die dann als Transmembransignal im Innern der Zelle erkannt wird.
- Manche (meist kleinere Proteine) steuern als Hormone Vorgänge im Körper.
- Als Antikörper dienen sie der Infektionsabwehr.
- Als Blutgerinnungsfaktoren verhindern die Proteine einerseits einen zu starken Blutverlust bei einer Verletzung eines Blutgefäßes und andererseits eine zu starke Gerinnungsreaktion mit Blockierung des Gefäßes.
- Proteine und Peptide mit sehr speziellen Funktionen, die nur in ganz bestimmten Spezies vorkommen, sind beispielsweise Seidenfäden in Spinnen und Insekten, auto-fluoreszierende Proteine in Quallen und Toxine in Schlangen, Skorpionen und Conotoxine in Kegelschnecken.
- Als Reservesubstanz dienen die Proteine dem Körper als Energielieferanten im Hungerzustand. Wobei die in Leber, Milz und Muskel gespeicherten Proteine im Hungerzustand zur Glukoneogenese und damit zur Energiegewinnung genutzt werden können, um die lebensnotwendigen Prozesse des Körpers aufrechtzuerhalten.
Mutationen in einem Gen können Veränderungen im Aufbau des Proteins verursachen, das durch das Gen kodiert wird. Die Folge können Fehler in der Proteinaktivität sein. Solche Fehler mit teils vollständigem Wegfall der Proteinaktivität liegen vielen erblichen Krankheiten zugrunde.
Räumlicher Aufbau
Die räumliche Struktur bedingt die Wirkungsweise der Proteine. Die Proteinstruktur lässt sich auf vier Betrachtungsebenen beschreiben:
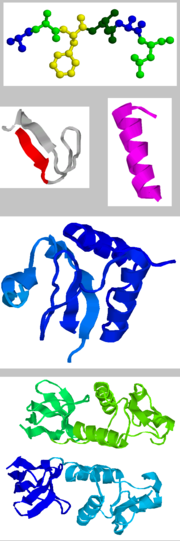
- Als Primärstruktur eines Proteins wird die Abfolge (Sequenz) der einzelnen Aminosäuren einer Polypeptidkette bezeichnet. Vereinfacht gesagt könnte man sich eine Kette vorstellen, in der jedes Kettenglied eine Aminosäure darstellt (Schreibweise: AS1–AS2–AS3–AS4- ...). Die Primärstruktur beschreibt lediglich die Aminosäurensequenz, jedoch nicht den räumlichen Aufbau des Proteins.
- Als Sekundärstruktur wird die Zusammensetzung des Proteins aus besonders häufig auftretenden Motiven für die räumliche Anordnung der Aminosäuren bezeichnet. Man unterscheidet dabei zwischen folgenden Strukturtypen: α-Helix, β-Faltblatt, β-Schleifen und ungeordnete, so genannte Random-Coil-Strukturen. Diese Strukturen ergeben sich durch Wasserstoffbrückenbindungen zwischen den Peptidbindungen des Polypeptid-Rückgrates.
- Die Tertiärstruktur ist die der Sekundärstruktur übergeordnete räumliche Anordnung der Polypeptidkette. Sie wird von den Kräften und Bindungen zwischen den Resten (d. h. den Seitenketten) der Aminosäuren bestimmt. Als Bindungskräfte, die diese dreidimensionale Struktur stabilisieren, wirken beispielsweise Disulfidbrücken, (kovalente Bindungen zwischen den Schwefelatomen zweier Cysteinreste) oder vor allem nicht-kovalente Wechselwirkungen wie die zuvor genannten Wasserstoffbrückenbindungen. Zusätzlich spielen hydrophobe, ionische und Van-der-Waals-Kräfte eine wichtige Rolle. Durch diese Kräfte und Bindungen faltet sich das Protein weiter.
- Viele Proteine müssen sich, um funktionsfähig sein zu können, zu einem Proteinkomplex zusammenlagern, der so genannten Quartärstruktur. Dies kann entweder eine Zusammenlagerung von unterschiedlichen Proteinen sein oder ein Verband aus zwei oder mehr Polypeptidketten die aus ein und derselben Polypeptidkette, dem sog. Precursor, hervorgegangen sind (vgl.: Insulin). Dabei sind die einzelnen Proteine häufig durch Wasserstoffbrücken und Salzbrücken aber auch durch kovalente Bindungen miteinander verknüpft. Die einzelnen Untereinheiten eines solchen Komplexes werden als Protomere bezeichnet. Einige Protomere können ihre Funktion auch als eigenständige Proteine besitzen, aber viele erreichen ihre Funktionalität nur im Komplex. Als Beispiel für aus mehreren Proteinen zusammengelagerte Komplexe können die Immunglobuline (Antikörper) dienen, bei denen jeweils zwei identische schwere und zwei identische leichte Proteine über insgesamt vier Disulfidbrücken zu einem funktionsfähigen Antikörper verbunden sind.
Diese Einteilung in Primär- bis Quartärstruktur erleichtert das Verständnis und die Beschreibung der sequentiellen Faltung von Proteinen. Unter physiologischen Bedingungen muss eine definierte Primärstruktur zu einer definierten Tertiärstruktur (oder Quartärstruktur) führen. Anders gesagt: Der Informationsgehalt, der sich in einer bestimmten dreidimensionalen Proteinstruktur äußert, ist bereits in der linearen Primärstruktur (d.h. in der "eindimensionalen" Aminosäuresequenz) enthalten.
Viele komplexe Proteine können sich nicht spontan falten, also ihre physiologische Struktur einnehmen, sondern brauchen dazu Faltungshelfer, sogenannte Chaperone. Die Chaperone binden an neugebildete (oder auch beschädigte, denaturierte) Aminosäureketten, und verhelfen ihnen unter Verbrauch chemischer Energie zu ihrer Struktur.
Man unterscheidet zwei Hauptgruppen von Proteinen:
- die globulären Proteine, deren Tertiär- oder Quartärstruktur annähernd kugel- oder birnenförmig aussieht und die meist in Wasser oder Salzlösungen gut löslich sind (beispielsweise das Protein des Eiklars, Ov-Albumin genannt),
- die fibrillären Proteine, die eine fadenförmige oder faserige Struktur besitzen, meist unlöslich sind und zu den Stütz- und Gerüstsubstanzen gehören (beispielsweise die Keratine in den Haaren und Fingernägeln, Kollagen, Actin und Myosin für die Muskelkontraktion).
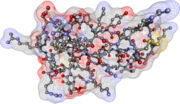
Proteinoberfläche
Der Einfachheit halber wird stellvertretend für die komplexe Proteinstruktur oft nur das Rückgrat (Backbone) des Proteins abgebildet (z.B. Abbildungen rechts oben). Zum Verständnis der Funktion ist jedoch die Oberfläche des Proteins von großer Bedeutung. Da die Seitenketten der Aminosäuren vom Rückgrat aus in den Raum ragen, tragen auch sie entscheidend zur Struktur bei: Der Verlauf des Rückgrats bestimmt den generellen dreidimensionalen Aufbau, aber die Konturen der Oberfläche und ihre chemischen Eigenschaften werden von den Seitenketten bestimmt.
Denaturierung
Sowohl durch chemische Einflüsse, wie zum Beispiel Säuren, Salze oder organische Lösungsmittel, als auch durch physikalische Einwirkungen, wie hohe oder tiefe Temperaturen oder auch Druck, können sich die Sekundär- und Tertiärstruktur und damit auch die Quartärstruktur von Proteinen ändern, ohne dass sich die Reihenfolge der Aminosäuren (Primärstruktur) ändert. Dieser Vorgang heißt Denaturierung und ist in der Regel nicht umkehrbar, das heißt der ursprüngliche dreidimensionale räumliche Aufbau kann ohne Hilfe nicht wiederhergestellt werden. Bekanntestes Beispiel dafür ist das Eiklar im Hühnerei, das beim Kochen fest wird, weil sich der räumliche Aufbau der Proteinmoleküle geändert hat. Der ursprüngliche flüssige Zustand kann nicht mehr hergestellt werden. Das Wiederherstellen des ursprünglichen Zustandes des denaturierten Proteins heißt Renaturieren.
Menschen denaturieren, das heißt kochen, ihre Speisen, um sie leichter verdaulich zu machen. Durch die Denaturierung ändern sich die physikalischen und physiologischen Eigenschaften der Proteine, wie z. B beim Spiegelei, das durch die Hitze in der Pfanne denaturiert wird. Hohes Fieber kann deshalb für den Menschen lebensgefährlich werden. Denn durch die zu hohe Körpertemperatur werden beim Fieber körpereigene Proteine denaturiert und können somit ihre lebensnotwendigen Aufgaben im Organismus nicht mehr erfüllen. Einige Proteine der roten Blutkörperchen denaturieren beispielsweise bereits bei 42 °C. Das Fieber hat eigentlich aber eine schützende Funktion, nicht eine zerstörende. Denn die hohe Temperatur beim Fieber soll Eindringlinge und Fremdkörper, sogenannte Antigene, zerstören und unschädlich machen. Diese Antigene denaturieren meist schon bei geringeren Temperaturen als die körpereigenen Proteine.
Die bei chemischer Spaltung der Proteinketten (Proteolyse) entstehenden Teilstücke nennt man Peptone.
Eiweißmangel
Eiweiß hat eine große Anzahl von Aufgaben in unserem Körper. Es ist zum Aufbau und zum Erhalt der Körperzellen notwendig und hilft bei der Heilung von Wunden und Krankheiten. Ein erwachsener Mensch sollte täglich etwa 0.8 Gramm Eiweiß pro Kilogramm Körpergewicht mit der Nahrung zu sich nehmen, bei schwangeren und stillenden Frauen nimmt der Bedarf etwas zu.[1] Bei körperlicher Aktivität steigt der Bedarf an Protein hingegen nicht.[2]
Ein Mangel kann folgende Symptome hervorrufen:
- Haarausfall (Haare bestehen zu 97–100 % aus Proteinen - Keratin)
- Im schlimmsten Fall kommt es zur Eiweißmangelkrankheit Kwashiorkor. Menschen (meist Kinder), die an Kwashiorkor leiden, erkennt man an ihrem sogenannten Hungerbauch, der durch eine übermäßige Einlagerung von Wasser (Ödeme) hervorgerufen wird. Weitere Symptome sind:
- Muskelschwäche
- Wachstumsstörungen
- Fettleber
- Andauernder Eiweißmangel führt zum Marasmus und zum Tod.
Zu Eiweißmangel kommt es in den Industrieländern allerdings höchst selten und auch nur bei extrem proteinarmen Ernährungsformen. Die durchschnittliche deutsche Mischkost dagegen enthält mit 100 Gramm Eiweiß pro Tag mehr als genug Proteine. Obwohl häufig in der Werbung Eiweißpulver als essentiell notwendig für Breitensportler angepriesen werden, deckt „Unsere übliche Ernährung [...] auch den Eiweißbedarf von Sportlern ab“, heißt es dazu in einem Bericht des Ministeriums für Ernährung und Ländlichen Raum Baden-Württembergs.
Proteinbiosynthese
→ Hauptartikel: Proteinbiosynthese
Mit der Nahrung nehmen wir Proteine auf. Bei unserer Verdauung werden diese Proteine in ihre Bestandteile zerlegt – die Aminosäuren. Auf neun Aminosäuren (von 21, die insgesamt benötigt werden) ist der menschliche Organismus besonders angewiesen, denn sie sind essenziell, das bedeutet, dass der Körper sie nicht selbst herstellen kann. Mit dem Blut werden die Aminosäuren in jede Zelle transportiert. Die Aminosäurensequenz ist in der Desoxyribonukleinsäure (DNA) kodiert. In den Ribosomen, der „Proteinproduktionsmaschinerie“ der Zelle, wird diese Information verwendet, um aus einzelnen Aminosäuren ein Proteinmolekül zusammenzusetzen, wobei die Aminosäuren in einer ganz bestimmten, von der DNA vorgegebenen Reihenfolge verknüpft werden.
Proteinlieferanten
Sehr proteinhaltige Nahrungsmittel sind:
Studien des amerikanischen Biochemikers Thomas Osborne und Lafayette Mendel, Professor für Physiologische Chemie in Yale, von 1914 zeigten, dass Ratten, die tierisches Eiweiß erhielten, schneller an Gewicht zunahmen, als Ratten, die nur pflanzliches Eiweiß erhielten. Daraus wurde voreilig geschlossen, dass tierisches Eiweiß „hochwertiger“ als pflanzliches Eiweiß sei. Tatsächlich kann man aber mit wenigen hochwertigen Pflanzenproteinen (Kartoffel, Soja) eine gleichwertige Ernährung erreichen. Es kommt bei Protein als Nahrung allein auf den Anteil an deren Bausteinen, den Aminosäuren, an.
- Für Details zum Thema siehe die Artikel essentielle Aminosäure, biologische Wertigkeit und Aminosäureindex.
Nachweis von Proteinen
- UV-Absorption
- Xanthoproteinreaktion
- Millon-Reaktion
- Ninhydrinreaktion
- Biuretreaktion
- Bradford-Test
- Proteinbestimmung nach Lowry
- BCA-Reaktion
3D-Darstellung
Zum besseren Verständnis von Aufbau und Funktion ist es unerlässlich, die räumliche Gestalt von Proteinen mithilfe geeigneter Grafikprogramme darzustellen.
→ Für weitere Details siehe den Artikel Molekulardesign.
Das meistverbreitete Dateiformat für Atompositionsdaten von Proteinen ist das PDB-Format der freizugänglichen Protein Data Bank. Eine PDB-Datei enthält zeilenweise Einträge für jedes Atom im Protein, sortiert nach der Aminosäuresequenz; im einfachsten Fall sind das Atomart und kartesische Koordinaten. Es handelt sich also um ein systemunabhängiges Klartext-Format.
Wirtschaftliche Nutzung
Die Gesamtmenge der als nachwachsende Rohstoffe in der stofflichen Nutzung verwendeten Proteine wird für Deutschland im Regelfall mit etwa 55.000 t pro Jahr angegeben.[3] Genaue Angaben über die Herkunft dieser Proteine gibt es nicht, es ist jedoch anzunehmen, dass sie zu einem großen Teil tierischer Herkunft sind.
Der Großteil pflanzlicher Proteine wird für die Futtermittelindustrie aufgewendet, so die als Nebenprodukte bei der Pflanzenölpressung und -extraktion anfallenden Preßrückstände (z. B. Raps- und Sojakuchen, Extraktionsschrot) und Nebenprodukte der Gewinnung von Stärke aus Getreide. Pflanzen, die zur Hauptnutzung als Proteinpflanzen angebaut werden, wie bspw. Lupine, Eiweißerbse und Ackerbohne, haben nur eine geringe Bedeutung[4] – die Gesamtfläche für den Anbau dieser Pflanzen als Nachwachsende Rohstoffe in Deutschland liegt bei etwa 30 ha pro Jahr.[5] Etwa 1.000 t Weizenproteine finden jährlich Einsatz in der Chemischen Industrie.
Von zentraler Bedeutung für die chemisch-technische und biotechnologische Industrie sind dagegen tierische Proteine. Dabei spielt vor allem die Gelatine eine zentrale Rolle, die in Europa vor allem aus Rinderspalt, Schweineschwarten sowie Knochen von Rindern und Schweinen gewonnen wird. In Deutschland werden jährlich etwa 32.000 t Gelatine in Speisequalität hergestellt, die europäische Gesamtproduktion beträgt 120.000 t (70 % Schweineschwarten, 18 % Knochen, 10 % Rinderspalt, 2 % Sonstige).[6][7] Verwendet werden in Deutschland etwa 90.000 t, wobei 2/3 im Ernährungsbereich und von dem Rest etwa die Hälfte für den Futtermittelbereich aufgewendet werden. Etwa 15.000 t werden in der chemischen und pharmazeutischen Industrie verwendet. Dabei finden sich die Haupteinsatzbereiche in der Pharmaindustrie, mit Umhüllungen von Tabletten und Vitaminpräparaten (Hart- und Weichkapseln) sowie Gelatinezäpfchen. Außerdem wird Gelatine für blutstillende Schwämmchen sowie als Blutplasmaersatz eingesetzt. In der analogen Fotografie stellt Gelatine die Basis für die fotoempfindlichen Schichten auf dem Film und dem Fotopapier dar. Auch moderne Druckerpapiere zum Ausdrucken von Farbbildern sind mit Gelatine beschichtet.[7]
Neben Gelatine stellt Casein eine wichtige Proteinquelle für die chemische Industrie dar. Das aus Milcheiweiß gewonnene Protein wird vor allem als Beschichtungsmaterial für Glanzpapiere sowie als Zusatz für Streichfarben verwendet (ca. 1–2 % je nach Hersteller). Zudem findet es Verwendung als Etikettenkleber auf Glasflaschen. Jährlich werden in Deutschland etwa 8.000 bis 10.000 t Casein eingesetzt.
Die Nutzung von Proteinen aus Blutmehl zur Herstellung von Biokunststoffen (z. B. Pflanztöpfe) befindet sich noch in der Entwicklung, ebenso ein Verfahren zur biotechnologischen Herstellung von Fasern aus Seidenproteinen zur Verarbeitung in Schäumen, Vliesstoffen oder Folien.[8][9]
Etwa 6.000 bis 7.000 t Proteine sind Autolyseprodukte aus Hefen (Hefeextrakte). Diese finden Anwendung vor allem in der Pharmazeutischen Industrie und der Nahrungsmittelindustrie sowie in der Biotechnologischen Industrie als Nährlösung für Mikroorganismen.
Siehe auch
- Membranprotein
- Peptid, Polypeptid, Peptidbindung, Proteindomäne,
- Enzym, Metalloenzym, Metalloprotein, Glykoproteine
- Eiweißsynthese, Proteolyse
- Chaperon, Hitzeschockproteine
- Hefe-Zwei-Hybrid-System, Proteinüberexpression bei Hefen
- Intein
Einzelnachweise
- ↑ DGE: Referenzwerte für die Nährstoffzufuhr
- ↑ DGE: Reference Values for Nutrient Intake, 1. Auflage, Frankfurt/Main, Umschau/Braus, 2000, ISBN 3-8295-7114-3, S. 31
- ↑ Fachagentur Nachwachsende Rohstoffe e. V. (Hrsg.): Daten und Fakten zu nachwachsenden Rohstoffen. Gülzow 2006; Seite 57 (PDF-Download)
- ↑ Ralf Pude, Barbara Wenig: Pflanzen für die Industrie. Pflanzen, Rohstoffe, Produkte. Fachagentur Nachwachsende Rohstoffe e. V., Gülzow 2005; Seite 11. (PDF-Download)
- ↑ Dominik Vogt, Christian Gahle, Michael Karus: Erstellung eines Überblicks zu Marktsituation und Trends zur stofflichen Nutzung nachwachsender Rohstoffe (NR) in Nordrhein-Westfalen. Erstellt durch: nova-Institut GmbH, Hürth 2005.
- ↑ K. Rappold: Gelatine - Ein natürliches Nahrungsmittel. bmi aktuell 1/2004, Hrsg. Informationszentrale für Backmittel und Backgrundstoffe zur Herstellung von Brot und Feinen Backwaren e.V.
- ↑ a b Homepage Gelatine Manufacturers of Europe, Abgerufen 18.09.2008.
- ↑ Verbeek, Johann und van den Berg, Lisa, 2008: Proteinous Bioplastics from Bloodmeal. In: bioplastics magazine 05/2008, S. 30.
- ↑ Geuder, Matthias, 2008: Biopolymere - Rohstoffe, Technologien, Anwendungen. In: Biowerkstoff-Report Okt./Nov./Dez. 2008, S.46. (PDF)
Literatur
- Jeremy M. Berg, John L. Tymoczko, Lubert Stryer: Biochemie. 6. Auflage. Spektrum, Heidelberg 2007, ISBN 3-82-741800-3
- Hubert Rehm: Der Experimentator - Proteinbiochemie/Proteomics. 4. Auflage. Spektrum, Heidelberg 2002, ISBN 3-82-741195-5
Weblinks
- Aminosäuren und Proteine
- Peptide, Polypeptide (Proteine)
- Protein Database (Aminosäurensequenzen, 3D-Strukturen,...)
- Proteinbilder
- Human Protein Atlas - Der Atlas enthält > 1 Million von Pathologen zertifizierte Abbildungen und gibt Auskunft über die Lokalisation und Expression von Proteinen in humanem Normal- und Tumorgewebe.
- Proteopedia Proteopedia ist eine interaktive 3D-Enzyklopädie über Proteine und andere Biomoleküle im Wikipedia-Format. (englisch)
- UniProt enthält Aminosäuresequenzen von und selektive Informationen zu natürlich vorkommenden Proteinen.
Wikimedia Foundation.