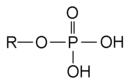
- Esterbindung
-
Ester 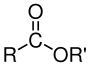
Carbonsäureester
Phosphorsäureester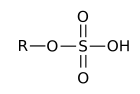
Schwefelsäureester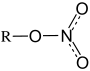
Salpetersäureester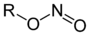
Ester der
Salpetrigen Säure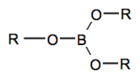
BorsäureesterEster bilden eine Stoffgruppe organischer Verbindungen, die formal oder tatsächlich durch die Reaktion einer Sauerstoffsäure und eines Alkohols unter Abspaltung von Wasser (eine Kondensationsreaktion) entstehen. Es gibt Ester von organischen Säuren (z. B. Carbonsäuren, Sulfonsäuren) und solche von anorganischen Säuren (z. B. Phosphorsäure, Borsäure).
Die Bezeichnung Ester wurde von dem Chemiker Leopold Gmelin im Jahre 1850 aus dem (heute veralteten) Begriff "Essigäther", einem historischen Namen für Ethylacetat, gebildet. Ester wurden zu dieser Zeit ebenfalls als "Äther" bezeichnet (anderes Beispiel: "Salpetersäureäthyläther"). "Äther" wiederum bedeutet (auch heute noch) etwas leicht Flüchtiges (vgl. auch ätherische Öle, Petrolether).
Inhaltsverzeichnis
Carbonsäureester
- Hauptartikel: Carbonsäureester
Carbonsäureester sind Ester der Carbonsäuren mit der funktionellen Gruppe –COOR. Sie setzen sich aus einem Säureteil und einem Alkoholteil zusammen.
Carbonsäureester sind eine in der Organischen Chemie häufig anzutreffende Stoffgruppe.
Phosphorsäureester
- Hauptartikel: Phosphorsäureester
Phosphorsäureester sind Ester der ortho-Phosphorsäure, die formal oder tatsächlich durch die Reaktion der Säure und Alkoholen unter Abspaltung von Wasser entstehen. Nukleinsäuren sind (als Teil ihrer Struktur) Ester der Phosphorsäure mit der Alkoholfunktion von Zuckern (z. B. Ribose oder Desoxyribose). In der Struktur unterscheidet man zwischen Monoester, Diester und Triester der ortho-Phosphorsäure. Unter den Estern der Phosphorsäure und ihren Derivaten sind Verbindungen als potente Insektengifte bekannt (z. B. E605). Unter den Derivaten finden sich auch hochtoxische Verbindungen, wie beispielsweise die chemischen Kampfstoffe Sarin, Tabun und Soman.
Schwefelsäureester
Schwefelsäureester sind Ester der Schwefelsäure. Sie sind in der Natur breit vertreten. (Beispiele: Carrageen; Heparin; die so genannten Sulfatide als Bestandteile der Hirnsubstanz). Salze von langkettigen Monoalkylschwefelsäureestern, häufig bezeichnet als Fettalkoholsulfate, finden Verwendung in kosmetischen Produkten als anionische Tenside (Beispiel: Natriumlaurylsulfat). Dimethylsulfat und Diethylsulfat werden als kraftvolle Reagenzien in der Chemie verwendet, um Methyl- oder Ethylgruppen auf andere Moleküle zu übertragen, sind aber giftig und karzinogen.
Besondere Ester
Es gibt sogar Ester von Säuren, die als freie Säuren instabil sind und nur als Derivate existieren können (z. B. Orthokohlensäureester). Auf der anderen Seite kommt es auch vor, dass die Alkoholkomponente eines Esters als freie Verbindung nicht existiert, da sie sich umlagern würde, und nur durch die Esterverbindung mit einer Säure stabilisiert wird (z. B. Vinylacetat).
Beispiele für Ester einiger weiterer Säuren
- Sulfonsäureester, die sogenannten Sulfonate
- Glycerintrinitrat (Sprengstoff Nitroglycerin)
- Borsäuremethylester (Nachweis von Bor durch grüne Flammenfärbung)
- Kieselsäureester
- Kohlensäurediethylester
Verwendung und Vorkommen
- Bienenwachs besteht hauptsächlich aus Estern des Myricylalkohols (C30H61OH) z. B. Palmitinsäuremyricylester (C15H31–COO–C30H61).
- Weiterhin sind Fette Ester aus Glycerol (Glycerin) und Fettsäuren.
- Zahlreiche Ester werden als Aromastoffe verwendet. Man nennt sie auch Fruchtester. Ethansäure-2-butylester (CH3–COO–C4H9) z. B. riecht nach Apfel, Ethansäure-2-methyl-1-propylester (CH3–COO–C3H7) nach Banane, Ethansäure-2-hexylester (CH3–COO–C6H13) nach Erdbeere.
- Aus dem Celluloseester Cellulosenitrat stellt man rauchloses Treibladungspulver (Schießpulver) her sowie den Kunststoff Celluloid, der heute noch zur Fabrikation von Tischtennisbällen dient.
- Polyester finden Verwendung als Kunststoffe, beispielsweise PET (PolyEthylenTerephthalat), welches zur Herstellung von Lebensmittelverpackungen benutzt wird.
- Ester finden aber auch in Weichmachern Verwendung. Ein Beispiel hierfür wären Ester der Alkylsulfonsäure Mesamoll und der Phthalsäureester Diethylhexylphthalat Weichmacher für PVC.
- Ferner finden Ester in der Medizin Verwendung: der sicher bekannteste ist Acetylsalicylsäure zur Behandlung von Schmerzen, Entzündungen und Fieber. Auch Heroin ist ein Ester der Essigsäure. Amylnitrit ((CH3)2CH–CH2–CH2–O–N=O) wirkt, wie auch andere Alkylnitrite sowie -nitrate, relaxierend auf die glatte Gefäßmuskulatur und wurde früher zur Behandlung akuter Angina pectoris-Anfälle benutzt. Hierfür ist es aber durch Salpetersäureester ersetzt worden. Des weiteren kann es als Methämoglobinbildner bei Cyanidvergiftungen eingesetzt werden.
- Ester kann man aber auch als Insektizid verwenden, z. B. Phosphorsäureester. Dazu gehören Parathion und Dichlorvos.
- Schwefelsäureester, genauer Fettalkoholsulfate, wie z. B. Natriumlaurylsulfat werden als Tenside in Kosmetika verwendet.
- Als Sprengstoff kann Glycerintrinitrat (auch Nitroglycerin, O2NO–CH2–CH(ONO2)–CH2–ONO2) verwendet werden.
- Manche militärische Kampfstoffe sind Ester. Tabun (Dimethylphosphoramidocyanidsäureethylester), Soman (Methylfluorophosphonsäure-1,2,2-trimethylpropylester), Sarin (Methylfluorphosphonsäureisopropylester) sind solche Ester.
- Phorbolester sind im Saft von Wolfsmilchgewächsen enthalten und können neben ausgeprägten Hautverätzungen und Gastroenteritiden auch maligne Tumore auslösen. Die karzinogene, also krebsfördernde Wirkung scheint durch Stimulation der Proteinkinase C zustande zu kommen, die das Wachstumsverhalten der Krebszellen modifiziert.
Wikimedia Foundation.