- Fettsäureabbau
-
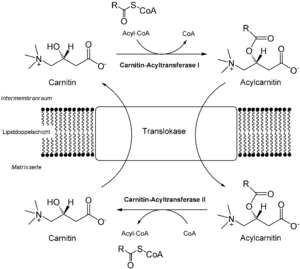 Damit die an Carnitin gebundene Fettsäure (Acylcarnitin) vom Intermembranraum in die Mitochondrienmatrix gelangen kann, wird eine Translokase benötigt. Die Carnitin- Acyltransferase I (auch als Carnitin-Palmitoyltransferase I bekannt) ist an der äußeren Mitochondrienmembran, die Carntin-Acyltransferase II (oder Carnitin- Palmitolytransferase II) an der inneren Mitochondrienmembran lokalisiert. Die Größenverhältnisse in der Abbildung sind nicht maßstabsgerecht.
Damit die an Carnitin gebundene Fettsäure (Acylcarnitin) vom Intermembranraum in die Mitochondrienmatrix gelangen kann, wird eine Translokase benötigt. Die Carnitin- Acyltransferase I (auch als Carnitin-Palmitoyltransferase I bekannt) ist an der äußeren Mitochondrienmembran, die Carntin-Acyltransferase II (oder Carnitin- Palmitolytransferase II) an der inneren Mitochondrienmembran lokalisiert. Die Größenverhältnisse in der Abbildung sind nicht maßstabsgerecht.Als β-Oxidation bezeichnet man den biochemischen Abbaumechanismus der Fettsäuren. Die Bezeichnung bezieht sich auf die ersten drei Reaktionsschritte, bei denen eine Oxidation am Beta-C-Atom (Cβ) stattfindet.
Die β-Oxidation wurde schon 1904 von Franz Knoop in Freiburg entdeckt. Erst 50 Jahre später indes wurde der genaue Mechanismus dieses Stoffwechselweges aufgeklärt. Die β-Oxidation erfolgt bei tierischen Zellen in den Mitochondrien, bei Pflanzlichen Zellen in den Peroxisomen.
Inhaltsverzeichnis
Schrittweiser Abbau
Der Abbau der Fettsäuren erfolgt, wie auch der Aufbau, schrittweise. Dies geschieht in einer sich wiederholenden Abfolge von 4 Einzelreaktionen.
Aktivierung
Bevor die β-Oxidation stattfinden kann, muss die abzubauende Fettsäure zunächst an das Coenzym A gebunden werden, dies geschieht im Cytoplasma. Im ersten Schritt der Aktivierung wird ATP zu AMP und Pyrophosphat gespalten, welches durch eine Pyrophosphatase weiter in Orthophosphat gespalten wird. AMP reagiert im darauf folgenden Schritt mit der Fettsäure zu Acyl-Adenylat. Im weiteren Reaktionsschritt kann die Fettsäure unter Abspaltung des AMP durch die frei werdende Energie mit dem Coenzym A verestert werden. Die so aktivierte Form der Fettsäure nennt man Acyl-CoA. Beide Reaktionen werden von einer von mehreren Fettsäure-CoA-Ligasen katalysiert.
Die folgenden Reaktionen finden in der Mitochondrienmatrix statt. Langkettige Fettsäuren können nicht selbstständig vom Cytoplasma durch die Mitochondrienmembranen diffundieren und werden daher, an Carnitin gebunden, in Form von Acyl-Carnitin, dorthin transportiert.
Abbau an der inneren Mitochondrienmembran
Nun beginnt der eigentliche Abbau:
- 1)

- An dem Acyl-CoA wird durch das Enzym Acyl-CoA-Dehydrogenase zwischen Kohlenstoffatom 2 (Cα) und 3 (Cβ) eine trans-Doppelbindung geknüpft. Dabei wird ein FAD zu FADH2 reduziert.
- 2)
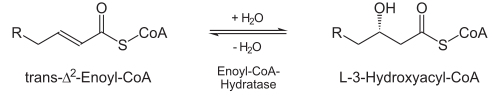
- Durch die Enoyl-CoA-Hydratase wird stereospezifisch Wasser an die neu entstandene Doppelbindung addiert. Es entsteht hierdurch L-3-Hydroxyacyl-CoA (auch: L-β-Hydroxyacyl-CoA).
- 3)
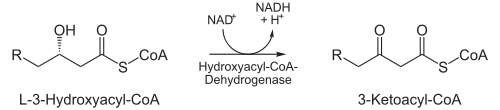
- In der nächsten Reaktion wird die C3-Hydroxylgruppe durch L-3-Hydroxylacyl-CoA-Dehydrogenase (auch: β-Hydroxylacyl-CoA-Dehydrogenase) zu einer Ketofunktion oxidiert. Dabei wird ein NAD+ zu NADH + H+ reduziert. Dieser Schritt ist der namensgebende für den gesamten Mechanismus.
- 4)
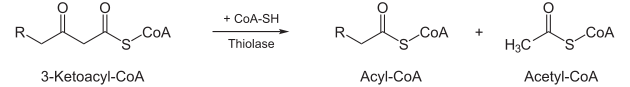
- Unter Aufnahme eines Coenzym A spaltet das Enzym Thiolase Acetyl-CoA (aktivierte Essigsäure) ab, und ein um zwei Kohlenstoffatome verkürztes Fettsäuremolekül (in Form von Acyl-CoA) bleibt zurück, welches wieder dem ersten Schritt zugeführt werden kann.
- Diese Reaktionsabfolge wiederholt sich so lange, bis zum Schluss zwei Acetyl-CoA übrigbleiben.
Das gebildete Acetyl-CoA kann zum weiteren Abbau in den Citrat-Zyklus einfließen oder zur Synthese von Ketokörpern dienen. FADH2 und NADH/H+ werden der Atmungskette zugeführt. Dort können daraus, durch Elektronentransportphosphorylierung, ATP regeneriert werden (1,5 im Fall von FADH2 und 2,5 aus NADH/H+).
Mittels der „normalen“ β-Oxidation lassen sich nur gesättigte Fettsäuren abbauen. Zum Abbau ungesättigter Fettsäuren sind weiterhin die Enzyme cis-Δ3-Enoyl-CoA-Isomerase und 2,4 Dienoyl-CoA-Reduktase vonnöten. Ein Sonderfall stellt die α-Oxidation dar, über die Phytansäure in Säugetieren abgebaut werden kann.
Der Abbau von Fettsäuren ist eine Reaktionsfolge, bei der sehr viel für den Körper nutzbare Energie frei wird. Bei einem vollständigem Abbau von einem Molekül Palmitat (durch β-Oxidation, Citrat-Zyklus und Atmungskette) werden etwa 98 bis 106 Moleküle ATP gebildet. Im Vergleich dazu entstehen bei dem Abbau von einem Molekül Glucose im statistischen Mittel nur etwa 30 Moleküle ATP.
Literatur
- Biochemie, Berg/Tymoczko/Stryer, 5. Auflage, Spektrum Akademischer Verlag GmbH Heidelberg 2003, ISBN 3827413036
Siehe auch
Weblinks
- 1)
Wikimedia Foundation.
