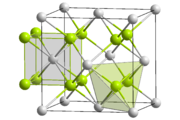
- Fluorit-Gitter
-
Fluorit violetter Fluorit aus Chiny Chemische Formel CaF2 Mineralklasse Halogenide
III/A.08-10 (nach Strunz)
9.2.1.1 (nach Dana)Kristallsystem kubisch Kristallklasse hexakisoktaedrisch 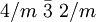
Farbe in reiner Form farblos, gelb, grün, rot, violett auch schwärzlich Strichfarbe weiß Mohshärte 4 Dichte (g/cm³) 3,2 Glanz Glasglanz Transparenz durchsichtig bis undurchsichtig Bruch muschelig bis splittrig Spaltbarkeit vollkommen nach {111} Habitus Kubische Kristalle und ihre Kombinationen; körnige, massige Aggregate Häufige Kristallflächen {001}, {111} Zwillingsbildung Durchkreuzungszwillinge nach (111) Kristalloptik Brechzahl n=1,433 bis 1,448 Doppelbrechung
(optische Orientierung)keine Weitere Eigenschaften Chemisches Verhalten wird durch Schwefelsäure gelöst Radioaktivität manchmal durch eingewachsene Uranminerale Magnetismus nicht magnetisch Besondere Kennzeichen blaue bis blaugrüne Fluoreszenz, gelegentlich Phosphoreszenz Fluorit oder Flussspat ist ein sehr häufig vorkommendes Mineral aus der Mineralklasse der einfachen Halogenide. Es kristallisiert im kubischen Kristallsystem mit der chemischen Zusammensetzung CaF2 und entwickelt meist kubische Kristalle in Form von Würfeln oder Oktaedern, aber auch körnige, massige Aggregate. Chemisch gesehen handelt es sich bei Fluorit um Calciumfluorid.
Inhaltsverzeichnis
Besondere Eigenschaften
 Blaue Fluoritkristalle aus Mailand
Blaue Fluoritkristalle aus MailandReiner Fluorit ist farblos und transparent, durch Verunreinigungen auch grau. Er kann aber durch Fremdbeimengungen fast alle Farben, wenn auch meist in schwacher Intensität, annehmen. Sehr verbreitet sind grüne, violette bis schwarzviolette und gelbe Farben, aber auch blaue, rote und braune Fluorite werden gefunden.
Durch Einlagerung von Lanthanoiden, zum Beispiel Eu2+, kann Fluorit unter Anregung mit UV-Licht starke Fluoreszenz zeigen, gelegentlich sogar Phosphoreszenz. [1]
Fluorit hat eine Mohssche Härte von 4 und eine sehr variable, oft violette oder grüne Farbe, ist manchmal aber auch farblos. Die dunkle Färbung vieler Fluorite entsteht durch eingelagerte seltene Erden oder radioaktive Bestrahlung des Flussspats (Stinkspat), wobei auch eingewachsene Uranminerale die Färbung verstärken können; die Strichfarbe ist weiß. Kristalle mit würfeligem Habitus sind häufig, oft findet man Durchdringungszwillinge.
Etymologie und Geschichte
Flussspat war schon im antiken Griechenland bekannt. Der deutsche Name geht auf die erwähnte Verwendung als Flussmittel in der Metallverarbeitung zurück. 1824 entdeckte der deutsche Mineraloge Friedrich Mohs die im ultravioletten Licht sichtbar werdende Fluoreszenz. Der irische Mathematiker und Physiker George Gabriel Stokes benannte das Phänomen der Fluoreszenz nach dem Fluorit in Analogie zur Opaleszenz zum Opal. [2]
Bildung und Fundorte
Fluorit kommt meist massiv, gelegentlich auch in kristalliner Form vor und entsteht primär in pneumatolytischen Gängen, also Gängen, die durch ein Entweichen mobiler Phasen beim Abkühlen eines Magmas entstehen und sind oft mit Baryt, Quarz, Topas, Calcit, Bleiglanz und Zinkblende assoziiert. Er bildet gelegentlich auch Nebengemengteil in Graniten, Karbonatiten und anderen magmatischen Gesteinen wie Pegmatiten.
Der weltweit größte Flussspat-Bergbau findet sich in Mexiko, in der Lagerstätte Las Cuevas, die vulkanischen Ursprungs ist. Weitere reichhaltige Flussspat-Lagerstätten liegen in China, im indischen Amba Dongar, in Südafrika (Zwartkloof sowie Witkop im Transvaal), in Namibia (Okorusu), im kenianischen Kario Valley und in den US-amerikanischen Bundesstaaten Illinois und Kentucky. Eine bekannte Fundstätte des Flussspats in Europa ist Castleton, im englischen Peak District, wo es unter dem Namen „Blue John“ bekannt ist und für die Schmuckherstellung abgebaut wird. Der Name ist eine Verballhornung des Französischen „bleu et jaune“, bedeutet also etwa „blau-gelb“. Deutsche Lagerstätten sind zum Beispiel die Grube Clara bei Wolfach im Schwarzwald und die Grube Käfersteige bei Pforzheim; daneben findet sich Fluorit auch im Oberpfälzer Wald (Umgebung von Nabburg) sowie im Schortetal bei Ilmenau im Thüringer Wald (siehe auch: Schaubergwerk Volle Rose).
Struktur
Fluorit kristallisiert im kubischen Kristallsystem in der höchstsymmetrischen Kristallklasse
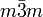 (kubisch-hexakisoktaedrisch) beziehungsweise der Raumgruppe
(kubisch-hexakisoktaedrisch) beziehungsweise der Raumgruppe 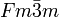 . In der Kristallstruktur bilden die Ca2+-Ionen eine kubisch dichtestete Kugelpackung, die einem kubisch flächenzentrierten Gitter (fcc, face centered cubic) entspricht. Die Flächenzentrierung der Elementarzelle (siehe Bild links) kann auch aus dem Raumgruppensymbol abgelesen werden („F“). Die Fluoridionen (F−) besetzen alle Tetraederlücken der dichtesten Kugelpackung aus Calciumionen. Da in einer dichtesten Kugelpackung immer doppelt so viele Tetraederlücken wie Packungsteilchen enthalten sind, ergibt sich in der Struktur ein Calcium-Fluor-Verhältnis von 1:2, was sich auch in der chemischen Formel des Fluorits, CaF2, widerspiegelt. Als Koordinationspolyeder ergibt sich für die Fluoridionen dadurch ein Tetraeder aus vier Calciumionen, die Calciumionen ihrerseits werden von acht Fluoratomen in Form eines Würfels umgeben.
. In der Kristallstruktur bilden die Ca2+-Ionen eine kubisch dichtestete Kugelpackung, die einem kubisch flächenzentrierten Gitter (fcc, face centered cubic) entspricht. Die Flächenzentrierung der Elementarzelle (siehe Bild links) kann auch aus dem Raumgruppensymbol abgelesen werden („F“). Die Fluoridionen (F−) besetzen alle Tetraederlücken der dichtesten Kugelpackung aus Calciumionen. Da in einer dichtesten Kugelpackung immer doppelt so viele Tetraederlücken wie Packungsteilchen enthalten sind, ergibt sich in der Struktur ein Calcium-Fluor-Verhältnis von 1:2, was sich auch in der chemischen Formel des Fluorits, CaF2, widerspiegelt. Als Koordinationspolyeder ergibt sich für die Fluoridionen dadurch ein Tetraeder aus vier Calciumionen, die Calciumionen ihrerseits werden von acht Fluoratomen in Form eines Würfels umgeben.Verwendung
als Rohstoff
Industriell wird Fluorit hauptsächlich als Flussmittel in der Metallindustrie und zur Herstellung von Fluor und Fluorwasserstoffsäure verwendet. Daneben ist Fluorit ein beliebter Schmuckstein und dient als Grundstoff für optische Linsen und opaleszierende Gläser.
Durch die Eigenschaft das Lichtspektrum gleichmäßig zu brechen lässt sich die Chromatische Aberration von Objektiven ausgleichen. Problematisch ist hier, dass für Hochleistungsobjektive besonders große Kristalle benötigt werden, diese werden künstlich gezüchtet. Kristalle dieser Größe haben die Eigenschaft, sich durch Hitze (durch Sonneneinstrahlung) bereits derart zu verziehen, dass sie die Rechnung der Optik signifikant verändern.
als Schmuckstein
Aufgrund seiner eher geringen Härte ist Fluorit als Schmuckstein für die gewerbliche Schmuckindustrie eher uninteressant. Gelegentlich wird er von Glyptikern zu kleinen, kunstgewerblichen Gegenständen verarbeitet. Da er aber durch seine Farbenvielfalt mit vielen Edelstein-Mineralen verwechselt werden kann, dient er oft als Grundlage für Imitationen (siehe auch Schmuckstein).
Stinkspat
Stinkspat wird die durch radioaktive Strahlung veränderte Kristallart von Fluorit bezeichnet. Durch die ionisierende Strahlung wird ein Elektron der Verbindung so angeregt, dass es die Elektronenhülle verlassen und auf einer Gitterdefektstelle (umgeben von vier Calciumatomen, sogenanntes F-Zentrum) durch Energieabgabe ein geringeres Energieniveau einnehmen kann. Die CaF2-Formeleinheit, aus der das Elektron entfernt wurde liegt nun als metallisches Calcium (Ca) und Fluorgas (F2) vor. Aufgrund der Elektronen in den F-Zentren (Gitterdefektstellen aufgrund eines fehlenden Fluoridions) und dem kolloidalen Calcium ist Stinkspat (im Gegensatz zum weiß-durchsichtigen Flussspat) dunkelblau, -violett bis schwarz und undurchsichtig (z.B. Wölsendorfer Stinkspat aus der Oberpfalz). Stinkspat kommt oft (aber nicht immer) zusammen mit Uranmineralien vor, die teilweise als feinste Partikel im Stinkspat eingeschlossen sein können (Radioaktivität!).
Stinkspat weist neben seinem Aussehen i. d. R. auch die folgenden zwei Merkmale auf:
- Durch Reiben/Schlagen des Kristalls wird das gasförmige und giftige Fluor freigesetzt, welches in Verbindung mit H2O (z.B. Luftfeuchtigkeit) zu 2HF und ½ O2 reagiert. Der radikalische atomare Sauerstoff (½ O2) wiederum verbindet sich mit dem molekularen Luftsauerstoff (O2) zu dem stark riechenden Ozon (O3), woher diese Verbindung ursprünglich ihre Bezeichnung hat.
- Durch Erhitzen des Stinkspates kann dem (F-Zentrum-)Elektron wieder genügend Energie zugeführt werden, sodass dieses unter Abgabe elektromagnetischer Strahlung im sichtbaren Bereich (Licht) in die Elektronenhülle eines Fluoratoms zurückkehrt. Aufgrund der Wiederherstellung des Flussspatkristalls verliert die wärmebehandelte Probe dabei auch ihre Farbe, bis sie weiß-durchsichtig ist.
Siehe auch
Einzelnachweise
- ↑ Edition Dörfler: Mineralien Enzyklopädie. Nebel Verlag, ISBN 3-89555-076-0
- ↑ Stokes G. G. (1852) Phil. Trans. 142, 463-562
Literatur
- Walter E. Tröger u.a. (Hrsg.): Optische Bestimmung gesteinsbildender Minerale, Schweizerbart, Stuttgart
- 1. - Bestimmungstabellen, 1982, ISBN 3-510-65106-5
- Martin Okrusch, Siegfried Matthes: Mineralogie. 7. Auflage. Springer Verlag, Berlin 2005, ISBN 3-540-23812-3
- Walter Schumann: Edelsteine und Schmucksteine. 13. Auflage. BLV Verlags GmbH, 1976/1989, ISBN 3-405-16332-3
Weblinks
- Mineralienatlas:Fluorit (Technische Informationen), Mineralienatlas:Mineralienportrait/Fluorit (Umfassendes Portrait)
- Flussspat aus Wölsendorf
- MinDat - Fluorite (engl.)
- Webmineral (engl.)
Wikimedia Foundation.