- Grenzflächenenergie
-
Grenzflächenspannung bezieht sich auf Kräfte, die zwischen zwei verschiedenen Phasen auftreten, die miteinander in Kontakt stehen. Sie bilden eine gemeinsame Grenzfläche, die unter Grenzflächenspannung steht. Phasen können flüssig, fest oder gasförmig sein. Unter verschiedenen Phasen versteht man Phasen, die sich nicht vermischen, wie z. B. Wasser und Öl oder Glas und Wasser. Grenzflächenspannung zwischen Flüssigkeiten und Gasphasen bezeichnet man meist als Oberflächenspannung.
Inhaltsverzeichnis
Phänomene
Die Grenzflächenspannung beschreibt die Gründe, warum …
- Wasser gerne Tropfen bildet (→ Tropfen);
- die Oberfläche einer Flüssigkeit in einem Reagenzglas eine Wölbung zeigen kann (→ Meniskus);
- Flüssigkeiten in einem Glasröhrchen ein Stück aufsteigen können, wenn ein Ende des Röhrchen senkrecht in die Flüssigkeit getaucht wird (→ Kapillarität);
- einige Insekten über das Wasser laufen können (→ Wasserläufer);
- von einer leichten, dünnen Regenjacke das Wasser abperlen kann (→ Benetzung).
Grenzflächenspannung ist „Grenzflächenenergie“ bzw. „Grenzflächenarbeit“
Grenzflächenspannung scheint eine Kraft zu sein, kann aber leichter als Grenzflächenarbeit oder Grenzflächenenergie verstanden werden. Sie beschreibt die Energie die umgesetzt werden muss, um die Grenzfläche um 1 m2 unter isothermen Bedingungen zu vergrößern.
In der Praxis spricht man häufig von Grenzflächenspannung, wenn Arbeit aufgewendet werden müsste, um die Grenzfläche zu vergrößern bzw. Energie freigesetzt wird, wenn sich die Fläche verkleinert. Ein System wie Wasser/Luft strebt aus diesen energetischen Gründen eine möglichst kleine Grenzfläche an. Das Wasser bildet Tröpfchen und nimmt nicht „freiwillig“ die Form eines Tellers an.
Phase und Phasengrenze
Innerhalb einer Phase wirken auf die die Phase bildenden Teilchen Kräfte in alle Raumrichtungen (Kohäsion). Bei den Teilchen kann es sich um Moleküle, Metallatome oder die Ionen eines Salzes handeln. Im Inneren der Phase heben sich die Kräfte gegeneinander auf. An der Phasengrenze ist das nicht der Fall. Hier fehlen Nachbarn, die zur eigenen Phase gehören.
Bei einer flüssigen Phase von Wasser (Abb. 1) wirken auf die Moleküle Dipol-Dipol-Momente in alle Raumrichtungen. An der Phasengrenze (Rand eines Tröpfchens) ist das nicht der Fall. Ein Wassermolekül am Rand hat viel weniger Nachbarn. Ein Wassermolekül, das sich aus dem Inneren der Phase an die Phasengrenze bewegt, muss über die Energie verfügen, um einen Teil der Dipol-Dipol-Momente zu überwinden. Bewegt es sich in die andere Richtung, wird entsprechende Energie frei. Um die Fläche der Phasengrenze zu vergrößern, muss Energie aufgewendet werden, da nun mehr Teilchen zur Bildung der größeren Fläche nötig werden. Daher strebt Wasser eine minimale Oberfläche an und bildet somit Tröpfchen.
Richtung der Grenzflächenspannung
Bei einer Seifenblase (Abb. 2) wird die Phase „Blasenhaut“ von beiden Seiten von je einer Gasphase begrenzt. Die zwei Grenzflächen der „Blasenhaut“ spannen die innere Gasphase zusammen. Die Kräfte wirken in der Richtung der Ausdehnung der Blasenhaut. Diese Richtung wird deutlicher, wenn man Abbildung 3 betrachtet. Sie entspricht einem Querschnitt durch Schaum. Die „Blasenhäute“ nehmen die kürzeste Verbindungslinien (Geraden) aufgrund der Richtung der Grenzflächenspannung ein.
Grenzfläche Flüssigkeit-Luft-Wand
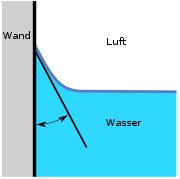
Berührt eine Grenzfläche Luft-Flüssigkeit eine feste Wand, stellt sich ein bestimmter Winkel zwischen Wand und Oberfläche der Flüssigkeit ein. Abbildung 4 zeigt diesen Kontaktwinkel für einen Fall einer senkrechten Wand, die sich gut benetzen lässt. Je stärker die Benetzung ist, desto kleiner wird der Winkel und umso höher steigt der obere Rand der Flüssigkeit. Dieses Verhalten in engen Röhren nennt man Kapillareffekt. Der Benetzungsgrad ist abhängig von der Art der Flüssigkeit, vom Material der Oberfläche und deren Beschaffenheit, wie z. B. seiner Rauigkeit.
Beeinflussbarkeit der Grenzflächenspannung
Wikimedia Foundation.



.jpg)