- 2-Aminobenzolcarbonsäure
-
Strukturformel 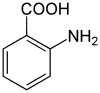
Allgemeines Name Anthranilsäure Andere Namen - 2-Aminobenzoesäure
- o-Aminobenzoesäure
- 2-Carboxyanilin
Summenformel C7H7NO2 CAS-Nummer 118-92-3 PubChem 227 Kurzbeschreibung geruchloses weißes kristallines Pulver Eigenschaften Molare Masse 137,14 g·mol−1 Aggregatzustand fest
Dichte 1,41 g·cm−3 [1]
Schmelzpunkt 146–148 °C [1]
Siedepunkt Zersetzung ab 200 °C [1]
Dampfdruck pKs-Wert 2,05 [2]
Löslichkeit schlecht in Wasser (5,72 g/l bei 25 °C) [1]
Sicherheitshinweise Gefahrstoffkennzeichnung [1] 
Reizend (Xi) R- und S-Sätze R: 36 S: keine S-Sätze WGK 1 [1] Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Anthranilsäure (2-Aminobenzoesäure, o-Aminobenzoesäure) ist eine aromatische, farblose bis blassgelbe, blau fluoreszierende Aminosäure, die als Zwischenprodukt für Farbstoffe, Pharmazeutika, Kosmetika, Fotografische- und Feinchemikalien, Schmierstoffadditive und Korrosionsschutzmittel verwendet wird.
Neben der Anthranilsäure existieren zwei weitere stellungsisomere Formen: die 3-Aminobenzoesäure (m-Aminobenzoesäure) und die 4-Aminobenzoesäure (p-Aminobenzoesäure).
Inhaltsverzeichnis
Geschichte
Anthranilsäure wurde 1841 von Carl Julius Fritzsche (1808–1871) beim alkalischen Abbau von Indigo entdeckt.
Herstellung
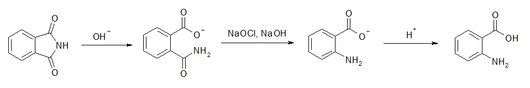
Eine technische Herstellung von Anthranilsäure erfolgt durch eine Hofmann-Umlagerung von Phthalimid in Gegenwart von Natriumhydroxid und Natriumhypochlorit.[3]
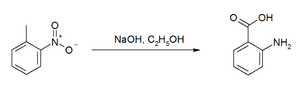
Eine weitere Herstellung gelingt durch eine intramolekulare Redoxreaktion aus 2-Nitrotoluol.[3]
Verwendung
Anthranilsäure dient weiterhin als Ausgangsstoff für die Synthese von Anthranilsäurederivaten, die wegen ihrer Ähnlichkeit zur Salicylsäure als Nichtopioid-Analgetika genutzt werden. Anthranilsäure selbst hat diese Wirkung nicht. Die Ausfuhr des Stoffes aus Deutschland ist teilweise erlaubnispflichtig (siehe Grundstoffüberwachungsgesetz), da sie als Ausgangsstoff für süchtigmachende Substanzen dienen kann.
Anthranilsäure spielt heute als Ausgangsmaterial für die Synthese der als Riechstoffe bedeutenden Anthranilsäureester und von Indigo sowie von Arzneistoffen und Pflanzenschutzmitteln (Akarizide) eine wichtige Rolle. Anthranilsäure kann zur Bestimmung und zum Nachweis von Ag, Cd, Ce, Co, Cu, Hg, Mn, Ni, Pb, Pd, U und Zn genutzt werden.
Weblinks
- Synthesis of Heterocycles from Anthranilic acid and its Derivatives
- Synthese und Cyclisierung von Anthranilohydroxamsäuren
Einzelnachweise
- ↑ a b c d e f g Eintrag zu Anthranilsäure in der GESTIS-Stoffdatenbank des BGIA, abgerufen am 29. Dezember 2007 (JavaScript erforderlich).
- ↑ CRC Handbook of Tables for Organic Compound Identification, Third Edition, 1984, ISBN 0-8493-0303-6.
- ↑ a b S. Hauptmann, J. Graefe, H. Remane: Lehrbuch der Organischen Chemie, VEB Deutscher Verlag für Grundstoffindustrie, Leipzig 1980
Wikimedia Foundation.