- Methylhalogenid
-
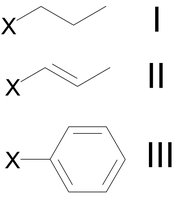 Struktur der verschiedenen Klassen monohalogenierter Kohlenwasserstoffe:
Struktur der verschiedenen Klassen monohalogenierter Kohlenwasserstoffe:
I=Halogenalkan (Halogenpropan), II=Halogenalken (Halogenpropen), III=Halogenaromat (Halogenbenzol); X=Fluor, Chlor, Brom oder IodAls Halogenkohlenwasserstoffe oder halogenierte Kohlenwasserstoffe, manchmal kurz auch Halone, werden Kohlenwasserstoffe bezeichnet, die zusätzlich zu Kohlenstoff und Wasserstoff noch eines oder mehrere der Halogene Fluor, Chlor, Brom oder Iod enthalten. In der organischen Chemie werden monohalogenierte Kohlenwasserstoffe mit R-X abgekürzt, wobei der Rest R für einen Alkyl- oder Aryl-Rest und das X für ein Halogenatom steht.
Inhaltsverzeichnis
Eigenschaften und Risiken
Die Halogenkohlenwasserstoffe sind stabile, lipophile (fettlösliche) Substanzen, die vielfach hervorragende organische Lösungsmittel sind. Sie kommen als teilweise extrem wirksame Gifte als Insektizide zum Einsatz. Deswegen werden sie weltweit in großen Mengen produziert. Trotz dieser in vielen Bereichen ausgezeichneten Eigenschaften stehen einige im Verdacht krebserregend zu sein. Auch akut nicht allzu toxische Verbindungen rufen Spätfolgen hervor, da sie sich durch ihre hohe Stabilität und ihren lipophilen und damit hydrophoben Charakter in der Fettschicht von Mensch und Tier anreichern. Bestimmte Halogenkohlenwasserstoffe wie DDT und seine Abbauprodukte DDE und DDD, Chlordan und 3,4-Dichloranilin scheinen auch durch Ähnlichkeit mit Steroiden in das Hormonsystem höherer Tiere einzugreifen. So wurden bei Fischen und Amphibien Geschlechtsumwandlungen entdeckt.[1] Bei amerikanischen Dickkopfelritzen (Pimephales promelas) verminderten natürliche und künstliche Östrogene die Spermienproduktion der Männchen und führten so zu einer starken Verringerung des Fischbestands.[2] Halogenkohlenwasserstoffe werden außerdem teilweise für den Abbau der Ozonschicht verantwortlich gemacht.
Darstellung und Vorkommen
Durch nukleophile oder radikalische Substitution bzw. durch Additionsreaktionen kann ein Halogen-Atom in eine Kohlenwasserstoffverbindung eingebaut werden:
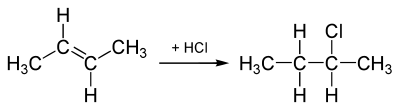 Beispiel einer Addition von Chlorwasserstoff an 2-Buten. Dadurch entsteht 2-Chlorbutan, ein Chlorkohlenwasserstoff
Beispiel einer Addition von Chlorwasserstoff an 2-Buten. Dadurch entsteht 2-Chlorbutan, ein ChlorkohlenwasserstoffDie Halogenkohlenwasserstoffe werden zum größten Teil künstlich hergestellt. Es existieren jedoch auch viele natürliche halogenierte Kohlenwasserstoffe (ca. 3.800 sind bekannt), wie z.Bsp. Purpur (Dibromindigo), Mono- und Diiodtyrosin, Chloramphenicol und Methylchlorid.[3] Viele dieser Stoffe werden von Bakterien als natürliche Antibiotika produziert. Der Mensch und viele andere Tiere bilden von Diiodthyrosin ausgehend das Schilddrüsenhormon Thyroxin, welches pro Molekül vier Atome Iod enthält.
siehe auch:
Einteilung
Aliphatische Halogenkohlenwasserstoffe
Die bei aliphatischen Halogenkohlenwasserstoffen verwendeten Halogene sind meist Fluor und Chlor. Man unterscheidet zwischen vollhalogenierten Halogenkohlenwasserstoffen (Fluorchlorkohlenwasserstoffe, FCKW) und teilhalogenierten Halogenkohlenwasserstoffen (H-FCKW).
Halogenalkane
Halogenalkane leiten sich von der Gruppe der Alkane ab. Sie bestehen aus gesättigten Kohlenwasserstoffmolekülen, bei denen ein oder mehrere Wasserstoffatome durch Elemente der 7. Hauptgruppe (Halogene) des Periodensystems ersetzt wurden.
Halogenalkane haben eine höhere Siedetemperatur als das jeweils entsprechende Alkan, da Halogenalkanmoleküle untereinander eine stärkere Wechselwirkung haben. Diese resultiert aus der stärkeren Elektronegativität von Halogenen gegenüber Wasserstoff. Bei Halogenalkanen gibt es deshalb neben den Van-der-Waals-Kräften auch schwache Dipolkräfte (Dispersionskräfte und Dipol-Dipol-Kräfte).
Halogenalkane (Halogenkohlenwasserstoffe) sind oft hervorragende Lösungsmittel für Stoffe, welche sich im Wasser nicht lösen. Außerdem können sie zur Entfettung von Metalloberflächen in der Metallverarbeitung genutzt werden.
In der chemischen Industrie werden sie als Ausgangsstoff zur Herstellung von diversen anderen Produkten verwendet. Dies beruht darauf, dass Halogenide oft gute Abgangsgruppen bei SN1- oder SN2-Substitutionen sind. Halogenalkane dienen auch zur Herstellung von Ethern aus Alkoholaten (Williamsonsche Ethersynthese).
Einige Halogenalkane sind krebserregend, oder stehen im Verdacht, krebserregend zu sein. Bei starker akuter wie auch bei chronischer Exposition rufen sie auch schwere Organschäden an Leber und Niere hervor. Zu diesen zählen besonders das 1,2-Dichlorethan, das Tetrachlormethan, das Chloroform, das Dichlormethan, sowie Halogenalkane, die gute Alkylierungsmittel sind, wie z. B. das Iodmethan.
Mehrfach halogenierte Alkane dürfen keinesfalls mit Alkalimetallen oder stark basischen Trocknungsmitteln behandelt werden, da es zu spontaner, explosionsartiger Zersetzung kommen kann.
Wichtige Halogenalkane:
- Chloroform (CHCl3) früher als Narkosemittel, heute als Lösungsmittel;
- Tetrachlormethan (CCl4) als Lösungsmittel und früher auch als Feuerlöschmittel;
- Hexachlorethan jahrelang als chlortragender Feststoff an Stelle von Risiken bergendem Chlorgas zur Raffination von primärem, aus der Elektrolyse entnommenem Metall, aber auch im Gießereibereich zur Wasserstoffentfernung und Ausspülung von in der Schmelze suspendierten Oxiden eingesetzt;
- Trichlorfluormethan, FCKW (CCl3F) als Treibgas bzw. Kühlmittel;
- Halothan (C2HBrClF3) als Inhalationsnarkotikum
Halogenalkene
Halogenalkene leiten sich von der Gruppe der Alkene ab. Sie bestehen aus ungesättigten Kohlenwasserstoffmolekülen, bei denen ein oder mehrere Wasserstoffatome durch Elemente der 7. Hauptgruppe (Halogene) des Periodensystems ersetzt wurden.
Sie besitzen trotz ihrer teilweisen Giftigkeit vielfältige Einsatzmöglichkeiten in der chemischen Industrie, vor Allem bei der Herstellung von Kunst- und Arzneistoffen.
Wichtige Halogenalkene:
- Vinylchlorid ist die Ausgangssubstanz zur Herstellung von PVC,
- 1,1-Dichlorethen wird zum Polyvinylidenchlorid (PVdC) verarbeitet,
- 2,2-Dichlorvinyl-dimethyl-phosphat (Dichlorvos) ist ein 1951 eingeführtes Insektizid,
- Clobetasol und Betamethason sind Medikamente auf Steroid-Basis,
- Halomon ist ein in Rotalgen vorkommendes Anti-Tumor-Medikament.
Aromatische Halogenkohlenwasserstoffe
Aromatische Halogenkohlenwasserstoffe (auch Halogenarene) leiten sich von der Gruppe der Aromaten oder Arene ab, bei denen ein oder mehrere Wasserstoffatome durch Elemente der 7. Hauptgruppe (Halogene) des Periodensystems ersetzt wurden.
Die meisten aromatischen Halogenverbindungen sind hochgiftig und werden oder wurden als Insektizide oder Fungizide eingesetzt. Viele davon sind mittlerweile verboten.
Wichtige Halogenaromaten:
- Chlorbenzol, ein wichtiges Lösungsmittel für Öle, Fette, Harze usw.,
- 2-Chlorphenol, ein Desinfektionsmittel,
- CS-Gas, ein Tränengas,
- DDT, ein in den meisten westlichen Industrieländern seit den 1970er Jahren verbotenes Insektizid,
- Decabromdiphenylether und Tetrabrombisphenol A sind Flammschutzmittel,
- Eosin, ein roter Farbstoff, der aus Steinkohleteer gewonnen wird,
- Merbromin (INN) ein dem Eosin ähnlicher Farbstoff, der früher (vor 2003) in Deutschland als Antiseptikum (Handelsname Mercurochrom®) vertrieben wurde.
Verwendung
Von Methan und Ethan leiten sich eine Reihe von Halogenalkanen ab, die in Technik und Alltag vielfältig Verwendung finden. Chloralalkane sind gebräuchliche Lösungsmittel für Fette und Harze: Dichlormethan und Trichlormethan (Chloroform) werden beispielsweise zum Extrahieren pflanzlicher Öle und zum Entfetten von Metallteilen verwendet. Trichlorethan wird bei der "chemischen Reinigung" als Kleiderbad eingesetzt.
Die mengenmäßig wichtigsten Halogenkohlenwasserstoffe sind die Chlorkohlenwasserstoffe (CKW), Fluorkohlenwasserstoffe (FKW) und die Fluorchlorkohlenwasserstoffe (FCKW). Zunehmend werden Bromkohlenwasserstoffe als Flammschutzmittel verwendet. Viele Halogenkohlenwasserstoffe wirken als ozonabbauende Verbindungen und/oder als Treibhausgase. Die Verwendungsbereiche für Halogenkohlenwasserstoffe in der nachfolgenden Auflistung sind heute weitgehend verboten oder durch Restriktionen und zeitlich begrenzte Verwendungszulassung stark eingeschränkt worden.
- Antibiotika
- Sehr viele antibiotisch wirkende Stoffe enthalten Halogenatome (z.Bsp. Chloramphenicol).
- Arzneistoffe
- Viele medikamentös wirksame Stoffe erfahren eine deutliche Wirkungssteigerung durch das Einführen eines Halogen-Atoms. Dies gilt insbesondere für Steroide wie Betamethason, Beclometason oder Chlormadinon. Zu bedenken ist hier, dass die Einführung eines Halogens auch die Toxizität des Stoffes beeinflussen kann.
- Feuerlöschmittel
- Die in Feuerlöschern und automatischen Löschanlagen verwendeten Halogenkohlenwasserstoffe nennt man Halone. Da sie im hohen Maß die Ozonschicht angreifen, ist die Produktion von Halonen weltweit seit dem 1. Januar 1994 verboten. Für die Entwicklungsländer gilt eine längere Ausstiegsfrist. Für teilhalogenierte Fluor-Brom-Kohlenwasserstoffe (HFBKW) war das Ausstiegsdatum der 1. Januar 1996. Seit dem Jahr 2000 dürfen in Europa Halone nur in solchen Anwendungsbereichen verwendet werden, die im Anhang VII der Verordnung (EG) Nr. 2037/2000 [4] [5] als kritische Verwendungszwecke aufgelistet und damit zugelassen sind, wie z.B. in der Zivilluftfahrt als gewichtsparendes Löschmittel, welches in Frachtern bzw. Frachträumen eingesetzt, und in Handfeuerlöschern mitgeführt wird. In der militärischen Luftfahrt wird es weiterhin als Löschmittel für Triebwerksschächte und Triebwerke eingesetzt und ist z.B. im Feuerlöschsystem (Fire Extinguisher System) der F/A-18 anzutreffen. Beispiele:
- Halon 1211 (Verwendung in Handfeuerlöschern, Bromchlordifluormethan, CF2ClBr)
- Halon 1301 (Verwendung in automatischen Löschanlagen, Bromtrifluormethan, CBrF3)
- Kältemittel
- Halogenkohlenwasserstoffe eignen sich auf Grund ihrer Eigenschaften hervorragend als Kältemittel.
- Lösungsmittel
- Halogenierte Kohlenwasserstoffe sind weitgehend unpolare Stoffe und daher gute Fettlösungsmittel. Hohe Dosen bzw. ständige Belastungen können zu Gesundheitsschäden führen.
- Pestizide
- Halogenkohlenwasserstoffe werden auch im Pflanzenschutz eingesetzt. Vor allem Chlorkohlenwasserstoffe (z.B. DDT) finden bzw. fanden ihre Verwendung im Bereich der Insektizide.
- Schmelzebehandlungsmittel
- Halogenkohlenwasserstoffe wurden als Ersatz für die risikobehaftete Anwendung von Chlorgas zwischen 1930 und 1990 zur Entfernung von Wasserstoff und flotierenden Oxyden bei der Schmelzebehandlung von Aluminium und seinen Legierungen in erheblichen Mengen eingesetzt. Danach wurde die Verwendung eingeschränkt bzw. wegen vermuteter Nähe zu Abbauprodukten ähnlich dem Seveso-Dioxin verboten.
- Treibgaskomponente in Sprühdosen
- die wichtigsten Treibmittel sind Trichlorfluormethan CCl3F und Dichlordifluormethan CCl2F2; beide Substanzen gelten als physiologisch unbedenklich. Es wurde allerdings herausgefunden, dass sie zum Abbau der Ozonschicht beitragen, da in der Stratosphäre Chlorradikale freigesetzt werden, die das Ozon in einer Reihe von Reaktionen zersetzen.
Markennamen und ihre Notation
Freon® ist der Markenname von DuPont, Frigen® der von Hoechst und Solkane® der von Solvay verwendete Name.
Analog zur Halon-Notation gilt die folgende Bezeichnungsweise für Freon®, Frigen® und Solkane®:
- R DKHF
- [D] steht für die Anzahl der Doppelbindungen
- [K] steht für die Anzahl der Kohlenstoff-Atome, um eins erniedrigt
- [H] steht für die Anzahl der Wasserstoff-Atome, um eins erhöht
- [F] steht für die Anzahl der Fluor-Atome
- [R] stammt vom englischen Wort für Kühlmittel (Refrigerant)
Wird der Stoff nicht als Kältemittel sondern z. B. als Treibmittel verwendet, wurde das R oft durch den Markennamen ersetzt.
Um von der Marken-Bezeichnung auf die Formel zu schließen, kann man folgendermaßen vorgehen: Man muss zu der Marken-Nummer die Zahl 90 hinzuzählen. In der daraus sich ergebenden Summe steht die erste Zahl für die Zahl der C-Atome, die zweite Zahl für die Zahl der H-Atome, die dritte Zahl für die Zahl der F-Atome. Die restlichen Bindungsplätze sind mit Cl-Atomen abgesättigt.
Beispiele:
- R22: 22 + 90 = 112 -> 1 C-Atom, 1 H-Atom, 2 F-Atome, 1 Cl-Atom -> CHClF2
- R134a (wichtig, weil in neueren Klimaanlagen enthalten, da chlorfrei): 134 + 90 = 224 -> 2 C-Atome, 2 H-Atome, 4 F-Atome -> C2H2F4; „a“ heißt in diesem Zusammenhang, dass 3 Fluor an einem C gebunden sind.
- R14 (Chlor- und Wasserstofffrei): 14 + 90 = 104 -> 1 C-Atome, 4 F-Atome -> CF4
Hat eine der Zahlen den Wert Null, wird sie bei vorgestellten Werten weggelassen. Die restlichen Bindungsplätze an den Kohlenstoffatomen sind durch Chloratome besetzt.
Beispielsweise für R11, CCl3F:
- Es ist keine Doppelbindung vorhanden, also ist D=0.
- Ferner ist die Anzahl der Kohlenstoffatome um eins erniedrigt (=K) auch 0.
- H=1, da kein Wasserstoffatom=0 um eins erhöht 1 ergibt.
- F=1 ist die Anzahl der Fluoratome im Molekül.
Also lautet die Bezeichnung: R11.
Sie haben üblicherweise ein (K=0) oder zwei (K=1) Kohlenstoffatome. Falls K größer ist als 1, liegt kein Reinstoff, sondern eine Mischung von Stoffen vor. Die Zusammensetzung einer solchen Mischung geht nicht direkt aus der Ziffernfolge hervor. Beispielsweise ist R502 eine Mischung aus R22 und R115 zu etwa gleichen Teilen.
Freon®, Frigen® oder Solkane® mit anderen Halogenen: Wenn der Stoff noch ein anderes Halogen als Fluor und Chlor enthält, wird seine Abkürzung, ein Buchstabe, und die Zahl der Atome angefügt wie z. B. bei R13B1.
- R13B1: 13 + 90 = 103 + 1 Bromatom -> 1 C-Atom, 0 H-Atom, 3 F-Atome, 1 Br-Atom -> CBrF3
Halon-Notation
Als Halone werden Methan- oder Ethan- Derivate bezeichnet die neben Fluor oder Chlor auch Brom enthalten[6][7]. Halon(e) ist kein Markenname sondern eine Abkürzung für Halogenkohlenwasserstoff(e).
Analog zur Freon®-, Frigen®- und Solkane®-Notation gilt die folgende Bezeichnungsweise für Halone:
- R KFCB
- [R] stammt vom englischen Wort für Kühlmittel (Refrigerant).
- [K] steht für die Anzahl der Kohlenstoff-Atome
- [F] steht für die Anzahl der Fluor-Atome
- [C] steht für die Anzahl der Chlor-Atome
- [B] steht für die Anzahl der Brom-Atome
Wenn das Halon nicht als Kühlmittel verwendet wird, wird das „R“ im Namen oft durch das Wort „Halon“ ersetzt.
Beispiele:
- R 1111 = CHFClBr
- R 13 = BrCF3 (Bromtrifluormethan, Freon FE 13B1)
Einzelnachweise
- ↑ BUND: http://www.bund.net/lab/reddot2/pdf/hormone.pdf Hormonaktive Substanzen im Wasser, September 2001, BestellNr. 45 078 (Link funktioniert nicht mehr)
- ↑ Proceedings of the National Academy of Sciences 104: 8897-8901 (2007)
- ↑ Andreas Hornung: Halogenasen aus Actinomyceten, (Diss. 2005)
- ↑ Basisrechtsakt auf www.eur-lex.europa.eu: [1]; als Pdf: [2]
- ↑ Konsolidierte Fassung (Pdf, Stand 31.07.2007): [3]
- ↑ http://www.umweltbundesamt.de/produkte/fckw/halone.htm#halone
- ↑ http://www.stmugv.bayern.de/umwelt/luftreinhaltung/ozon/stratosphaere.htm
Wikimedia Foundation.
