- Phenylethan
-
Strukturformel 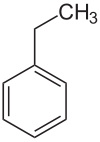
Allgemeines Name Ethylbenzol Andere Namen - Ethylbenzen
- Phenylethan
Summenformel C8H10 CAS-Nummer 100-41-4 PubChem 7500 Kurzbeschreibung farblose Flüssigkeit [1] Eigenschaften Molare Masse 106,17 g·mol−1 Aggregatzustand flüssig
Dichte 0,87 g·cm−3 [1]
Schmelzpunkt −95 °C [1]
Siedepunkt 136 °C [1]
Dampfdruck Löslichkeit - schwer löslich in Wasser: 140 mg·l−1 (20 °C) [1]
- löslich in organischen Lösungsmitteln
Sicherheitshinweise Gefahrstoffkennzeichnung aus RL 67/548/EWG, Anh. I [2] 

Leicht-
entzündlichGesundheits-
schädlich(F) (Xn) R- und S-Sätze R: 11-20 S: (2)-16-24/25-29 MAK 100 ml·m−3, 440 mg·m−3 [1]
Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Ethylbenzol (Ethylbenzen, Phenylethan) ist eine farblose, benzolähnlich riechende Flüssigkeit. Es ist ein aromatischer Kohlenwasserstoff mit der Summenformel C8H10.
Inhaltsverzeichnis
Eigenschaften
Ethylbenzol riecht benzolartig. In Wasser ist die farblose Flüssigkeit unlöslich, in organischen Lösungsmitteln jedoch löslich. Der Siedepunkt bei Normaldruck liegt bei 136 °C. Bei dieser Temperatur beträgt die Verdampfungswärme 35,57 kJ/mol[3] Die Dampfdruckfunktion ergibt sich nach Antoine entsprechend log10(P) = A−(B/(T+C)) (P in bar, T in K) mit A = 4,07488, B = 1419,315 und C = −60,539 im Temperaturbereich von 329,74 bis 410,27 K.[4] Oberhalb des Normaldrucksiedepunkts gelten die Parameter A = 4,40536, B = 1695,026 und C = −23,698 im Temperaturbereich von 420 bis 600 K.[5]
Sicherheitstechnische Kenngrößen
Ethylbenzol gilt als entzündliche Flüssigkeit. Oberhalb der Flammpunktes können sich entzündliche Dampf-Luft-Gemische bilden. Die Verbindung hat einen Flammpunkt bei 23 °C.[6] Der Explosionsbereich liegt zwischen 1 Vol% (43 g/m3) als untere Explosionsgrenze (UEG) und 7,8 Vol% (340 g/m3) als obere Explosionsgrenze (OEG).[6] Die Zündtemperatur beträgt 430 °C.[6] Der Stoff fällt somit in die Temperaturklasse T2.
Herstellung
Ethylbenzol wird in der Industrie an einem Katalysator durch Alkylierung von Benzol mit Ethen hergestellt, hierbei gibt es die Flüssigphasen-Alkylierung und die Gasphasen-Alkylierung. Sehr wenig Ethylbenzol wird über Feinfraktionierung aus C8-Aromatenfraktion isoliert. Dieses Verfahren wird auch Superfraktion genannt, ist jedoch gegenüber der Alkylierung nicht konkurrenzfähig.
Verwendung
Ethylbenzol wird Benzin zur Erhöhung der Oktanzahl (Klopffestigkeit) beigemengt. Es ist Lösungsmittel für Farben und findet sich in Kunststoffen. Es ist wichtiger Ausgangsstoff für die Synthese des Styrols. Neben dem Benzol und dem Toluol gehört Ethylbenzol zu den technisch wichtigen Aromaten, den so genannten BTEX-Aromaten.
Gefahren
Ethylbenzol ist entzündlich und gesundheitsschädlich. Es ist schwach wassergefährdend (WGK 1[1]). Mit Anteilen von 1 bis 7,8 Prozent in der Luft bildet es explosive Gemische.
Metabolismus
Im Körper wird die Ethylkette des Moleküls angegriffen. Ethylbenzol wird zu Mandelsäure und Benzoesäure oxidiert. Weitere Zwischenprodukte im Metabolismus des Ethylbenzols sind Phenylessigsäure und Methylphenylcarbinol, das Endprodukt ist Mandelsäure, es wird schließlich über den Harn ausgeschieden.
Quellen
- ↑ a b c d e f g h Eintrag zu Ethylbenzol in der GESTIS-Stoffdatenbank des BGIA, abgerufen am 13. März 2008 (JavaScript erforderlich)
- ↑ Eintrag zu CAS-Nr. 100-41-4 im European chemical Substances Information System ESIS
- ↑ Majer, V.; Svoboda, V., Enthalpies of Vaporization of Organic Compounds: A Critical Review and Data Compilation, Blackwell Scientific Publications, Oxford, 1985, 300.
- ↑ Williamham, C.B.; Taylor, W.J.; Pignocco, J.M.; Rossini, F.D., Vapor Pressures and Boiling Points of Some Paraffin, Alkylcyclopentane, Alkylcyclohexane, and Alkylbenzene Hydrocarbons, J. Res. Natl. Bur. Stand. (U.S.), 1945, 35, 219–244.
- ↑ Ambrose, D.; Broderick, B.E.; Townsend, R., The Vapour Pressures Above the Normal Boiling Point and the Critical Pressures of Some Aromatic Hydrocarbons, J. Chem. Soc. A:, 1967, 633–641.
- ↑ a b c E. Brandes, W. Möller: Sicherheitstechnische Kenngrößen – Band 1: Brennbare Flüssigkeiten und Gase, Wirtschaftsverlag NW – Verlag für neue Wissenschaft GmbH, Bremerhaven 2003
Literatur
- Ethylbenzol, S. Hirzel Verlag GmbH & Co, ISBN 3-7776-0722-3
- Jochen Ackermann: Reaktionstechnische Untersuchungen zur Synthese von Ethylbenzol aus 1,3-Butadien unter Verwendung basischer Feststoffkatalysatoren. Shaker Verlag GmbH (2001), ISBN 3-8265-9254-9
- Albrecht Xahil Tribukait: Untersuchung zum Einfluß des Drehimpulses auf die Dissoziationsgeschwindigkeit von Toluol und Ethylbenzol. Cuvillier (1999), ISBN 3-89712536-6
Wikimedia Foundation.
