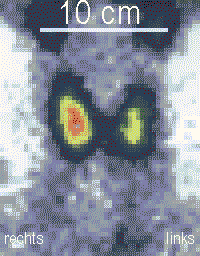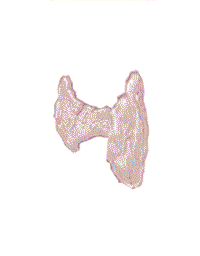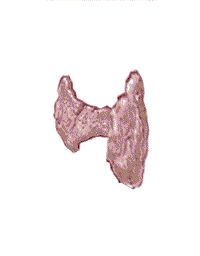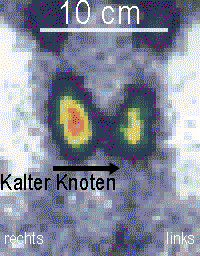- Schilddrüsenkarzinom
-
Klassifikation nach ICD-10 C73 Bösartige Neubildung der Schilddrüse ICD-10 online (WHO-Version 2006) Als Schilddrüsenkrebs (Schilddrüsenkarzinom, lat. Struma maligna) wird eine bösartige Neubildung der Schilddrüse bezeichnet. Der Schilddrüsenkrebs wird in verschiedene Typen unterteilt, von denen der häufigste Typ oft im jungen Erwachsenenalter auftritt. Störende Schilddrüsenknoten sind meistens das erste Symptom. Zur Untersuchung wird neben Ultraschall auch die Szintigraphie angewandt. Die Behandlung besteht aus Operation und der Radiojodtherapie.
Inhaltsverzeichnis
Häufigkeit
Bei Schilddrüsenkrebs handelt es sich um den häufigsten Tumor der endokrinen Organe. In Deutschland erkranken pro Jahr über 5000 Personen[1], in den USA wird die jährliche Neuerkrankungsrate (Inzidenz) mit 34000 angegeben.[2] Frauen erkranken insgesamt häufiger an Schilddrüsenkrebs als Männer. In den USA sind 74% der Schilddrüsenkarzinome bei Frauen diagnostiziert wurden.[2] Der Altersgipfel liegt insgesamt bei Frauen um 54 Jahre, bei Männern um 57 Jahre.[1] Allerdings variiert der Altersgipfel in Abhängigkeit vom Krebstyp:
- anaplastischer Typ: ca. 60. Lebensjahr
- follikulärer Typ: ca. 50. Lebensjahr
- papillärer Typ: ca. 25. Lebensjahr
- medullärer Typ: ca. 40-50. Lebensjahr
Ursachen
Die Ursachen sind im Einzelnen nicht vollständig geklärt. Es besteht ein ursächlicher Zusammenhang mit Jodmangel (etwa 2,3fach erhöhtes Risiko). Auch Strahlung (v.a. im Kindes- und Jugendlichenalter) spielt - wie bei vielen Krebserkrankungen - eine wesentliche Rolle: nach den Atombombenabwürfen auf Hiroshima und Nagasaki stieg in den betroffenen Gebieten das Risiko für ein Schilddrüsenkarzinom um ein Vielfaches an. Ähnliches gilt für die Gebiete, die nach der Katastrophe von Tschernobyl von einem massiven radioaktiven Niederschlag (Fallout) betroffen waren.
In Deutschland halten die Behörden große Mengen von Tabletten mit Kaliumiodid bereit, die im Falle eines Reaktorunfalles an Personen unter 45 Jahre ausgeteilt werden sollen, um eine Iodblockade der Schilddrüse zu erreichen.
Symptome
Typischerweise wird eine Knotenbildung im Bereich der Schilddrüse bemerkt. Dabei kann die Schilddrüse insgesamt vergrößert sein (Struma) oder normalgroß bleiben. Vergrößerte Halslymphknoten können auch schon vor einem tastbaren Schilddrüsenknoten auftreten. Heiserkeit als Ausdruck einer Stimmbandnervenlähmung sowie verwachsene Lymphknoten sind Spätsymptome bei weit fortgeschrittenem Krebs.
Untersuchungen
- Hauptartikel: Untersuchung der Schilddrüse
- Beim Abtasten der Schilddrüse sind derbe und nicht-schluckverschiebliche Knoten sowie eine begleitende Schwellung von Hals-Lymphknoten verdächtig auf eine bösartige Veränderung.
- Im Ultraschall erscheinen Schilddrüsenkarzinome meist echoarm, selten echoreich. Auch Entzündungen oder Verkalkungen können echoarm sein, Zysten sind in der Regel echofrei.
- In der Schilddrüsenszintigraphie sind kalte Knoten in 3% der Fälle ein Karzinom (einzelner kalter Knoten: 15%), sonst Entzündungen, Fibrosen, Verkalkungen, Zysten, Blutungen oder Adenome.
- Bei kalten Knoten ist unter Umständen eine Feinnadelpunktion mit Punktionszytologie indiziert (Beurteilung der entnommenen Zellen unter dem Mikroskop).
- Blutuntersuchungen:
- Die Schilddrüsenhormonwerte (TSH, fT3, fT4) geben keine Informationen über ein eventuell vorhandenes Schilddrüsenkarzinom.
- Der Tumormarker Calcitonin weist auch vor einer eventuellen Schilddrüsenoperation auf ein medulläres Schilddrüsenkarzinom oder eine C-Zellhyperplasie hin.
- Der Tumormarker Thyreoglobulin dient nur zur Verlaufsbeurteilung nach Operation bei den nicht-medullären Schilddrüsenkarzinomen.
- Eine Kehlkopfspiegelung (Laryngoskopie) erfolgt üblicherweise vor und nach einer Schilddrüsen-OP zur Frage einer möglichen Schädigung der Stimmband-Nerven (Nervus recurrens).
- Der Ausschluss der Diagnose Schilddrüsen-Karzinom ist mit letzter Sicherheit nur durch eine operative Entfernung der verdächtigen Anteile der Schilddrüse mit anschließender Beurteilung des Zellgewebes (Histologie) möglich.
Typen des Schilddrüsenkrebs
Abhängig vom Ausgangsgewebe unterscheidet man folgende Typen:
Differenzierte Karzinome
- Papilläres Schilddrüsenkarzinom (PTC) 40 %
Der Hauptmetastasierungsweg des papillären Karzinoms geht über die Lymphbahnen, wobei besonders regionäre Halslymphknoten betroffen sind. Pathohistologisch können hier eosinophile Kalziumansammlungen (Psammomkörper) nachgewiesen werden.
- Follikuläres Schilddrüsenkarzinom (FTC) 30 %
Das follikuläre Karzinom metastasiert in der Regel zuerst über das Blut. Für follikuläre Karzinome der Schilddrüse ist eine immunhistochemisch nachweisbare Expression von Thyreoglobulin typisch.
Undifferenzierte Karzinome
- Anaplastisches Karzinom 15-25 %; da bei diesem Tumortyp die undifferenzierten Karzinomzellen nicht mehr am Iodstoffwechsel teilnehmen ist im Gegensatz zur Behandlung der differenzierten Karzinome eine Radiojodtherapie nicht zielführend.
Medulläres Karzinom
- Mit 5-10 % selten ist das medulläre Karzinom (MTC), auch C-Zell-Karzinom genannt.
Erstmals 1959 als eigene Entität neben den differenzierten und undifferenzierten Schilddrüsenkarzinomen beschrieben, tritt das medulläre Karzinom familiär (ca. 15%) oder sporadisch (ca. 85% der medullären Schilddrüsenkarzinome; Altersgipfel zw. 50.-60. Lebensjahr) auf. Bei dem familiären Typ unterscheidet man das familiäre Auftreten allein des medullären Schilddrüsenkarzinoms (FMTC) vom Syndrom der multiplen endokrinen Neoplasie Typ 2A und 2B. Das MTC beruht auf bösartigen Neubildungen der parafollikulären, Calcitonin-produzierenden Zellen (sog. C-Zellen), die aufgrund entwicklungsgeschichtlicher Zusammenhänge in der Schilddrüse liegen, aber in keinem Zusammenhang mit der eigentlichen Schilddrüsenfunktion (Thyreozyten) stehen. Der sensitivste Tumormarker des medullären Karzinomes ist somit das Calcitonin. In der Tumornachsorge dienen erhöhte Werte als Indikator für ein Rezidiv. Bei der Therapie des C-Zell-Karzinoms gilt es zu beachten, dass eine nuklearmedizinische Radiojodtherapie nicht angezeigt ist, da die C-Zellen nicht am Jodstoffwechsel teilnehmen.
- Seltener finden sich beim Schilddrüsenkrebs die Typen Plattenepithelkarzinom, Sarkome, Hämangiosarkome oder Metastasen anderer Tumoren.
Behandlung
Operative Schilddrüsenentfernung
Grundsätzlich muss bei Schilddrüsenkrebs die Schilddrüse vollständig entfernt werden (Thyreoidektomie).
Ausnahme ist das sogenannte Mikrokarzinom. Als Mikrokarzinom wird das papilläre Schilddrüsenkarzinom mit der Stadieneinteilung pT1a N0 M0 bezeichnet. pT1a bezeichnet hierbei einen einzelnen Tumor (""a"") mit einem in der Pathologie gemessenen Tumordurchmesser von <1 cm, N0 den fehlenden Nachweis eines Tumorbefalls der lokalen Lymphknoten und M0 das Fehlen von Fernmetastasen. Zusätzlich sollte der Tumor nicht im Randbereich des Schilddrüsengewebes gefunden werden und die Kapsel der Schilddrüse nicht überschreiten. In diesem Fall wird das Therapievorgehen der geringen Risikoeinschätzung angepasst: Es wird ausschließlich der befallene Schilddrüsenlappen operativ entfernt und von einer anschließenden Radiojodtherapie (Ablation) abgesehen.
Operative Lymphknotenentfernung
Neben der Schilddrüsenentfernung werden meist auch die Lymphknoten des Schilddrüsengebietes entfernt (sog. Lymphadenektomie, auch Neck-Dissection genannt), da die Lymphknoten vom Krebs befallen werden können.
Radiojodtherapie
Nach der Schilddrüsenoperation wird zumeist eine Radiojodtherapie zur Entfernung des postoperativ verbliebenen Schilddrüsengewebes durchgeführt (Ablation). Dabei wird radioaktives Jod-131 verabreicht, das sich ausschließlich im Schilddrüsengewebe anreichert. Aufgrund der physikalischen Eigenschaften des Jod-131 (überwiegender β-Strahler) werden benachbarte Strukturen nur gering von der Strahlung betroffen. Bestimmte andere Organe (Speicheldrüsen, Schweißdrüsen, Magenschleimhaut, Nieren, Blase) sind lediglich an der Ausscheidung des Jod beteiligt und erhalten ebenfalls eine geringe Strahlendosis.
Eine wirksame Ablation kann nur durchgeführt werden, wenn zuvor TSH ausreichend stimuliert wurde. Dies wurde in der Vergangenheit meist durch einen Schilddrüsenhormonentzug erreicht, indem nach der Operation die fehlenden Hormone zunächst nicht ersetzt wurden. Anstelle dieses geschilderten Schilddrüsenhormonentzugs, der zu einer deutlichen Hypothyreose mit z. T. erheblichen körperlichen und psychischen Belastungen für die Patienten führt, kann seit 2005 in Europa auch der TSH-Wert mit der Gabe von gentechnisch-hergestelltem TSH (rhTSH, rekombinantes humanes TSH) auf die gewünschte Höhe für die Ablation (Radiojodtherapie) gebracht werden. Ab 2007 gibt es in Deutschland spezielle DRGs (Diagnosis Related Groups) für den Einsatz des sehr teuren rhTSH, so dass auch Patienten der gesetzlichen Krankenkassen zunehmend mit rhTSH für die Radiojodtherapie vorbehandelt werden. Das rhTSH wird dabei an zwei aufeinander folgenden Tagen intramuskulär (i. m.) injiziert. In den folgenden Tagen steigt der TSH-Wert für eine kurze Zeit an und fällt schnell wieder ab. Für eine optimale Aufnahme des radioaktiven Jods ist es von entscheidender Bedeutung, dass der TSH-Wert möglichst hoch ist. Daher ist bei der Gabe von rhTSH ein exaktes Zeitmanagement unerlässlich. Bestimmte Konstellationen, wie die Einnahme von gerinnungshemmenden Substanzen (z. B. Marcumar) als Kontraindikation für eine i. m.-Gabe oder eine fehlende Sicherheit, ob und wann die Ablation durchgeführt werden soll, können gegen die Anwendung des rhTSH und für eine Therapie in Hypothyreose sprechen.
Anschließende Hormontherapie
Im Anschluss an die Operation und Radiojodtherapie wird begonnen, die Schilddrüsenfunktion durch künstliche Schilddrüsenhormone zu ersetzen. Hierfür wird in der Regel L-Thyroxin (freies T4) gegeben. Zur Erstdosierung mit L-Thyroxin gilt die Faustregel, dass ein Mensch 2 Mikrogramm L-Thyroxin pro Kilogramm Körpergewicht benötigt, wenn keine Schilddrüse mehr vorhanden ist. Zur Kontrolle der richtigen Dosierung wird der TSH-Wert verwendet. Zu diesem Zeitpunkt der Behandlung liegt der Zielwert des TSH bei 0,05 - 0,1 mU/l (die früher propagierte Suppression des TSH wird aufgrund der Belastung des Herz-Kreislauf-Systems als Risikofaktor für Herzinfarkt und Schlaganfall heute nicht mehr empfohlen). Zur Minderung von Schilddrüsenüberfunktions-Symptomen kann auch L-Carnitin eingesetzt werden. Es gibt allerdings noch keine Erfahrungen mit einer Langzeiteinnahme von L-Carnitin.
Kontrolluntersuchungen
Nach 3 Monaten sollte das Ergebnis der Radiojodtherapie mit einer sog. Radiojoddiagnostik dokumentiert werden. Im Hormonentzug (4 Wochen vor der Untersuchung keine Einnahme des L-Thyroxins) wird eine geringe Menge 131jod verabreicht und die Verteilung im Körper nach 48 Stunden mit einer Szintigraphie ermittelt. Auch für diese Radiojoddiagnostik ist - hier bereits seit 2001 - ein Hormonentzug nicht mehr notwendig (s. o.). Bei dem Einsatz von rhTSH zur Vorbereitung einer Radiojoddiagnostik muss allerdings bedacht werden, dass für eine evtl. notwendige erneute Radiojodtherapie auch das rhTSH erneut verabreicht werden muss. Als weiterer Parameter wird der TG-Wert (Thyreoglobulin) im Blut bestimmt als Maß für die Anzahl von Schilddrüsenzellen im Organismus. Sind noch Schilddrüsenreste im Halsbereich oder jodspeichernde Metastasen (Streuherde) vorhanden, wird eine weitere Radiojodtherapie angeschlossen. In diesem Fall wird eine erneute Radiojoddiagnostik nach 3 Monaten durchgeführt. Sind beide Untersuchungsergebnisse negativ (niedriges bis nicht mehr nachweisbares TG und keine auffällige jodspeicherung im Körper) gilt die Radiojoddiagnostik als unauffällig. Dann wird eine weitere Radiojoddiagnostik zur Bestätigung der Ergebnisse in weiteren 9 Monaten vorgenommen. Danach sollten regelmäßige Kontrollen des Tumormarkers Thyreoglobulin lebenslang einmal pro Jahr durchgeführt werden. Je nach Risikoeinschätzung des individuellen Tumors (low oder high risk) gelten lebenslang unterschiedliche Zielbereiche für den TSH-Wert bei der Dosierung der Schilddrüsenhormone:
- Low-Risk Karzinome: TSH 0,1 - 0,2 mU/l
- High-Risk Karzinome: TSH 0,05 - 0,1 mU/l
Für die Kontrolle und Nachsorge gibt es inzwischen neuere Leitlinien, in denen die Ultraschall-Untersuchung des Halses und die Bestimmung des Tumormarkers Thyreoglobulin unter Stimulation (rhTSH) eine größere Bedeutung haben, während die Radiojoddiagnostik eine wesentlich geringere Rolle spielt als in dem oben geschilderten Vorgehen.
Prognose
Differenzierte Karzinome
Die Heilungschancen bei differenzierten Schilddrüsenkarzinomen sind im Allgemeinen sehr gut. Meist werden durchschnittliche 10-Jahres-Überlebensraten von über 90 % bei der papillären und ca. 80 % bei der follikulären Variante angegeben (bei Behandlung).[3][4]Als Prognosefaktoren gelten Patientenalter sowie Größe, Ausbreitung und histologische Differenzierung des Tumors; Lymphknotenmetastasen scheinen die Prognose nicht wesentlich zu beeinflussen. Wegen des erhöhten Rezidivrisikos ist eine konsequente Nachsorge äußerst wichtig.
Medulläres und anaplastisches Karzinom
Folgende 5-Jahres-Überlebensraten gelten durchschnittlich (bei Behandlung):
- Medulläres Karzinom: 60-70 %
- Anaplastisches Karzinom: unter 10 %
Ähnliche Erkrankungen
Folgende Erkrankungen können ähnliche Symptome wie der Schilddrüsenkrebs verursachen:
- Zyste
- Struma nodosa (kalter Knoten / heißer Knoten)
- Adenom
- Metastasen (bspw. von einem Mammakarzinom)
Selbsthilfe
Auf Grund der Seltenheit von Schilddrüsenkrebs ist es für Patienten überaus schwer, Betroffene für den Erfahrungsaustausch zu finden, es gibt daher nur wenige lokale Selbsthilfegruppen. Auf Bundesebene gibt es zwei Selbsthilfe-Organisationen, die sich für die Interessen von Schilddrüsenkrebspatienten einsetzen, praktische Informationen geben (richtige Einnahme von Schilddrüsenhormonen, jodarme Ernährung vor Radiojodtherapie) und über neueste Studien und Leitlinien kritisch informieren.
Weiterführende Informationen und Belege
Literatur
- ETA-Leitlinie - European consensus for the management of patients with differentiated thyroid carcinoma of the follicular epithelium. (pdf, online)
- Ch. Reiners: Die Folgen von Tschernobyl - Schilddrüsenkrebs nach der Reaktorkatastrophe Tschernobyl. in: Der Internist. Berlin 39.1998,6(Jun), 592-593. PMID 9677515 ISSN 0020-9554
Weblinks
Einzelnachweise
- ↑ a b C. Reiners u.a.: Struma maligna - Schilddrüsenkarzinome. Deutsche Medizinische Wochenschrift 2008; 133, Nr. 43, S. 2215-2228.
- ↑ a b R Michael Tuttle et al.: Overview of the management of differentiated thyroid cancer. UpToDate 2008, Version 16.2
- ↑ Österreichische Gesellschaft für Chirurgische Onkologie: Prognose des differenzierten (papillären, follikulären) Schilddrüsenkarzinoms
- ↑ Medizinische Universität Wien: Prognose des differenzierten (papillären, follikulären) Schilddrüsenkarzinoms
Bitte beachte den Hinweis zu Gesundheitsthemen!
Wikimedia Foundation.