- Tetrahydrofolat
-
Strukturformel 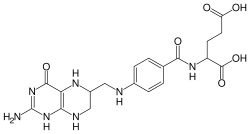
Allgemeines Name Tetrahydrofolsäure Andere Namen - H4Folat
- FH4
- Coenzym F
- N-[(6S)-5,6,7,8-Tetrahydropteroyl]- L-glutaminsäure
- 2-((4-((2-Amino-4-oxo- 5,6,7,8-tetrahydro-1H-pteridin- 6-yl)methylamino)benzoyl) amino)pentandisäure
Summenformel C19H23N7O6 CAS-Nummer 29347-89-5 PubChem 1129 Eigenschaften Molare Masse 445,43 g/mol Aggregatzustand fest
Sicherheitshinweise Gefahrstoffkennzeichnung 
unbekannt R- und S-Sätze R: ? S: ? Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Tetrahydrofolsäure (H4Folat, FH4), auch Coenzym F, ist ein biochemisches Derivat der Folsäure (= Vitamin B9) und, gebunden an Polyglutamat, fungiert im Stoffwechsel aller Lebewesen als wichtiger Methylgruppendonator.
Inhaltsverzeichnis
Biologische Bedeutung
Tetrahydrofolsäure und ihre Derivate sind von besonderer Bedeutung im Aminosäure- und Purin-Stoffwechsel sowie bei der Homoacetatgärung. Sie wird zur Entgiftung von Ameisensäure, die aus Methanol gebildet wird, benötigt.
Biosynthese und Transport
Biosynthetisch entsteht FH4 aus FH2, das selbst aus Folsäure entsteht. Katalysiert werden beide Reaktionen vom Enzym Dihydrofolatreduktase. Stoffe, die dieses Enzym in seiner Funktion hemmen, wie z. B. Methotrexat (Antimetabolit), wirken als Zellgifte.
Wirkungsort von FH4 ist im Zytosol und in den Mitochondrien von Zellen. Um FH4 zunächst vom Blutplasma ins Zytosol zu verschaffen, produziert die Zelle das Transportprotein Folattransporter 1, der die Ein- und Ausschleusung katalysiert. Um ins Innere des Mitochondriums zu gelangen, gibt es gleichermaßen den mitochondrialen Folattransporter.[1]
Reaktionen als Substrat
FH2, FH4 und seine Derivate werden durch Bindung an Polyglutamat an der Ausschleusung gehindert und so im Zytosol und den Mitochondrien der Zellen gespeichert. Nur in dieser Form können viele der kohlenstoffübertragenden Reaktionen stattfinden. Für die Bindung von FH2 und FH4 an Polyglutamat wird das Enzym Folylpolyglutamat-Synthetase benötigt.
Aus FH4-Polyglutamat werden mehrere abgeleitete Stoffe erzeugt, die als Kohlenstoff-Überträger in wichtigen Stoffwechselwegen fungieren. Meist bleibt nach der Reaktion FH4-Polyglutamat übrig, das wiederverwendet wird.
- 10-Formyl-FH4-Polyglutamat ist Reaktionspartner bei der Biosynthese von IMP und Methionin. Es wird aus FH4-Polyglutamat mithilfe des multifunktionellen Enzyms C1-THF-Synthase hergestellt.
- Formyl-FH4-PG wird mithilfe desselben Enzyms in zwei Schritten zu 5,10-Methylen-FH4-Polyglutamat umgesetzt. Dieses nimmt an der Biosynthese von TMP und an der gegenseitigen Umwandlung von Glycin zu Serin teil.
- Letztgenannter Stoff wiederum wird mit der Methylentetrahydrofolat-Reduktase oder mit Ferredoxin zu 5-Methyl-FH4-Polyglutamat umgewandelt, welches Homocystein zu Methionin methyliert und eine Rolle als Methyl-Überträger bei der bakteriellen Methanbildung spielt.[1][2]
Einzelnachweise
Weblinks
Wikimedia Foundation.
