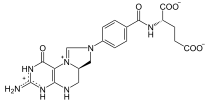
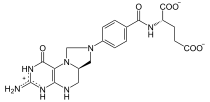
- C1-THF-Synthase
-
C1-THF-Synthase —
Masse/Länge Primärstruktur 934 Aminosäuren Bezeichner Gen-Name MTHFD1 Externe IDs OMIM: 601634 UniProt: P11586 Enzymklassifikationen EC, Kategorie 1.5.1.5 Oxidoreduktase Reaktionsart (De-)Hydrierung Substrat 5,10-Methylen-THF(-PG) + NADP+ Produkte 5,10-Methenyl-THF(-PG) + NADPH EC, Kategorie 3.5.4.9 Hydrolase Reaktionsart Hydrolyse Substrat 5,10-Methenyl-THF(-PG) + H2O Produkte 10-Formyl-THF(-PG) EC, Kategorie 6.3.4.3 Ligase Reaktionsart Addition eines Formylrests Substrat Tetrahydrofolat(-PG) + Formiat + ATP Produkte 10-Formyl-THF(-PG) + ADP + Phosphat Vorkommen Übergeordnetes Taxon Eukaryoten C1-THF-Synthase (genauer Zytoplasmatische C-1–Tetrahydrofolat-Synthase) heißt das Enzym in Eukaryoten, das drei verschiedene Reaktionen im Folsäure-Stoffwechsel katalysiert. Bakterienenzyme mit den gleichen Funktionen kommen nur als einzelne Proteine vor. Beim Menschen ist das Enzym in allen Gewebetypen zu finden, und es existiert ein paraloges mitochondriales Enzym, das allerdings nur Ligaseaktivität zeigt. Mutationen im MTHFD1-Gen können durch Verringerung einer oder mehrerer der drei Enzymfunktionen zu erhöhtem Risiko für Neuralrohrdefekten beim Neugeborenen führen, das durch Zufuhr von Folsäure während der ersten Schwangerschaftswochen gesenkt werden kann.[1][2][3]
Das Risiko für Abruptio placentae ist bei Müttern, die homozygot für eine bestimmte Mutation des MTHFD1-Gens sind, mehrfach erhöht. Nach einer Studie an 600 Chinesen erhöhen bestimmte Varianten der C1-THF-Synthase die Homocystein-Werte und das Risiko für Magenkrebs. Auch für das pathologische Geschehen bei Migräne mit Aura werden einzelne Varianten des Enzyms verantwortlich gemacht.[4][5][6]
Katalyierte Reaktionen
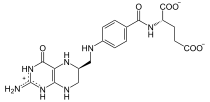 + ATP + HCOO-
+ ATP + HCOO- 
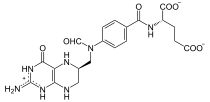 + ADP + Phosphat
+ ADP + PhosphatAn Tetrahydrofolsäure (THF) wird eine Formylgruppe addiert, um 10-Formyl-THF zu erhalten.
10-Formyl-THF wird zu 5,10-Methenyl-THF umgesetzt.
5,10-Methenyl-THF wird zu 5,10-Methylen-THF hydriert.
Einzelnachweise
- ↑ UniProt P11586
- ↑ PROSITE-Eintrag
- ↑ Walkup AS, Appling DR: Enzymatic characterization of human mitochondrial C1-tetrahydrofolate synthase. In: Arch. Biochem. Biophys.. 442, Nr. 2, Oktober 2005, S. 196–205. doi:10.1016/j.abb.2005.08.007. PMID 16171773.
- ↑ Parle-McDermott A, Mills JL, Kirke PN, et al: MTHFD1 R653Q polymorphism is a maternal genetic risk factor for severe abruptio placentae. In: Am. J. Med. Genet. A. 132, Nr. 4, Februar 2005, S. 365–8. doi:10.1002/ajmg.a.30354. PMID 15633187.
- ↑ Wang L, Ke Q, Chen W, et al: Polymorphisms of MTHFD, plasma homocysteine levels, and risk of gastric cancer in a high-risk Chinese population. In: Clin. Cancer Res.. 13, Nr. 8, April 2007, S. 2526–32. doi:10.1158/1078-0432.CCR-06-2293. PMID 17438114.
- ↑ Oterino A, Valle N, Pascual J, et al: Thymidylate synthase promoter tandem repeat and MTHFD1 R653Q polymorphisms modulate the risk for migraine conferred by the MTHFR T677 allele. In: Brain Res. Mol. Brain Res.. 139, Nr. 1, September 2005, S. 163–8. doi:10.1016/j.molbrainres.2005.05.015. PMID 15953655.
Weblinks
- reactome.org: MTHFD1 dimer [cytosol]
Wikimedia Foundation.