- DHFR
-
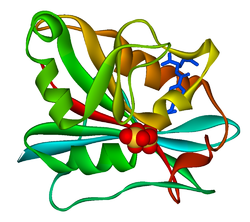
Dihydrofolat-Reduktase Vorhandene Strukturdaten: s. UniProt Größe 186 Aminosäuren Bezeichner Gen-Name DHFR Externe IDs OMIM: 126060 UniProt: P00374 Enzymklassifikation EC, Kategorie 1.5.1.3 Oxidoreduktase Reaktionsart Reduktion Substrat 7,8-Dihydrofolat + NADPH + H+ Produkte 5,6,7,8-Tetrahydrofolat + NADP+ Vorkommen Homologie-Familie DHFR Übergeordnetes Taxon Lebewesen Dihydrofolatreduktase (DHFR), auch Dihydrofolsäure-Reduktase, heißen Enzyme, die Folsäure zu Dihydrofolsäure (DHF) und DHF und Tetrahydrofolsäure (THF) hydrieren. Diese Reaktionen aktivieren das Vitamin Folsäure und sind unentbehrlich für die Nukleotid-Biosynthese in allen Lebewesen. Beim Menschen kommt DHFR in allen Gewebetypen vor. Mutationen am DHFR-Gen können DHFR-Mangel und dieser megaloblastäre Anämie verursachen.[1]
Die DHFR in Protozoen und manchen Pflanzen ist ein Doppelenzym, das zusätzlich die Funktion der Thymidylatsynthase hat; aufgrund dieser strukturellen Eigenheit ist die protozoische DHFR Target bei der Entwicklung von Antibiotika, z. B. gegen den Malariaerreger Plasmodium falciparum oder Kryptosporidien.[2][3][4]
Inhaltsverzeichnis
Katalysierte Reaktionen
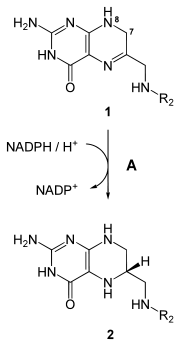
7,8-Dihydrofolsäure wird mit NADPH als Elektronendonor zu Tetrahydrofolsäure reduziert (s. Abb.). Außerdem kann Folsäure zu DHF reduziert werden; diese Reaktion läuft jedoch langsamer ab.[5]
Weitere Funktionen
Die Anwesenheit von DHFR in Endothelzellen ist ausschlaggebend für die Funktion von Tetrahydrobiopterin in der NO-Synthase.[6]
Regulation und Hemmung
DHFR ist ein ausgiebig untersuchtes Enzym, das als Target für die Chemotherapie und bei anderen Krankheiten gilt. Das Enzym kann durch Folsäure-Antagonisten wie Methotrexat, Aminopterin oder Trimethoprim kompetitiv gehemmt werden. Die Hemmung bewirkt einen Mangel an Tetrahydrofolsäure, wodurch die Thymin-Synthese (Thymidylat-Synthase benötigt THF) sowie die Purinsynthese (Aufbau des Puringrundkörpers) verhindert wird, worauf die Zelle abstirbt.[7]
Siehe auch
Einzelnachweise
- ↑ UniProt P00374
- ↑ Prosite-Eintrag
- ↑ Ochong E, Bell DJ, Johnson DJ, et al: Plasmodium falciparum strains harboring dihydrofolate reductase with the I164L mutation are absent in Malawi and Zambia even under antifolate drug pressure. In: Antimicrob. Agents Chemother.. 52, Nr. 11, November 2008, S. 3883–8. doi:10.1128/AAC.00431-08. PMID 18725445
- ↑ Bolstad DB, Bolstad ES, Frey KM, Wright DL, Anderson AC: Structure-based approach to the development of potent and selective inhibitors of dihydrofolate reductase from cryptosporidium. In: J. Med. Chem.. 51, Nr. 21, November 2008, S. 6839–52. doi:10.1021/jm8009124. PMID 18834108
- ↑ EC 1.5.1.3
- ↑ Chalupsky K, Cai H: Endothelial dihydrofolate reductase: critical for nitric oxide bioavailability and role in angiotensin II uncoupling of endothelial nitric oxide synthase. In: Proc. Natl. Acad. Sci. U.S.A.. 102, Nr. 25, June 2005, S. 9056–61. doi:10.1073/pnas.0409594102. PMID 15941833
- ↑ Abali EE, Skacel NE, Celikkaya H, Hsieh YC: Regulation of human dihydrofolate reductase activity and expression. In: Vitam. Horm.. 79, 2008, S. 267–92. doi:10.1016/S0083-6729(08)00409-3. PMID 18804698
Weblinks
Wikimedia Foundation.