- NaK (Legierung)
-
NaK ist die Bezeichnung für eine Legierung, die aus Natrium und Kalium besteht und ein Eutektikum bildet, d.h. die Gemische aus beiden Komponenten haben einen niedrigeren Schmelzpunkt als die der reinen Stoffe. Sie ist in einem weiten Konzentrationsbereich bei Raumtemperatur flüssig und ist gelegentlich zur Kühlung von Kernreaktoren verwendet worden.
Inhaltsverzeichnis
Eigenschaften
Physikalische Eigenschaften
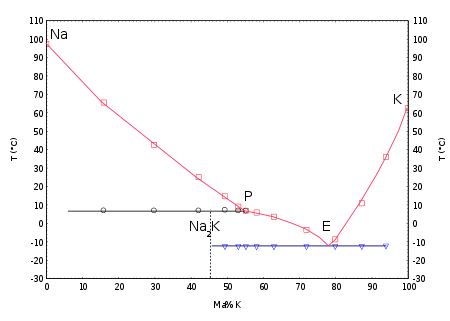 Fest-flüssig-Phasendiagramm von Natrium und Kalium[1]
Fest-flüssig-Phasendiagramm von Natrium und Kalium[1]
NaK-Mischungen mit einem Kaliumgehalt zwischen 40 % und 90 % sind bei Raumtemperatur flüssig. Das Eutektikum liegt bei einer Konzentration von 22 % Natrium und 78 % Kalium, hat einen Schmelzpunkt von -11 °C und einen Siedepunkt von 785 °C.[2] Bei einer Dichte von 0,866 g/cm³ (21 °C) ist die Legierung leichter als Wasser. Die Grenzflächenspannung ist sehr hoch, so dass die Flüssigkeit die Neigung hat, große Tropfen zu bilden.
Chemische Eigenschaften
NaK reagiert wie seine Bestandteile Natrium und Kalium sehr leicht mit Wasser und Sauerstoff. Bei Lagerung unter Luft bildet sich ein Belag aus gelbem Kaliumhyperoxid der leicht entzündlich ist. Da es aus Alkalimetallen besteht, wirkt es stark reduzierend.
Herstellung
Industriell wird NaK durch Destillation hergestellt.[3] Hierbei werden flüssiges Natrium und Kaliumchlorid einer Destillationskolonne kontinuierlich zugeführt. In der Reaktionszone reagiert das Kaliumchlorid mit dem Natrium, so dass Natriumchlorid und Kalium entstehen. Im darüberliegenden Verstärkungsteil der Kolonne wird das leichtersiedende Kalium angereichert und über Kopf als Gemisch mit Natrium in beliebiger Konzentration abgezogen.
Verwendung
Kühlmittel in Kernkraftwerken
NaK wird häufig in Versuchsreaktoren zur Kernspaltung mit schnellen Neutronen verwendet. Der niedrige Schmelzpunkt der Legierung erlaubt ein einfacheres Abschalten, verglichen mit kommerziellen Reaktoren, da beim Einsatz anderer flüssiger Kühlmittel mit höheren Schmelzpunkten, wie etwa Natrium oder Blei, der Einsatz einer externen Beheizung erforderlich wäre.
Katalyse
NaK kann als Katalysator in verschiedenen Reaktionen eingesetzt werden, wie z.B. bei der Herstellung von Ibuprofen.
Trocknungsmittel
Aufgrund der hohen Reaktivität mit Wasser und des flüssigen Zustandes kann es auch als Entwässerungsmittel eingesetzt werden, um Restfeuchte aus Lösungsmitteln, z. B. Tetrahydrofuran, abzutrennen.
Einzelnachweise
- ↑ G.L.C.M. van Rossen, H. van Bleiswijk: Über das Zustandsdiagramm der Kalium-Natriumlegierungen, in: Z. Anorg. Chem., 1912, 74, S. 152–156.
- ↑ MSDS Callery Chemical Company, 3. Januar 2000
- ↑ The Manufacture of Potassium and NaK, Jackson, C.B.; Werner, R.C.; January 1, 1957 (Englisch)
Wikimedia Foundation.
