- De-Mayo-Reaktion
-
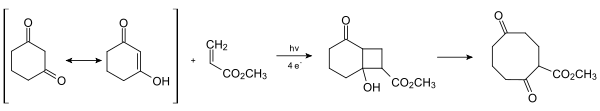
Bei der De-Mayo-Reaktion handelt es sich um eine Dominoreaktion, bei welcher zunächst eine [2+2]-Cycloaddition eines Olefins an eine enolisierbare β-Diketoverbindung als vorgelagertes Gleichgewicht erfolgt. Das Hauptprodukt dieser konzertierten disrotatorischen Photoaddition ist bei elektronenarmen Olefinen das Kopf-Schwanz-Produkt. Diesem Reaktionsschritt folgt eine Retro-Aldol-Reaktion, die zur Öffnung des Cyclobutanringes führt. Über ein Keto-Enol-Gleichgewicht bildet sich alsdann mechanistisch eine 1,5-Diketoverbindung.
Die Reaktion wurde nach Paul Jose de Mayo (1924–1994) benannt.[1]
Inhaltsverzeichnis
Reaktionssequenz
Literatur
- P. de Mayo, H. Takeshita und A. B. M. Sattar: The Photochemical Synthesis of 1,5-Diketones and their Cyclisation. A New Annulation. In: Proceedings of the Chemical Society. 1962, S. 119 doi:10.1039/PS9620000097
- P. de Mayo, Acc. Chem. Res. (Review), 1971, 4, S. 49 doi:10.1021/ar50038a001
- J. J. Li: Name Reactions. A Collection of Detailed Reaction Mechanism. Springer, 2003, S. 105. ISBN 3-540-40203-9
Weblinks
Einzelnachweise
- ↑ zu Paul Jose de Mayo siehe: James F. King und Karl Overton: Paul Jose de Mayo. 8 August 1924-26 July 1994. In: Biographical Memoirs of Fellows of the Royal Society. Band 45, 1999, S. 113–128. doi:10.1098/rsbm.1999.0009
Wikimedia Foundation.