- Fünffachbindung
-
Eine Fünffachbindung ist eine Form der chemischen Bindung zwischen zwei Atomen, die über Elektronenpaare vermittelt wird (Elektronenpaarbindung). Zwischen den Atomen gewährleisten fünf Paare von Bindungselektronen den Zusammenhalt des darauf aufbauenden Moleküls.
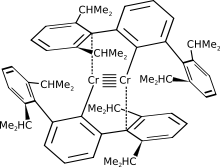
Die erst im November 2005 entdeckte Fünffachbindung besteht aus einer Metall-Metall-Bindung der Verbindung Ar-Cr2-Ar (dunkelrote Kristalle, thermisch stabil bis 200 °C) mit einem Aryl-Rest (Ar = Terphenyl-Ligand C6H3-2,6-(C6H3-2,6-iPr2)2).
Die Bindung setzt sich aus folgenden einzelnen Bindungen zusammen:
- einer σ-Bindung (dz²)
- zwei π-Bindungen (jeweils entartet, eine Knotenebene, dxz, dyz)
- zwei δ-Bindungen (jeweils entartet, zwei Knotenebenen, dxy und dx²-y²)
Damit unterscheidet sich die Fünffachbindung nur durch eine zusätzliche (entartete) δ-Bindung von der Vierfachbindung.
Weblinks
- Informationen über die Fünffachbindung (PDF, 717 kB)
Siehe auch
MehrfachbindungenDoppelbindung | Dreifachbindung | Vierfachbindung | Fünffachbindung
Wikimedia Foundation.
Schlagen Sie auch in anderen Wörterbüchern nach:
Doppelbindungen — Eine Doppelbindung ist eine Form der chemischen Bindung, bei der zwei Atome über zwei verschiedene Atombindungen verknüpft werden. Meist besteht eine Doppelbindung aus einer σ und einer π Bindung. Entstehung einer normalen Doppelbindung … Deutsch Wikipedia
Isolierte Doppelbindung — Eine Doppelbindung ist eine Form der chemischen Bindung, bei der zwei Atome über zwei verschiedene Atombindungen verknüpft werden. Meist besteht eine Doppelbindung aus einer σ und einer π Bindung. Entstehung einer normalen Doppelbindung … Deutsch Wikipedia
Konjugat — Unter Konjugation versteht man in der Chemie die Überlappung von π Orbitalen (π=PI), einer π Bindung mit einem p Orbital eines sp2 hybridisierten (Kohlenstoff )Atoms oder mit weiteren π Orbitalen. Im ersteren Falle (konjugierte Radikale,… … Deutsch Wikipedia
Konjugierte Doppelbindung — Unter Konjugation versteht man in der Chemie die Überlappung von π Orbitalen (π=PI), einer π Bindung mit einem p Orbital eines sp2 hybridisierten (Kohlenstoff )Atoms oder mit weiteren π Orbitalen. Im ersteren Falle (konjugierte Radikale,… … Deutsch Wikipedia
Konjugierte Doppelbindungen — Unter Konjugation versteht man in der Chemie die Überlappung von π Orbitalen (π=PI), einer π Bindung mit einem p Orbital eines sp2 hybridisierten (Kohlenstoff )Atoms oder mit weiteren π Orbitalen. Im ersteren Falle (konjugierte Radikale,… … Deutsch Wikipedia
Zweifachbindung — Eine Doppelbindung ist eine Form der chemischen Bindung, bei der zwei Atome über zwei verschiedene Atombindungen verknüpft werden. Meist besteht eine Doppelbindung aus einer σ und einer π Bindung. Entstehung einer normalen Doppelbindung … Deutsch Wikipedia
Atombindung — Die Atombindung (auch kovalente Bindung, Elektronenpaarbindung oder homöopolare Bindung) ist eine Form der chemischen Bindungen und ist als solche für den festen Zusammenhalt von Atomen in molekular aufgebauten chemischen Verbindungen… … Deutsch Wikipedia
Bindungsarten — Die chemische Bindung ist ein physikalisches Phänomen, durch das zwei oder mehrere Atome oder Ionen fest zu chemischen Verbindungen aneinander gebunden sind. Dieses beruht darauf, dass es für die meisten Atome oder Ionen energetisch günstiger ist … Deutsch Wikipedia
Doppelbindung — Eine Doppelbindung ist eine Form der chemischen Bindung, bei der zwei Atome über zwei verschiedene Atombindungen verknüpft werden.[1] Meist besteht eine Doppelbindung aus einer σ und einer π Bindung. Entstehung einer normalen Doppelbindung … Deutsch Wikipedia
Doppelbindungsregel — Die empirisch aufgestellte Doppelbindungsregel besagt, dass es den Elementen der 3. Periode des Periodensystems nicht mehr möglich sein sollte, stabile chemische Verbindungen mit (p p)π Mehrfachbindungen auszubilden. Inhaltsverzeichnis 1… … Deutsch Wikipedia