- Komplexometrische Titration
-
Die Komplexometrie auch Chelatometrie (v. gr. chele „Krebsschere“) wurde 1945 von Gerold Schwarzenbach entwickelt.[1][2] Sie beruht auf der Bildung von sogenannten Chelatkomplexen (Umschlingungskomplexe mit mehrzähnigen Liganden). Sie eignet sich zur quantitativen Bestimmung von Metallionen in wässrigen Lösungen mit Hilfe von so genannten Komplexbildnern.
Zu der zu titrierenden Lösung wird ein Indikator gegeben, der im an das Metallion gebundenen Zustand eine andere Farbe zeigt, als im freien Zustand. Da der Indikator nur schwach an das Metallion gebunden ist, wird er bei der Zugabe des Chelatliganden freigesetzt, wodurch sich die Farbe der Lösung ändert. Häufig wird in einer Pufferlösung gearbeitet, um den pH-Wert konstant zu halten.
Chelatebildner sind organische mehrarmige Moleküle, die das Metallion umschließen; in diesem Zusammenhang wird von mehrzähnigen Liganden gesprochen. Im Handel befinden sich eine Reihe von Chelatebildner unter den Namen Komplexon, Idranal oder Titriplex, gefolgt von einer römischen Ziffer.
Chelatbildner für die Komplexometrie Komplexon Trivialname Abkürzung Strukturformel I Nitrilotriessigsäure NTA 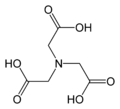
II Ethylendiamintetraessigsäure EDTA 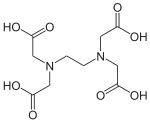
III Ethylendiamintetraessigsäure-
DinatriumsalzEDTA-Na2 IV Cyclohexandiamintetraessigsäure CDTA -CDTA_svg.png)
V Diethylentriaminpentaessigsäure DTPA 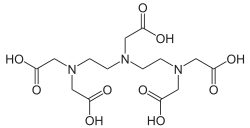
VI Ethylenglykol-bis(aminoethylether)-
N,N,N′N′-TetraessigsäureEGTA 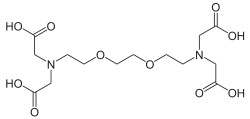
VII N-(2-Hydroxyethyl)-ethylendiamin-
N,N,N′-triessigsäure-TrinatriumsalzHEDTA 
VIII Triethylentetraminhexaessigsäure TTHA 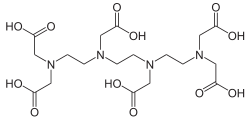
Quellen
- ↑ Schwarzenbach, G. & Flaschka, H. (1965): Die Komplexometrische Titration. Ferdinand Enke Verlag, Stuttgart.
- ↑ G. Schwarzenbach, E. Kampitsch und R. Steiner (1945): Komplexone I. Über die Salzbildung der Nitrilotriessigsäure. In: Helvetica Chimica Acta. Bd. 28, Nr. 1, S. 828–840. doi:10.1002/hlca.194502801121
Siehe auch
Weblinks
Wikimedia Foundation.
