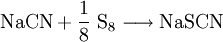- NaSCN
-
Strukturformel Allgemeines Name Natriumthiocyanat Andere Namen - Natriumrhodanid
- Natriumsulfocyanid
Summenformel CNNaS CAS-Nummer 540-72-7 Kurzbeschreibung farbloser Feststoff [1] Eigenschaften Molare Masse 81,07 g·mol−1 Aggregatzustand fest
Dichte 1,73 g·cm–3 [1]
Schmelzpunkt 287 °C [1]
Siedepunkt Zersetzung: >368 °C [2]
Dampfdruck Löslichkeit löslich in Wasser: 1250 g·l−1 (20 °C) [2]
Sicherheitshinweise Gefahrstoffkennzeichnung aus RL 67/548/EWG, Anh. I [3] 
Gesundheits-
schädlich(Xn) R- und S-Sätze R: 20/21/22-32-52/53 S: (2)-13-61 LD50 764 mg·kg−1 [2]
WGK 1 – schwach wassergefährdend [1] Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Natriumthiocyanat ist eine gesundheitsschädliche chemische Verbindung mit der Formel NaSCN, die bei Raumtemperatur als weißer, hygroskopischer Feststoff vorliegt.[4] Es wird in vielen Synthesen verwendet, die das Thiocyanation (Rhodanid) SCN− benötigen.
Inhaltsverzeichnis
Darstellung, Eigenschaften und Verwendung
Die Darstellung von Natriumthiocyanat wird mit Natriumcyanid und elementarem Schwefel durchgeführt:
Kristalle von NaSCN sind orthorhombisch, wobei jedes Na+ von drei Schwefel- und drei Stickstoffliganden umgeben ist.[5] Verwendung findet NaSCN bei der Umwandlung von Halogenalkanen in entsprechende Alkylthiocyanate, wobei auch Kaliumthiocyanat und seltener Ammoniumthiocyanat eingesetzt werden können. Diese Verbindungen werden auch als Pseudohalogenide bezeichnet, da sie viele Analogien zu den echten Halogeniden aufweisen. Beispiele für derartige Synthesen sind die Herstellung von Isopropylthiocyanat (Siedepunkt 146–151 °C) aus Isopropylbromid mit NaSCN in heißem Ethanol.[6] Durch starke Säuren wird aus NaSCN Isothiocyansäure (S=C=NH, pKa = −1,28) freigesetzt.[7] Zur Herstellung von Thioharnstoff wird aus NaSCN das instabile HSCN in situ erzeugt, welches dann mit organischen Aminen Thioharnstoffverbindungen bildet.[8] Wie die beiden anderen erwähnten Thiocyanate (von K+ und NH4+) wird NaSCN in der Phototechnik (Sensibilisierung), Galvanotechnik (Glanzbildner für Kupferbäder), Metallurgie (Extraktion von Zirconium, Hafnium und Lanthanoiden), Textilindustrie (Färbehilfsmittel, Bedrucken), chemischen Industrie und Analytik (Produktion von Herbiziden und Fungiziden, Fe3+-Nachweis) verwendet. Natriumthiocyanat ist als mindergiftig eingestuft, d. h. gesundheitsschädlich beim Verschlucken und bei Berührung mit der Haut, allerdings entwickelt es bei Kontakt mit Säure sehr giftige Gase. Das krebserzeugende und wassergefährdende Potential von NaSCN ist als relativ gering zu bewerten.
Siehe auch
Quellen
- ↑ a b c d Eintrag zu Natriumthiocyanat in der GESTIS-Stoffdatenbank des BGIA, abgerufen am 7. Feb. 2008 (JavaScript erforderlich)
- ↑ a b c d Sicherheitsdatenblatt (Merck)
- ↑ Eintrag zu CAS-Nr. 540-72-7 im European chemical Substances Information System ESIS
- ↑ [1] Chemische Daten von Merck
- ↑ van Rooyen, P. H., Boeyens, J. C. A. (1975) "Sodium thiocyanate" Acta Crystallographica, B31, 2933-2934.
- ↑ Shriner, R. L. (1943) "Isopropyl Thiocyanate" Organic Syntheses, 2, 366 . http://www.orgsyn.org/orgsyn/pdfs/CV2P0366.pdf
- ↑ Chiang, Y., Kresge, A. J. (2000) “Determination of the Acidity Constant of Isothiocyanic Acid in Aqueous Solution” Canadian Journal of Chemistry, 78, 1627-1628.
- ↑ Allen, C. F. H., VanAllan, J. (1955) "2-Amino-6-Methylbenzothiazole" Organic Syntheses, 3, 76. http://www.orgsyn.org/orgsyn/pdfs/CV3P0076.pdf
Literatur
- Holleman, Wiberg: Lehrbuch der Anorganischen Chemie. 101. Auflage. Berlin, New York: De Gruyter 1995. ISBN 3-11-01-2641-9
Wikimedia Foundation.