- Boroxin
-
Strukturformel 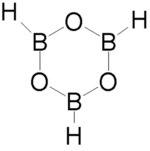
Allgemeines Name Boroxin Andere Namen - Cyclotriboroxan
- 1,3,5,2,4,6-trioxatriborinane
Summenformel B3H3O3 CAS-Nummer 289-56-5 Eigenschaften Molare Masse 83,45 g·mol−1 Sicherheitshinweise EU-Gefahrstoffkennzeichnung [1] keine Einstufung verfügbar R- und S-Sätze R: siehe oben S: siehe oben Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Boroxin ist eine heterocyclische Verbindung des Bors mit Sauerstoff, die auch Cyclotriboroxan (B3H3O3) genannt wird. Es ist sehr reaktionsfreudig und reagiert schon bei Raumtemperatur spontan mit Sauerstoff und Kohlenmonoxid[2].
Verwendung
Boroxin dient zur Herstellung von Verbindungen, die für Elektrolyte von Lithium-Polymer-Akkumulatoren[3] und für optische Materialien[4] benutzt werden.
Derivate
Abgeleitete Verbindungen mit der für Boroxin typischen Ringstruktur (B3O3-R3) werden auch Boroxine[5] genannt. Sie entstehen häufig bei Reaktionen von Borsäuren.[6]
- Trihydroxyboroxin (H3B3O6, CAS: 13460-51-0)
- Trimethoxyboroxin (C3H9B3O6, CAS: 102-24-9)
- Trimethylboroxin (C3H9B3O3, CAS: 823-96-1)
- Triarylboroxine[7]
- Tri(4-bromophenyl)boroxin
- 3-Chlorpropoxyboroxin
- 2-Chlorethoxyboroxin
- 2,4,6-Trivinylcyclotriboroxan pyridin (CAS: 95010-27-6)
Die Synthese von Boroxinderivaten erfolgt durch die Kondensation von Borsäuren. Die meisten Boroxine liegen in Anwesenheit von Wasser in einem Gleichgewicht mit ihren entsprechenden Borsäuren vor.
Einzelnachweise
- ↑ In Bezug auf ihre Gefährlichkeit wurde die Substanz von der EU noch nicht eingestuft, eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ G. H. Lee II, R. F. Porter: Gaseous Boroxine: Mechanisms of Reactions with Oxygen and Carbon Monoxide. In: Inorganic Chemistry. 5, 1966, S. 1329–1333, doi:10.1021/ic50042a007.
- ↑ http://cheme.eng.shizuoka.ac.jp/~f-klab/f-journal.htm
- ↑ Q. G. Wu, G. Wu, L. Brancaleon, S. Wang: B3O3Ph3(7-azaindole): Structure, Luminescence, and Fluxionality. In: Organometallics. 18, 1999, S. 2553-2556, doi:10.1021/om990053t (online).
- ↑ http://www.freepatentsonline.com/6335423.html
- ↑ http://www.alfa.com/media/pdf/brochures/Boronic%20Acid%20Brochure.pdf
- ↑ G.Alcaraz, L. Euzenat,O. Mongin,C. Katan, I. Ledoux, J. Zyss, M. Blanchard-Desce, M. Vaultier: Improved transparency–nonlinearity trade-off with boroxine-based octupolar molecules. In: Chemical Communications. 2003, S. 2766–2767, doi:10.1039/b308664j (online).
Wikimedia Foundation.
