- Tetraazidomethan
-
Strukturformel 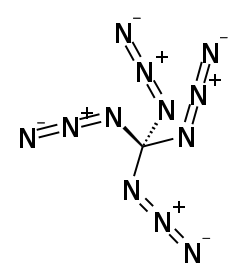
Allgemeines Name Tetraazidomethan Andere Namen - Kohlenstofftetraazid
Summenformel CN12 CAS-Nummer 869384-16-7 PubChem 16059578 Kurzbeschreibung farblose Flüssigkeit
Eigenschaften Molare Masse 180,09 g·mol−1 Sicherheitshinweise EU-Gefahrstoffkennzeichnung [1] keine Einstufung verfügbar R- und S-Sätze R: siehe oben S: siehe oben Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Tetraazidomethan ist eine thermisch instabile Kohlenstoff-Stickstoff-Verbindung mit einem Stickstoffgehalt von 93,3 %. Formal ist es das Tetraazidoderivat des Methans. Die hochenergetische, zu einer spontanen explosiven Zersetzung neigende Substanz wurde erstmals 2006 von einer Gruppe an der TU Chemnitz hergestellt.[2]
Inhaltsverzeichnis
Darstellung und Gewinnung
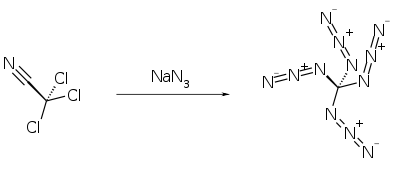
Die Synthese von Tetraazidomethan gelingt durch die Umsetzung von Trichloracetonitril mit Natriumazid in Acetonitril.[2]
Eine zweite Herstellungsvariante geht von Triazidocarboniumhexachloroantimonat [C(N3)3]SbCl6 aus, welches bei einer Umsetzung mit Natriumazid die Zielverbindung ergibt.[2]
Eigenschaften
Reines Tetraazidomethan ist eine farblose Flüssigkeit, die extrem gefährlich zu spontanen Explosionen neigt. Neben der thermischen Instabilität ist die Verbindung extrem empfindlich gegenüber mechanischer Belastung.[2]
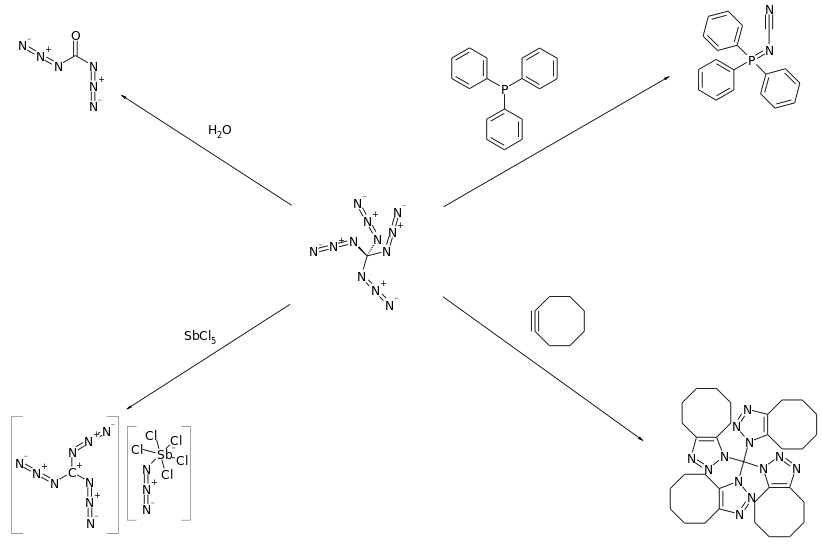
In Lösung eröffnet die Verbindung einige interessante Synthesereaktionen, wie die Hydrolyse zu Kohlensäurediazid, Cycloadditionsreaktionen mit Alkenen und Alkinen sowie Reaktionen mit Phosphinen. Starke Lewis-Säure wie Antimonpentachlorid spalten ein Azidanion unter Bildung des entsprechenden Triazidocarboniumsalzes [C(N3)3][SbCl5N3] ab.[2]
Verwendung
Eine praktische Verwendung von freiem Tetraazidomethan ist wegen der hohen Instabilität ausgeschlossen. In Formulierungen wird ein Potential für energetische Mischungen gesehen.[3]
Einzelnachweise
- ↑ In Bezug auf ihre Gefährlichkeit wurde die Substanz von der EU noch nicht eingestuft, eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ a b c d e K. Banert, Y.-H. Joo, T. Rüffer, B. Walfort, H. Lang: Die aufregende Chemie des Tetraazidomethans in Angew. Chem. 119 (2007) 1187–1190, doi:10.1002/ange.200603960
- ↑ "Tetraazidomethane: Chemistry with a Bang", Chemical & Engineering News, Dec. 18, 2006, 46.
Wikimedia Foundation.