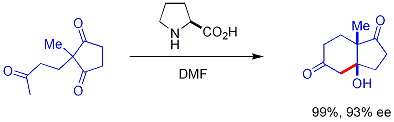
- Hajos-Parrish-Eder-Sauer-Wiechert Reaktion
-
Die Hajos-Parrish-Eder-Sauer-Wiechert-Reaktion ist eine Reaktion in der organischen Chemie. Es handelt sich hierbei um eine Prolin-katalysierte asymetrische Aldol-Reaktion. Die Reaktion wurde benannt nach den Entdeckern bei den Unternehmen Hoffmann-La Roche[1] [2] und der Schering AG.[3]
Inhaltsverzeichnis
Geschichte
Das ursprüngliche Verfahren wurde von Zoltan G. Hajos und David R. Parrish in den 1970er Jahren entdeckt und liefert das optisch aktive Aldolprodukt - das bicyclische Ketol. Die Eder-Sauer-Wiechert-Modifikation erweitert die Reaktion um einen Kondensationsschritt und man erhält das optisch aktive Endion auf dem Weg dieser asymmetrischen organokatalytischen Reaktion. Die Reaktion und die so erhaltenen chiralen Verbindungen wurden schnell häufig in der Steroid-Synthese genutzt um den C- und D-Ring des Steran-Gerüstes aufzubauen.
In der ursprünglichen Arbeit wird natürlich vorkommendes Prolin als chiraler Katalysator für eine Aldolreaktion benutzt. Die Ausgangsverbindung ist ein achirales Triketon und es werden nur 3 mol% S-Prolin benutzt um ein Ketol mit 93% Enantiomerenüberschuss herzustellen dabei arbeiteten sie bei moderaten Temperaturen und DMF als Lösungsmittel. Im Gegensatz dazu arbeitete die Schering Gruppe unter nicht-biologischen Bedingungen mit 47 mol% (S)-Prolin in einer 1N Perchlorsäure und Acetonitril als Lösungsmittel bei 80°C. Es wurde daher auch nicht das von Hajos und Parrish gefundene Produkt isoliert sondern anstatt dessen das ungesättigte Produkt der Aldolkondensation. [4]
Hajos und Parrish haben die absolute Konfiguration für das cis-verknüpfte 7a-Methyl-6,5-bicylische Ketol durch CD-Spektroskopie bestimmt und diese Ergebnisse mit Hilfe der Röntgenstrukturanalyse bestätigt.[5] Die Struktur des Ketols ist demnach die folgende:
Im Jahr 2000 hat eine Untersuchung von List et al gezeigt, dass eine Aldoladdition zwischen einem Keton und einem Aldehyd in Anwesenheit von Prolin ebenfalls zu einer asymmetrischen Induktion mit deutlichem Enantiomerenüberschuss führt. [6].
Die Autoren wiesen ausdrücklich auf die Ähnlichkeit zwischen der Prolin-katalysierten asymmetrischen Aldolreaktion und dem Enzym Aldolase A hin denn beide haben ein Enamin-Intermediat als Übergangszustand.
Reaktionsmechanismus
Es gab bislang eine Reihe von Vorschlägen über den Mechanismus der asymmetrischen Katalyse der Reaktion. Hajos schlug 1974 ein Halbaminal als entscheidendes Intermediat vor während Agami im Jahr 1984 ein Enamin als Intermediat bevorzugte. Durch experimentelle Ergebnisse schlug er ein Enamin mit zwei Prolin-Molekülen als Übergangszustand anhand der kinetischen Daten vor. [7] Entsprechend ist auch der von Houk 2001 vorgeschlagene Mechanismus des Übergangszustandes. Hier reicht ein einzelnes Prolin-Molekül aus um den Übergangszustand mit Hilfe einer Wasserstoffbrückenbindung auszubilden.[8] [9]
Der Reaktionsmechanismus wie ihn 2000 die Gruppe um List vorgestellt hat basiert auf der Bildung eines Enamins und die beobachtete Stereochemie kann mit Hilfe des Zimmermann-Traxler-Modells erklärt werden.[6]
Herkunft des Namens der Reaktion
Im Jahr 1985 wurde als erstes von C. Agami die Prolin-katalysierte asymetrische Robinson Annelierung als Hajos-Parrish Reaktion bezeichnet.[10] Auch Henri B. Kagan bezeichnete (zusammen mit Agami) diese Reaktion in einem Abstract mit diesem Namen.[11] Später im Jahr 2001 publizierte Kagan eine Arbeit und bezeichnete die Reaktion hier als Hajos-Parrish-Wiechert Reaktion. [12] Im Jahr 2002 wurde dann in eine Veröffentlichung von Benjamin List zwei Namen ergänzt und so wird die Reaktion heute praktisch einheitlich in der wissenschaftlichen Literatur als Hajos-Parrish-Eder-Sauer-Wiechert Reaktion bezeichnet.
Einzelnachweise
- ↑ Z. G. Hajos, D. R. Parrish, German Patent DE 2102623 1971.
- ↑ Zoltan G. Hajos, David R. Parrish: In Asymmetric synthesis of bicyclic intermediates of natural product chemistry J. Org. Chem. 1974, 39, 1615-1621. doi:10.1021/jo00925a003
- ↑ Ulrich Eder, Gerhard Sauer, Rudolf Wiechert: In New Type of Asymmetric Cyclization to Optically Active Steroid CD Partial Structures, Angew. Chem. Int. Ed. Engl. 1971, 10, 496-497 doi:10.1002/anie.197104961.
- ↑ Benjamin List: In Proline-catalyzed asymmetric reactions Tetrahedron 2002, 58, 5573-5590 Vorlage:Doi.
- ↑ I.L. Karle, J. Karle: In The crystal structure of digitoxigenin Acta Cryst. ,Sect.B25, '1969, 434-442.
- ↑ a b Richard A. Lerner, Carlos F. Barbas III: In Proline-Catalyzed Direct Asymmetric Aldol J. Am. Chem. Soc. 2000, 122, 2395-2396 doi:10.1021/ja994280y.
- ↑ Stereochemistry-59 : New insights into the mechanism of the proline-catalyzed asymmetric robinson cyclization; structure of two intermediates. asymmetric dehydration Tetrahedron, Volume 40, Issue 6, 1984, Pages 1031-1038 Claude Agami, Franck Meynier, Catherine Puchot, Jean Guilhem and Claudine Pascard doi:doi:10.1016/S0040-4020(01)91242-6
- ↑ Bahmanyar, S.; Houk, K. N.: In The Origin of Stereoselectivity in Proline-Catalyzed Intramolecular Aldol Reactions J. Am. Chem. Soc. 2001; 123, 12911-12912. doi:10.1021/ja011714s
- ↑ S. Bahmanyar, N.K. Houk: In Transition States of Amine-Catalyzed Aldol Reactions Involving Enamine Intermediates: Theoretical Studies of Mechanism, Reactivity, and Stereoselectivity J. Am. Chem. Soc. 2001, 123, 11273-11283 doi:10.1021/ja011403h
- ↑ C. Agami, J. Levisalles, C.J. Puchot: In J. Chem. Soc., Chem. Commun. 1985, 8, 441-442
- ↑ J. Am. Chem. Soc. 1986, 108, 2353-2357
- ↑ H.B. Kagan et al: In Nonlinear Effects in Asymmetric Catalysis: A Personal Accoun Synlett 2001, 888–899
Wikimedia Foundation.