- Hajos-Wiechert-Keton
-
Strukturformel 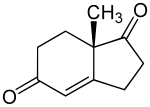
Allgemeines Name Hajos-Wiechert-Keton Andere Namen - (S)-(+)-Hajos-Parrish-Keton
- 5,6,7,8-Tetrahydro-8-methylindan-1,5-dion
- (7aS)-7a-Methyl-2,3,6,7-tetrahydroindol-1,5-dion
Summenformel C10H12O2 CAS-Nummer 17553-86-5 PubChem 736943 Eigenschaften Molare Masse 164,20 g·mol−1 Aggregatzustand fest
Schmelzpunkt 57–64 °C[1]
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung [1] 
Gefahr
H- und P-Sätze H: 301-315-317-319-335 EUH: keine EUH-Sätze P: 261-280-301+310-305+351+338 [1] EU-Gefahrstoffkennzeichnung [1] 
Gesundheits-
schädlich(Xn) R- und S-Sätze R: 22-36/37/38-43 S: 26-36/37 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Das Hajos-Wiechert-Keton, auch Hajos-Parrish-Keton, ist eine bicyclische chemische Verbindung.
Inhaltsverzeichnis
Darstellung
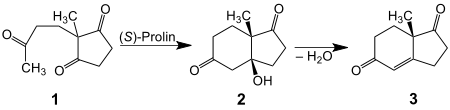
Die Verbindung kann auf organokatalytischem Wege erhalten werden. Die Aldoladdition zum (S)-(+)-Hajos-Parrish-Ketol 2 wird durch die natürliche Aminosäure (S)-(–)-Prolin katalysiert. Die Reaktion läuft bei Raumtemperatur ab.[2][3] Wird die Reaktion mit höherer Katalysatorbeladung und bei höherer Temperatur durchgeführt, so erhält man das (S)-(+)-Hajos-Wiechert-Keton 3, das durch Abspaltung von Wasser aus dem Hajos-Parrish-Ketol entsteht.[4] Wenn man die unnatürliche Aminosäure (R)-(+)-Prolin als Katalysator verwendet, erfolgt die Synthese die optische Enantiomere (R)-(–)-2 und (R)-(–)-3.[3] Das geschieht auch wenn man in der Reaktion anstatt von (S)-(+)-Prolin die β-Aminosäure (S)-Homoprolin als Katalysator anwendet [5].
Reaktionsmechanismus
Es gibt mehrere Vorschläge zum Reaktionsmechanismus der (S)-(–)-Prolin-katalysierten Bildung des (S)-(+)-Hajos-Wiechert-Ketons. Diese Vorschläge stammen u. a. von Hajos und Parrish (1974),[2] Claude Agami et al. (1984)[6] sowie Bahmanyar und Houk (2001)[7] und werden unter dem Lemma Hajos-Parrish-Eder-Sauer-Wiechert-Reaktion im Detail erläutert.
Verwendung
Das Hajos-Wiechert-Keton (Hajos-Parrish-Keton) (S)-(+)-3 ist ein Synthesebaustein zur Totalsynthese von Steroiden und anderen natürlichen Verbindungen. So gelang beispielsweise die enantioselektive Totalsynthese von (+)-Cortistatin A ausgehend vom (S)-(+)-3 Hajos-Parrish-Keton [8][9][10][11] und der ent-Deoxycholsäure[12] ausgehend vom (R)-(–)-3 Hajos-Parrish-Keton.
Einzelnachweise
- ↑ a b c d Datenblatt (S)-(+)-2,3,7,7a-Tetrahydro-7a-methyl-1H-indene-1,5(6H)-dione bei Sigma-Aldrich, abgerufen am 3. April 2011.
- ↑ a b Z. G. Hajos, D. R. Parrish: Asymmetric Synthesis of Bicyclic Intermediates of Natural Product Chemistry, J. Org. Chem. 1974, 39, 1615–1621.
- ↑ a b , Z. G. Hajos, D. R. Parrish, US Patent 3975440 1976, Priorität 9. Dezember 1970.
- ↑ U. Eder, G. Sauer, R. Wiechert, in: Angew. Chem. Int. Ed. Engl. 1971, 10, 496–497.
- ↑ Michael Limbach: β-Homoamino acids as catalysts on enantioselective intra- and intermoelcular aldol reactions, Tetrahedron Letters 47 (2006) 3843–3847.
- ↑ Claude Agami, Franck Meynier, Catherine Puchot, Jean Guilhem und Claudine Pascard: Stereochemistry-59 : New insights into the mechanism of the proline-catalyzed asymmetric robinson cyclization; structure of two intermediates. asymmetric dehydration, Tetrahedron, 40, 1984, 1031-1038 doi:10.1016/S0040-4020(01)91242-6.
- ↑ S. Bahmanyar, N. K. Houk: In Transition States of Amine-Catalyzed Aldol Reactions Involving Enamine Intermediates: Theoretical Studies of Mechanism, Reactivity, and Stereoselectivity, J. Am. Chem. Soc. 2001, 123, 11273-11283 doi:10.1021/ja011403h.
- ↑ H. M. Lee, C. Nieto-Oberhuber, M. D. Shair: Enantioselective Synthesis of (+)-Cortistatin A, a Potent and Selective Inhibitor of Endothelial Cell Proliferation, in: J. Am. Chem. Soc. 2008, 130, 16864–16866; doi:10.1021/ja8071918.
- ↑ S. Yamashita, K. Iso, M. Hirama: A Concise Synthesis of the Pentacyclic Framework of Cortistatins, in Org. Lett. 2008, 10, 3413–3415; doi: 10.1021/ol8012099.
- ↑ J. L. Frie, C. S. Jeffrey, E. J. Sorensen: A Hypervalent Iodine-Induced Double Annulation Enables a Concise Synthesis of the Pentacyclic Core Structure of the Cortistatins, in Org. Lett. 2009, 11, 5394–5397; doi:10.1021/ol902168g.
- ↑ Shuji Yamashita, Kentaro Iso, Kazuki Kitajima, Masafumi Himuro, and Masahiro Hirama: Total Synthesis of Cortistatins A and J in:J.Org.Chem. 2011, 76(8), 2408-2425 doi:10.1021/jo2002616.
- ↑ B. W. Katona, N. P. Rath, S. Anant, W. F. Stenson, D. F. Covey: Enantiomeric Deoxycholic Acid: Total Synthesis, Characterization, and Preliminary Toxicity toward Colon Cancer Cell Lines, in: J. Org. Chem. 2007, 72, 9298–9307; doi:10.1021/jo701559q.
Kategorien:- Giftiger Stoff
- Sensibilisierender Stoff
- Gesundheitsschädlicher Stoff
- Cyclopentanon
- Cyclohexenon
Wikimedia Foundation.