- Kauffmann-Olefinierung
-
Unter einer Kauffmann-Olefinierung versteht man eine von Thomas Kauffmann entwickelte Reaktion zum Überführen eines Ketons oder eines Aldehydes in eine Methylen-Gruppe. Die Reaktion ist mit der Tebbe-Reaktion, der Wittig-Reaktion oder dem Lombardo-Reagenz verwandt.
Inhaltsverzeichnis
Herstellung des Reagenzes
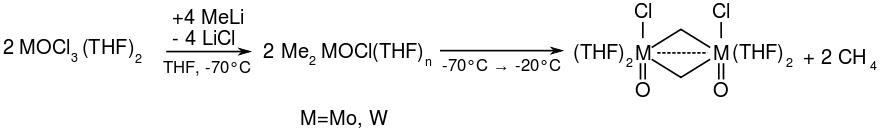
Das Reagenz für die Kauffmann-Olefinierung wird in situ aus verschiedenen Molybdän- oder Wolframchloriden durch Umsetzung mit Methyllithium bei tiefen Temperaturen (−78 °C) hergestellt.[1][2][3][4]
Das Olefinierungsreagenz entsteht beim Aufwärmen des Reaktionsgemisches. Es konnte anhand von NMR-Studien gezeigt werden, dass es sich bei der reaktiven Spezies nicht um ein Schrock-Carben (wie beispielsweise das Tebbe-Reagenz) handelt.
Mechanismus
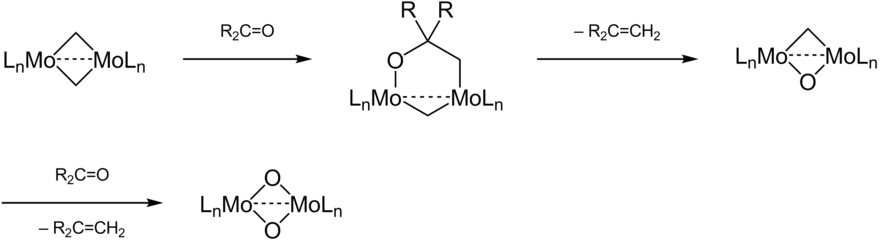
Mechanistische Untersuchungen haben gezeigt, dass es sich bei dem Olefinierungs-Prozess um eine Abfolge von Cycloadditions- und Cycloeleminierungsschritten besteht.
Einsatzgebiet
Die Kauffmann-Olefinierung hat längere Zeit praktisch keine Beachtung in der Literatur gefunden. In jüngerer Zeit hat sie jedoch eine Anwendung in der Naturstoffsynthese als sehr mildes und nicht-basisches Olefinierungsreagenz gefunden.[5] Im Rahmen dieser Arbeit wurde eine Kombination aus dem Olefinierungsschritt und einer Olefinmetathese entwickelt.[6] Dabei ist bemerkenswert, dass die anorganischen Reaktionsprodukte der Kauffmann-Olefinierung den Metathese-Katalysator nicht zersetzt.
Einzelnachweise
- ↑ T. Kauffmann, M. Papenberg, R. Wieschollek, J. Sander: "Alkylchromium and Alkylmanganese Reagents, IV. — On the Aldehyde and Cheleselective Alkylation of Organic Carbonyl Compounds with Monoalkylchromium(III) Reagents." in Chem. Ber. 1992, 125, 143–148. doi:10.1002/cber.19921250126
- ↑ T. Kauffmann, P. Fiegenbaum, M. Papenberg, R. Wieschollek, D. Wingbermühle: "Organomolybdän- und Organowolfram-;Reagenzien, III. Chemoselektive, nichtbasische Carbonylmethylenierungs-;Reagenzien aus MoOCl3(THF)2 und MoOCl4: Bildung, Thermolabilität, Struktur" in Chem. Ber. 1993, 126, 79–87.doi:10.1002/cber.19931260114
- ↑ T. Kauffmann, J. Braune, P. Fiegenbaum, U. Hansmersmann, C. Neiteler, M. Papenberg, R. Wiescholleck: In Chem. Ber. 1993, 126, 89–96.
- ↑ T. Kauffmann: In Angew. Chem. 1997, 109, 1312–1329.
- ↑ K. Oesterreich, D. Spitzner: In Tetrahedron 2002, 58, 4331–4334.
- ↑ K. Oesterreich, I. Klein, D. Spitzner: In Synlett 2002, 1712–1714.
Wikimedia Foundation.