- Tebbe-Reagenz
-
Strukturformel 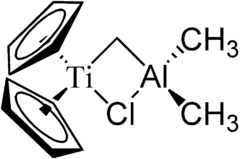
Allgemeines Name Tebbe-Reagenz Andere Namen - μ-Chlorobis(cyclopentadienyl)- (dimethylaluminium)-μ-methylentitan (IUPAC)
Summenformel C13H18AlClTi CAS-Nummer 67719-69-1 Kurzbeschreibung roter Feststoff [1]
Eigenschaften Molare Masse 284,62 g·mol−1 Aggregatzustand fest
Dichte 0,93 g·cm−3 [1]
Löslichkeit löslich in Toluol, Diethylether
Sicherheitshinweise EU-Gefahrstoffkennzeichnung [2] keine Einstufung verfügbar R- und S-Sätze R: siehe oben S: siehe oben LD50 636 mg/kg (Ratte, oral) [1]
Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Das Tebbe-Reagenz (nach Frederick Nye Tebbe, kurz Fred Tebbe) ist eine metallorganische Verbindung, die der Methylenierung von Ketonen oder Estern, der Tebbe-Methylenierung, dient.[3] Es handelt sich hierbei um einen zweikernigen verbrückten Komplex mit einem Titan- und einem Aluminium-Kern. Am Titankern, der über eine Methylengruppe und über eine Chlorbrücke mit dem Aluminiumkern verbrückt ist, sind zwei Cyclopentadienyl-Reste gebunden. Am Aluminiumkern befinden sich noch zwei Methylreste. Das Tebbe-Reagenz ist ein pyrophorer roter Feststoff und wird deshalb nur unter Schutzgas gehandhabt. Kommerziell ist es meist als Lösung (zum Beispiel: in Toluol) erhältlich.
Inhaltsverzeichnis
Herstellung
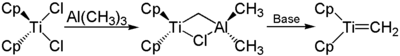
Tebbe-Reagenz wird aus Titanocendichlorid (Cp2Cl2Ti) und Trimethylaluminium durch dreitägiges Rühren bei Raumtemperatur hergestellt.[4] Das eigentlich zur Methylenierung benötigte Schrock-Carben kann hieraus in situ durch Behandlung mit milden Basen (zum Beispiel Pyridin) erhalten werden.
Reaktionsmechanismus
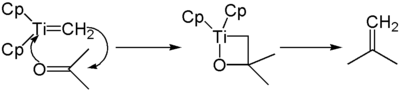
Das durch Basenzusatz erhaltene Schrock-Carben addiert zunächst an die Carbonylkomponente unter Bildung eines Oxatitanacyclobutans. Nach Ringöffnung erhält man das methylenierte Produkt.
Ähnlich wie im Falle Phosphors im Wittig-Reagenz ist die Affinität von Titan zu Sauerstoff Triebkraft der Reaktion.
Einsatzspektrum
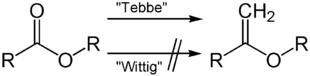
Anders als bei anderen Olefinierungen (vgl. Wittig-Reaktion, Horner-Wadsworth-Emmons-Reaktion) ist der Einsatz des Tebbe-Reagenz auf die Einführung von Methylengruppen beschränkt. Allerdings können bei Verwendung des Tebbe-Reagenz auch Ester eingesetzt werden, die sich zum Beispiel mit der Wittig-Reaktion nicht umsetzen lassen.
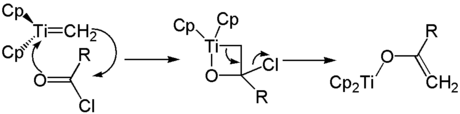
Ein weiteres Anwendungsgebiet des Tebbe-Reagenz liegt in der Synthese von Titanenolaten. Das aus einem Carbonsäurechlorid und dem Tebbe-Reagenz gewonnene Oxatitanacyclobutan-Derivat zerfällt unter Abspaltung des Chloridions zum Titanenolat.
Alternativen zum Tebbe-Reagenz sind das Petasis-Reagenz und das Lombardo-Reagenz.
Weblinks
http://www.organische-chemie.ch/OC/Namen/Tebbe.htm
Quellen
- ↑ a b c Datenblatt Tebbe-Reagenz bei Sigma-Aldrich, abgerufen am 6. Juni 2010.
- ↑ In Bezug auf ihre Gefährlichkeit wurde die Substanz von der EU noch nicht eingestuft, eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ F. N. Tebbe, G. W. Parshall, G. S. Reddy, J. Am. Chem. Soc. 1978, 100, 3611-3613.
- ↑ W.A. Herrmann, Advances in Organometallic Chemistry 1982, 20, 195-197.
Wikimedia Foundation.