- Lacosamid
-
Strukturformel 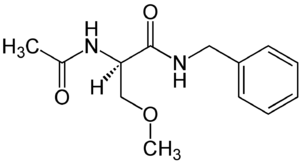
Allgemeines Freiname Lacosamid Andere Namen - IUPAC: (R)-2-(Acetylamino)-N-benzyl-3-methoxypropanamid
- Harkoserid
- Erlosamid
Summenformel C13H18N2O3 CAS-Nummer 175481-36-4 PubChem 219078 ATC-Code N03AX18
Arzneistoffangaben Wirkstoffklasse Verschreibungspflichtig: ja Eigenschaften Molare Masse 250,29 g·mol−1 Sicherheitshinweise Bitte beachten Sie die eingeschränkte Gültigkeit der Gefahrstoffkennzeichnung bei Arzneimitteln EU-Gefahrstoffkennzeichnung [1] Keine Einstufung verfügbarR- und S-Sätze R: siehe oben S: siehe oben Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Lacosamid (Handelsname: Vimpat®; Hersteller: UCB) ist ein Arzneistoff aus der Gruppe der Antikonvulsiva, der in der Behandlung von epileptischen Anfällen eingesetzt wird.
Inhaltsverzeichnis
Klinische Angaben
Anwendungsgebiete (Indikationen)
Lacosamid kann zur Zusatzbehandlung fokaler epileptischer Anfälle mit oder ohne sekundäre Generalisierung bei Patienten ab 16 Jahren angewendet werden.
Pharmakologische Eigenschaften
Wirkungsmechanismus (Pharmakodynamik)
Der Wirkmechanismus von Lacosamid ist nicht vollständig aufgeklärt. Es wird angenommen, dass die antikonvulsive Wirkung u. a. auf einer Hemmung spannungsabhängiger Natriumkanäle beruht. Weiterhin beeinflusst Lacosamid den Eiweißstoff collapsin response mediator protein-2 (CRMP-2). CRMP-2 kommt vornehmlich im Zentralnervensystem vor and ist für die Differenzierung von Nervenzellen sowie für das Aussprossen von Nervenleitungen von Bedeutung.
Sonstige Informationen
Geschichtliches
Lacosamid wurde in den 1990er Jahren durch den US-amerikanischen Chemiker Harold Kohn synthetisiert[2] und später durch Schwarz in den Anwendungsgebieten Epilepsie und Schmerz entwickelt. Das Arzneimittel ging nach der Übernahme von Schwarz an UCB über.
Die Erstzulassung als Antikonvulsivum erfolgte 2008 in der EU. Die US-amerikanische Gesundheitsbehörde FDA hatte zuvor einen Zulassungsantrag für die Schmerzbehandlung bei diabetischer Polyneuropathie abgelehnt. Einen entsprechenden Zulassungsantrag für die EU zog UCB im September 2008 zurück.
Einzelnachweise
- ↑ In Bezug auf ihre Gefährlichkeit wurde die Substanz von der EU noch nicht eingestuft, eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ Choi D, Stables JP, Kohn H. Synthesis and anticonvulsant activities of N-Benzyl-2-acetamidopropionamide derivatives. J Med Chem. 1996;39:1907-16, PMID 8627614.

Bitte den Hinweis zu Gesundheitsthemen beachten!
Wikimedia Foundation.
