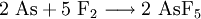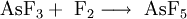- AsF5
-
Strukturformel 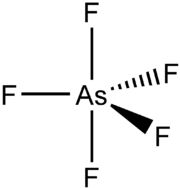
Allgemeines Name Arsen(V)-fluorid Andere Namen Arsenpentafluorid, Pentafluoroarsorane
Summenformel AsF5 CAS-Nummer 7784-36-3 Kurzbeschreibung farbloses Gas Eigenschaften Molare Masse 169,91 g·mol−1 Aggregatzustand gasförmig
Dichte 2,138 g·cm−3 (flüssig am Siedepunkt)[1]
Schmelzpunkt Siedepunkt −52,8 °C[1]
Löslichkeit Alkohol, Ether, Benzol[2]
Sicherheitshinweise Gefahrstoffkennzeichnung aus RL 67/548/EWG, Anh. I [3] 

Giftig Umwelt-
gefährlich(T) (N) R- und S-Sätze R: 23/25-50/53 S: (1/2)-20/21-28-45-60-61 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Arsenpentafluorid, AsF5, ist eine chemische Verbindung bestehend aus den Elementen Arsen und Fluor, in der Arsen die Oxidationsstufe +V besitzt.
Inhaltsverzeichnis
Darstellung
Arsenpentafluorid kann durch Reaktion direkt aus den Elementen dargestellt werden.[2]
Weitere Methoden sind die Fluorierung von Arsen(III)-fluorid oder Arsenoxiden mit elementarem Fluor.
Es kann auch ohne den Einsatz von elementarem Fluor aus Arsentrifluorid und Antimonpentafluorid mit Brom als Katalysator erhalten werden.
Eigenschaften
Arsenpentafluorid ist bei Raumtemperatur ein farbloses Gas. Es besitzt eine trigonal-bipyramidale Geometrie. Es ist ebenso wie Antimon(V)-fluorid eine starke Lewis-Säure, ein Fluorierungs- und Oxidationsmittel.
Reaktionen
Durch Wasser wird Arsenpentafluorid hydrolysiert. Es geht durch Reaktion mit Fluorid-Donatoren in das oktaedrisch gebaute Hexafluoroarsenat(V) über, z.B.:
![\mathrm{AsF_5 + SF_4 \longrightarrow SF_3^+ [AsF_6]^-}](/pictures/dewiki/55/79206063fe0ac3e6e1755412beb4dd24.png) .
.
Quellen
- ↑ a b c Eintrag zu Arsen(V)-fluorid in der GESTIS-Stoffdatenbank des BGIA, abgerufen am 24.12.2007 (JavaScript erforderlich)
- ↑ a b G. Brauer (Hrsg.), Handbook of Preparative Inorganic Chemistry 2nd ed., vol. 1, Academic Press 1963, S. 198-9.
- ↑ Nicht explizit in RL 67/548/EWG, Anh. I gelistet, fällt aber dort mit der angegebenen Kennzeichnung unter den Sammelbegriff „Arsenverbindungen“; Eintrag in der GESTIS-Stoffdatenbank des BGIA, abgerufen am 31. März 2009 (JavaScript erforderlich)
Literatur
- O. Ruff, W. Menzel und H. Plaut, Z. anorg. allg. Chem. 206/-/1932 S. 61ff.
Wikimedia Foundation.