- Chemische Verbindung
-
Als chemische Verbindung bezeichnet man einen Reinstoff, der aus zwei oder mehr verschiedenen chemischen Elementen besteht, die – im Gegensatz zu Gemischen – in einem festen Atomanzahl- und daher auch Massenverhältnis zueinander stehen. Charakteristisch für jede chemische Verbindung ist ihre eindeutige Chemische Struktur. Oft nicht eindeutig ist die Summenformel, mit der man unter Verwendung der molaren Masse beispielsweise die Menge an Produkten einer chemischen Reaktion errechnen kann (in der Stöchiometrie, mit Hilfe eines Reaktionsschemas). Isomere chemische Verbindungen besitzen dieselbe Summenformel, aber eine unterschiedliche Molekülstruktur.
Inhaltsverzeichnis
Arten von chemischen Verbindungen
Grob unterscheidet man bei den über 17 Millionen bekannten chemischen Verbindungen ionische, d. h. salzartige Verbindungen sowie Komplexe, metallische sowie molekulare Verbindungen. Auch die Unterteilung anorganisch/organisch ist grundlegend, wobei als „organisch“ die Kohlenstoff-Verbindungen bezeichnet werden (mit wenigen Ausnahmen). Anorganische Verbindungen gibt es etwa eine halbe Million, organische Verbindungen über 16 Millionen.
Grundsätzlich gibt es also im Hinblick auf die Art der Bindung zwischen den beteiligten Elementen vier Arten von chemischen Verbindungen:
- Molekulare Verbindungen (in der Regel aus einem nichtmetallischen Element und einem oder mehreren weiteren Nichtmetallen)
- Ionische Verbindungen (in der Regel aus einem Metall und einem oder mehreren Nichtmetallen)
- Metallische Verbindungen (aus Metallen)
- Komplexe Verbindungen (aus Metall-Kationen und Ionen oder Molekülen)
Eine genauere Unterscheidung von Verbindungen und deren Zuordnung zu einem dieser vier Typen kann mit Hilfe der Elektronegativitäts-Differenz der an der Bindung beteiligten Elemente vorgenommen werden. Zudem gibt es Übergangsformen zwischen den vier o. g. Idealtypen.
Molekulare Verbindungen
Molekulare Verbindungen entstehen aus Nichtmetall und Nichtmetall – sie sind Nichtleiter (Isolatoren) mit zumeist relativ niedrigem Siedepunkt (diamantartige oder kunststoffartige Verbindungen mit Riesenmolekülen ausgenommen).
Die kleinsten Teilchen molekularer Verbindungen sind neutrale Atomverbände (Moleküle). Diese bestehen aus zwei Atomen (zum Beispiel im Kohlenmonoxid, CO), aus drei Atomen (zum Beispiel im Kohlendioxid) oder auch aus einigen Tausend oder Zehntausend Atomen (Riesenmoleküle, Polymere, zum Beispiel im Kunststoff Polyethylen oder im Erbgut-Molekül Desoxyribonukleinsäure DNS). Die Atome in den Molekülen sind über Atombindungen verknüpft, das heißt, dass die miteinander verbundenen Atome Paare von Außenelektronen gemeinsam nutzen (Elektronenpaarbindung).
Beispiele für molekulare Verbindungen sind neben Wasser auch Methangas, Zucker, Kohlensäure, Polyethylen usw.
Ionische Verbindungen
Ionische Verbindungen (Salze) bestehen aus Kationen und Anionen. Sie sind oft salzartig:
- spröde,
- kristallförmig
- von hohem Schmelz- und Siedepunkt und
- elektrisch leitfähig nur in Schmelze oder Lösung.
Die Ionen entstehen bei der Reaktion von Metall- und Nichtmetallatomen dadurch, dass die Metallatome Elektronen abgeben (Oxidation), die dann von den Nichtmetallatomen aufgenommen werden (Reduktion). Die so gebildeten Metall-Kationen und Nichtmetall-Anionen vereinigen sich auf Grund der elektrischen Anziehungskräfte zu Ionenkristallen. Nach den Nichtmetallen unterscheidet man bei ionischen Verbindungen zum Beispiel Oxide (Sauerstoff als Anion), Sulfide (mit Schwefel), Fluoride, Chloride, Bromide, Iodide, Nitride (mit Stickstoff), Carbide (mit Kohlenstoff), Hydride (mit Wasserstoff) usw. Oft kommt Sauerstoff als drittes Element hinzu; man spricht dann von Sulfaten, Chloraten, Nitraten, Carbonaten usw.
Beispiele für Ionenverbindungen sind Eisen(III)-oxid (dem Rost ähnlich), Pyrit (Eisensulfid), Natriumchlorid (Kochsalz) und Kalziumsulfat (Gips).
Intermetallische Verbindung
Intermetallische Verbindung (umgangssprachlich oft auch als Legierungen bezeichnet) entstehen aus Metall und Metall – sie sind:
- elektrisch leitfähig
- gut verformbar
- glänzend und
- gute Wärmeleiter
- bei Zimmertemperatur meistens fest.
Beile aus Bronzelegierungen. Bronze war der erste von Menschen hergestellte Werkstoff (s. unter Bronzezeit)
Die Vereinigung von unterschiedlichen Metallen zu Legierungen kann – ins Besondere beim Zusammengießen von Metallschmelzen – in beliebigen Mengenverhältnissen erfolgen.
Wenn sich jedoch „intermetallische Verbindungen“ bilden, so sind in ihnen die beteiligten Elemente nur in ganz bestimmten Mengenverhältnissen enthalten („intermetallische Phase“, „stöchiometrische Zusammensetzung“, s. unter Stöchiometrie).
Beispiele für Legierungen sind Bronze (aus Kupfer und Zinn), Messing (Kupfer mit Zink) und Kupfernickel (als Münzmetall). Beispiele für intermetallische Verbindungen sind die zwischen Magnesium und Germanium (Formel: Mg2Ge), das Al2Cu, das Magnesiumsilicid Mg2Si, die Bronze Cu4Sn sowie das Zementit Fe3C (aus Eisen und Kohlenstoff, wobei dieser sich wie ein Metall verhält) und WC (Wolframcarbid).
Komplexe
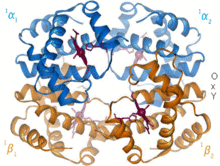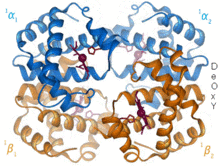 Der Blutfarbstoff Hämoglobin – ein Eisenkomplex im Blut, dessen Struktur sich mit der Aufnahme (Oxygenation) bzw. der Abgabe von Sauerstoff (Desoxygenation) ändert. (Komplexbildungsreaktion)
Der Blutfarbstoff Hämoglobin – ein Eisenkomplex im Blut, dessen Struktur sich mit der Aufnahme (Oxygenation) bzw. der Abgabe von Sauerstoff (Desoxygenation) ändert. (Komplexbildungsreaktion)
Verbindungen höherer Ordnung (Komplexe) entstehen bei einer Komplexbildungsreaktion zumeist aus Buntmetallkation und Molekülen mit freien Elektronenpaaren (Liganden). Sie sind oft auffallend farbig.
Beispiele: Der rote Blutfarbstoff Hämoglobin aus Eisen-II-Ionen und Eiweißmolekülen und der tiefblaue Kupfertetrammin-Komplex aus Kupfer-II-Ionen und Ammoniak.
Binäre, ternäre und quaternäre Verbindungen
Chemische Verbindungen lassen sich auch über die Anzahl der beteiligten chemischen Elemente einteilen.
Binäre Verbindungen setzen sich aus zwei verschiedenen Elementen zusammen und haben die allgemeine Formel AxBy. Chlorwasserstoff (HCl), Natriumfluorid (NaF) und Wasser (H2O) setzen sich jeweils aus zwei Elementen zusammen und sind damit alle binäre Verbindungen. Die Verbindungen können molekulare, ionische (Salze) oder intermetallische Verbindungen sein.
Analog dazu setzen sich ternäre Verbindungen aus drei verschiedenen Elementen zusammen, wie zum Beispiel Natriumcarbonat (Na2CO3), das sich aus Natrium, Kohlenstoff und Sauerstoff zusammensetzt.
Eine quaternäre Verbindung ist beispielsweise Kaliumhydrogencarbonat (KHCO3).
Der Begriff primäre Verbindung macht hingegen keinen Sinn, da definitionsgemäß chemische Verbindungen aus mindestens zwei Elementen zusammengesetzt sein müssen. Unterschiedliche Stoffe aus nur einem Element werden Modifikationen genannt. Gelegentlich wird auch der Begriff Elementverbindung verwendet.
Organische Verbindungen
Molekulare Verbindungen, in denen Kohlenstoff in Verbindung mit Wasserstoff enthalten ist, werden als „organisch“ bezeichnet. Sie bilden den weitaus größten Teil aller chemischen Verbindungen und leiten sich vom Methangas, der Gruppe der Alkane bzw. den Kohlenwasserstoffen ab. Im Kohlenwasserstoffgerüst organischer Verbindungen befinden sich oft weitere Atomgruppen, die die Eigenschaften der organischen Verbindung beeinflussen.
Dem Kohlenstoffgerüst entsprechend werden organische Verbindungen unterteilt in:
- aliphatische Kohlenwasserstoffe (Aliphaten, hierunter acyclische Kohlenwasserstoffe, gesättigte (Alkane), ungesättigte (Alkene und Alkine) und cyclische Kohlenwasserstoffe),
- aromatische Kohlenwasserstoffe (Aromaten, unterteilt in einfache Aromaten und kondensierte Aromaten),
- Heterocyclen sowie
- biochemische Verbindungen (Alkaloide, Aminosäuren, Kohlenhydrate, Proteine, Steroide, Terpene, Vitamine usw.)
Den funktionellen Gruppe entsprechend teilt man organische Verbindungen ein in
- Sauerstoff- und Hydroxyverbindungen (Alkohole, Aldehyde, Ester, Ether, Ketone, Carbonsäuren usw.),
- Stickstoffverbindungen (Amine, Amide, Nitroverbindungen, Nitrile),
- Schwefelverbindungen (Alkanthiole, Sulfide und Disulfide, Ester der Schwefelsäure, Sulfone, Sulfoxide, Thionamide, Thiolester, Thiosäure),
- Phosphorverbindungen (Phosphate, Phosphine),
- Metallorganische Verbindungen.
Siehe auch
- Organische Verbindung
- GHS = Global harmonisiertes System zur Einstufung und Kennzeichnung von Chemikalien
Weblinks
 Wiktionary: chemische Verbindung – Bedeutungserklärungen, Wortherkunft, Synonyme, Übersetzungen
Wiktionary: chemische Verbindung – Bedeutungserklärungen, Wortherkunft, Synonyme, Übersetzungen
Wikimedia Foundation.




