- Overman-Umlagerung
-
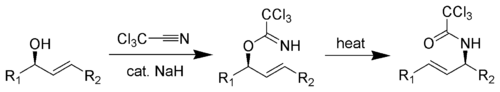
Die Overman-Umlagerung stellt eine Spezialform der Claisen-Umlagerung dar. Dabei wird ein Allylalkohol mit Trichloracetonitril zum Trichloracetimidat umgesetzt. Dieser lagert dann in einer Claisen-Umlagerung zum allylischen Trichloracetamidat um.[1][2][3][4] Die Reaktion wurde nach ihrem Entdecker dem amerikanischen Chemiker Larry E. Overman benannt.
Die [3,3]-sigmatrope Umlagerung ist eine diastereoselektive Umlagerung und wird in Gegenwart von Hitze und katalytischen Mengen an Quecksilber(II)- oder Palladium(II)-Salzen durchgeführt. Die so erhalten Allylamin-Verbindungen können zur Herstellung biologisch bedeutender Verbindungen und nicht-natürlicher Aminosäuren verwendet werden.[5] Die Overman-Umlagerung kann auch enantioselektiv mit Hilfe eines chiralen Auxiliars katalysiert werden.[6][7]
Einzelnachweise
- ↑ L. E. Overman: "A general method for the synthesis of amines by the rearrangement of allylic trichloroacetimidates. 1,3 Transposition of alcohol and amine functions", in: J. Am. Chem. Soc. 1976, 98 (10), 2901–2910; doi:10.1021/ja00426a038.
- ↑ L. E. Overman: "Allylic and propargylic imidic esters in organic synthesis", in: Accounts of Chemical Research 1980, 13 (7), 218–224; doi:10.1021/ar50151a005.
- ↑ L. E. Overman: Organic Syntheses Coll. Vol. 6, 507.
- ↑ L. E. Overman: "Thermal and mercuric ion catalyzed [3,3]-sigmatropic rearrangement of allylic trichloroacetimidates. 1,3 Transposition of alcohol and amine functions", in: J. Am. Chem. Soc. 1974, 96 (2), 597–599; doi:10.1021/ja00809a054.
- ↑ Y. K. Chen, A. E. Lurain, P. J. Walsh: "A General, Highly Enantioselective Method for the Synthesis of D and L α-Amino Acids and Allylic Amines", in: J. Am. Chem. Soc. 2002, 124 (41), 12225–12231; doi:10.1021/ja027271p.
- ↑ C. E. Anderson, L. E. Overman: "Catalytic Asymmetric Rearrangement of Allylic Trichloroacetimidates. A Practical Method for Preparing Allylic Amines and Congeners of High Enantiomeric Purity", in: J. Am. Chem. Soc. 2003, 125 (41), 12412–12413; doi:10.1021/ja037086r.
- ↑ Asymmetric Overman Rearrangement, Organic Syntheses 2005, 82, 134.
Literatur
- M. Isobe, Y. Fukuda, T. Nishikawa, P. Chabert, T. Goto, in: Tetrahedron Lett. 1990, 31, 3327.
- T. Allmendinger, E. Felder, E. Hungerbühler, in: Tetrahedron Lett. 1990, 31, 7301–7304.
- T. Nishikawa, M. Asai, N. Ohyabu, M. Isobe: "Improved Conditions for Facile Overman Rearrangement", in: J. Org. Chem. 1998, 63 (1), 188–192; PMID 11674062.
Wikimedia Foundation.