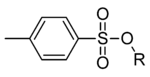
- Para-Toluolsulfonsäurechlorid
-
Strukturformel 
Allgemeines Name para-Toluolsulfonsäurechlorid Andere Namen - Toluol-4-sulfonylchlorid
- Toluol-4-sulfonsäurechlorid
- 4-Methylbenzol-1-sulfonylchlorid
- p-Toluolsulfochlorid
- Tosylchlorid
- p-Toluolsulfonylchlorid
- Toluol-4-sulfochlorid
- TosCl
- TsCl
Summenformel C7H7ClO2S CAS-Nummer 98-59-9 Kurzbeschreibung weißer bis grauer Feststoff[1] Eigenschaften Molare Masse 190,64 g·mol−1 Aggregatzustand fest
Dichte 1,49 g·cm−3[1]
Schmelzpunkt Siedepunkt 135 °C (13 hPa)[1]
Dampfdruck Löslichkeit Zersetzung mit Wasser[1]
Sicherheitshinweise Gefahrstoffkennzeichnung [1] 
Ätzend (C) R- und S-Sätze R: 34 S: 26-36/37/39-45 LD50 4680 mg/kg (Ratte, oral)[2]
WGK 1[1] Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. para-Toluolsulfonsäurechlorid ist eine chemische Verbindung aus der Gruppe der Sulfonsäuren. Sie ist das Säurechlorid der para-Toluolsulfonsäure und wird umgangssprachlich oft als Tosylchlorid, geschrieben TsCl, bezeichnet.
Inhaltsverzeichnis
Darstellung
Die Verbindung kann durch eine Reaktion ähnlicher einer Friedel-Crafts-Alkylierung aus Toluol hergestellt werden. Hierzu wird Toluol mit Sulfurylchlorid und Aluminiumchlorid als Katalysator zur Reaktion gebracht.[3]
Eine weitere Möglichkeit besteht in der Umsetzung von para-Methylanilin in einer sandmeyer-ähnlichen Reaktion. Hierzu wird das Amin zunächst mit Natriumnitrit diazotiert. Das entstandene Diazoniumsalz wird dann mit Schwefeldioxid in Gegenwart von Kupfer(I)-chlorid und Magnesiumchlorid zur Reaktion gebracht.[4]
Tosylchlorid ist ein Abfallprodukt der Saccharin-Herstellung. Hier entstehen neben dem hierfür benötigte o-Toluolsulfonylchlorid auch das p-Toluolsulfonylchlorid welches nach der Trennung voneinander als Feinchemikalie veräußert wird.[5]
Eigenschaften
para-Toluensulfonsäurechlorid ist ein ätzender Feststoff mit einem charakteristischem eigentümlichem Geruch, der bei 67 °C schmilzt und bei 135 °C bei einem Druck von 13 hPa siedet. Ab einer Temperatur von 220 °C zersetzt er sich.[1]
Verwendung
p-Tosylchlorid wird in der organischen Chemie zur Herstellung von Tosylaten aus Alkoholen verwendet. Hierzu wird der Alkohol zunächst durch Einsatz einer Base deprotoniert. Das entstandene Alkoholat geht nun eine nukleophile Substitution mit p-Tosylchlorid ein, wobei das am Schwefel gebundene Chlorid als Abgangsgruppe dient. Tosylate dienen dazu Hydroxylgruppen in Abgangsgruppen umzuwandeln, was durch Bildung des Tosylats, das selbst eine gute Abgangsgruppe darstellt, erreicht werden kann.[5]
Literatur
- Reinhard Brückner: Reaktionsmechanismen. 3. Auflage, Spektrum Akademischer Verlag, München 2004, ISBN 3-8274-1579-9.
- Autorenkollektiv: Organikum. 22. Auflage. Wiley-VCH, 2004, ISBN 978-3527311484.
Quellen
- ↑ a b c d e f g h i Eintrag zu CAS-Nr. 98-59-9 in der GESTIS-Stoffdatenbank des BGIA, abgerufen am 27.07.2008 (JavaScript erforderlich)
- ↑ Sicherheitsdatenblatt Merck
- ↑ A. Töhl, O. Eberhard: Ueber die Einwirkung des Sulfurylchlorids auf aromatische Kohlenwasserstoffe, in: Chem. Ber. 1893, 26, 2940–2945. doi:10.1002/cber.189302603118
- ↑ H. Meerwein, G. Dittmar, R. Göllner, K. Hafner, F. Mensch, O. Steinfort: Untersuchungen über aromatische Diazoverbindungen, II. Verfahren zur Herstellung Aromatischer Sulfonsäurechloride, Eine Neue Modifikation der Sandmeyerschen Reaktion, in: Chem. Ber. 1957, 90', 841–852. doi:10.1002/cber.19570900602
- ↑ a b H. Beyer, W. Walter: Lehrbuch der organischen Chemie, S. Hirzel Verlag Stuttgart, 19. Auflage 1981, 514 ISBN 3-7776-0356-2
Wikimedia Foundation.