- Psilocyn
-
Strukturformel 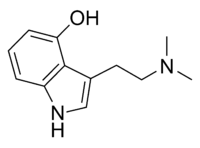
Allgemeines Name Psilocin Andere Namen - 4-Hydroxy-N,N-dimethyltryptamin (4-OH-DMT)
- 3-[2-(Dimethylamino)ethyl]-1H-indol-4-ol
Summenformel C12H16N2O CAS-Nummer 520-53-6 PubChem 4980 Kurzbeschreibung farblose Kristalle Eigenschaften Molare Masse 204,27 g·mol−1 Aggregatzustand fest
Schmelzpunkt Löslichkeit sehr schlecht in Wasser löslich [2], löslich in Methanol
Sicherheitshinweise Gefahrstoffkennzeichnung [3] 
Gesundheits-
schädlich(Xn) R- und S-Sätze R: 22 S: 36/37/39 LD50 7 mg·kg−1 (Kaninchen, i.v.) [3]
WGK 3 [3] Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Psilocin ist ein Indolalkaloid und zählt zu den Tryptaminen. Es ist das Hydrolyse-Produkt des Psilocybins und ist als solches die eigentlich psychoaktive Form des Psilocybins. Daneben kommt es aber auch selbst als Alkaloid vor. Die freie Base zersetzt sich an der Luft. Wegen seiner halluzinogenen Wirkung wird es oft als Rauschmittel verwendet. Die Folgen eines Konsums ähneln einem LSD-Rausch, sind jedoch in der Regel kürzer und weniger intensiv.
Inhaltsverzeichnis
Geschichte
Albert Hofmann und sein Laborassistent Hans Tscherter bei Sandoz isolierten 1959 Psilocin und seinen Phosphatester Psilocybin aus halluzinogenen Pilzen.
Chemie
Psilocin entsteht bei der Dephosphorylierung von Psilocybin, z.B. unter stark sauren oder alkalischen Bedingungen. Psilocin ist wegen seiner phenolischen OH-Gruppe relativ instabil.
Unter alkalischen Bedingungen und in Anwesenheit von Sauerstoff bildet es sofort bläuliche und stark blaue Abbauprodukte. Ähnliche Produkte entstehen auch unter sauren Bedingungen, der Anwesenheit von Sauerstoff und Eisen(III)-Ionen (Keller-Reagenz FeCl3 / MeOH / HCl).
Psilocin ist ein basisches Amin. Seine Salze, die es z.B. mit Säuren bilden kann, sind normalerweise stabiler als Psilocin.
Pharmakologie
Psilocin ist ein Partialagonist am 5-HT2A-Rezeptor[4] und gehört somit zu den klassischen Halluzinogenen. Sein Bindungprofil (soweit es bekannt ist) ist weniger komplex als das von LSD. Die Bindung von Psilocin am 5-HT2C-Rezeptor ist wahrscheinlich für Nebeneffekte verantwortlich (z.B. auf den Blutzuckerspiegel).
Nebenwirkungen des Konsums
Fälle von HPPD sind bekannt - Im Extremfall Auslösung von Drogenpsychosen.[5]
Toxizität
Das Verhältnis von Wirkdosis zu tödlicher Dosis liegt im Vergleich zu anderen psychoaktiven Substanzen weit auseinander. Würde das Psilocin in Form von frischen Pilzen (sog. Magic Mushrooms) konsumiert, läge die Dosis für eine physiologisch tödliche Vergiftung bei etwa 1 kg Pilzen / kg Körpergewicht.
Rechtslage
Deutschland
Mit der Vierten Betäubungsmittel-Gleichstellungsverordnung (4. BtMGlV)[6] vom 21. Februar 1967, in Kraft getreten am 25. Februar 1967, wurden Psilocybin und Psilocin in der Bundesrepublik Deutschland den betäubungsmittelrechtlichen Vorschriften des Opiumgesetzes unterstellt. Heute sind Psilocybin und Psilocin in Anlage I zu § 1 BtMG (nicht verkehrsfähige und nicht verschreibungsfähige Stoffe) aufgelistet. Der Erwerb, der Besitz und die Weitergabe dieser Substanzen ist somit generell verboten.
Quellen
- ↑ Thieme Chemistry (Hrsg.): Römpp Online. Version 3.1. Georg Thieme Verlag, Stuttgart 2007.
- ↑ The Merck Index. An Encyclopaedia of Chemicals, Drugs and Biologicals. 14. Auflage, 2006, S. 1363, ISBN 978-0-911910-00-1.
- ↑ a b c Sicherheitsdatenblatt von Sigma-Aldrich
- ↑ David E. Nichols (2004): Hallucinogens. In: Phamacol. Ther. 101:131-181. PDF
- ↑ Espiard ML. et al. (2005): Hallucinogen persisting perception disorder after psilocybin consumption: a case study. In: Eur. Psychiatry. 20(5-6):458-460. PMID 15963699
- ↑ 4. BtMGlV vom 21. Februar 1967
Weblinks
- TIHKAL: Psilocin
Wikimedia Foundation.
