- Technetiumphytat
-
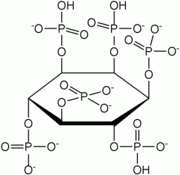
Strukturformel 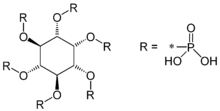
Allgemeines Name Phytinsäure Andere Namen IP6
Summenformel C6H18O24P6 CAS-Nummer 83-86-3 PubChem 890 ATC-Code V09DB07
Eigenschaften Molare Masse 660,08 g/mol Sicherheitshinweise Gefahrstoffkennzeichnung [1] keine Gefahrensymbole R- und S-Sätze R: keine R-Sätze S: keine S-Sätze Bitte beachten Sie die eingeschränkte Gültigkeit der Gefahrstoffkennzeichnung bei Arzneimitteln WGK 3[1] Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Phytinsäure (Hexaphosphorsäureester des Inosits, IP6) gehört zu den bioaktiven Substanzen. Sie dient in Pflanzen wie z. B. Hülsenfrüchten, Getreide und Ölsamen als Speicher für Phosphat und Ionen (für Kalium-, Magnesium-, Calcium-, Mangan-, Barium- und Eisen-II-Ionen), die der Keimling zum Wachstum benötigt. Aufgrund seiner komplexbildenden Eigenschaften kann es vom Menschen mit der Nahrung aufgenommen, Mineralstoffe im Magen und Darm wie Calcium, Magnesium, Eisen und Zink unlöslich binden, so dass sie dem Körper nicht mehr zur Verfügung stehen. Phytinsäure kommt in der Natur als Anion, Phytat genannt, vor. Besonders viel Phytat ist in Mais, Soja, Weizen- und Gerstekleie enthalten, aber nicht in Roggenkleie.
Inhaltsverzeichnis
Mineralstoffwechsel und Phytat
Nicht viele Mineralien werden direkt vom Magen aufgenommen, die meisten werden erst in Dünn- oder Dickdarm resorbiert. Mit den Mineralien aufgenommene Substanzen, die diese binden und selbst aber nicht aufgenommen werden, können daher eine Aufnahme der Mineralien durch den Körper noch im Darm verhindern. Phytinsäure hat diese Eigenschaft. Hinzu kommt, dass Kalzium, Magnesium und Zink in einem Recycling-Prozess über die Bauchspeicheldrüse ausgeschieden und später vom Darm rückresorbiert werden. Phytat kann daher bei diesen Ionen einen echten Mangel verursachen - wenn es in reinem Zustand oder großen Mengen gegessen wird, beispielsweise bei einer reinen Ernährung mit Soja.
Vor- und Nachteile
Phytinsäure wurde bisher nur als unerwünschter Inhaltsstoff in Lebensmitteln angesehen, da die von ihr in der Pflanze gebundenen Mineralstoffe vom Körper nicht aufgenommen werden können. Bei der Herstellung von Vollkornprodukten wird deshalb durch spezielle Teigführung der Phytingehalt reduziert. Einige Vertreter der Vollwerternährung glauben jedoch, dass die Eigenschaft, Mineralien zu binden, in einer ausgewogenen Mischkost keinen wesentlichen Nachteil darstellt. Diese Kost sollte jedoch durch eine zusätzliche Zinkquelle in Form von Mineralsupplementen ergänzt werden.
Phytinsäure verzögert z. B. den Abbau von Stärke im Körper. Dadurch könne nach Ansicht einiger Anhänger der Vollwerternährung die Blutzuckerkonzentration reguliert werden. Darüber hinaus würde Phytinsäure ein Zuviel an Metallionen, vor allem Eisen, in der Nahrung binden, welche ein erhöhtes Risiko für Darmkrebs darstellen würden.
Phytat und Gülle
Wiederkäuer sind die einzigen Säugetiere, die Phytinsäure abbauen und das dabei anfallende Phosphat verwerten können, da sie in ihren Mägen spezielle Bakterien als Flora besitzen. Diese Bakterien produzieren ein Enzym, die Phytase, die den Abbau von Phytat zu Zucker und Phosphat ermöglicht.
Die Tatsache, dass nur Wiederkäuer in der Lage sind, Phytat zu verarbeiten und zu nutzen, ist der Grund dafür, dass Gülle vom Schwein und anderen Haustieren soviel Phosphat enthält. Dies führt in dichtbesiedelten Gebieten wie Deutschland oder Taiwan immer wieder zu einem Entsorgungs- und Umweltproblem. Aus diesem Grund fügt man in letzter Zeit das Phytase-Enzym bei der Fütterung von Schweinen hinzu, wodurch die Tiere auch besser ernährt sind, weil sie das Phosphat nun für sich nutzen.
Nuklearmedizin
Das radioaktive 99mTechnetiumphytat wird in der Nuklearmedizin als Tracer bei der statischen Leberszintigrafie verwendet.
Quellen
- Harland, BF. und Donald Oberleas, D.: Effects of Dietary Fiber and Phytate on the Homeostasis and Bioavailability of Minerals, in Gene A. Spiller (Editor): CRC Handbook of Dietary Fiber in Human Nutrition. Third Edition. CRC Press, 2001. ISBN 0849323878. S. 161-170.
- Shears, SB. (2001): Assessing the omnipotence of inositol hexakisphosphate. Cell. Signal. 13(3), 151-158; PMID 11282453
- Raboy, V. (2003): myo-Inositol-1,2,3,4,5,6-hexakisphosphate. Phytochemistry 64(6), 1033-1043, (2003)
- Alcazar-Roman, AR. et al. (2006): Inositol hexakisphosphate and Gle1 activate the DEAD-box protein Dbp5 for nuclear mRNA export. Nat. Cell Biol. 8(7), 711-716, PMID 16783363
- Weirich, CS.,et al. (2006): Activation of the DExD/H-box protein Dbp5 by the nuclear-pore protein Gle1 and its coactivator InsP6 is required for mRNA export. Nat. Cell Biol. 8(7), 668-676, PMID 16783364
Bitte beachte den Hinweis zu Gesundheitsthemen!
Wikimedia Foundation.