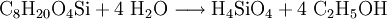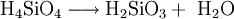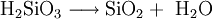- Tetraethoxyorthosilikat
-
Strukturformel 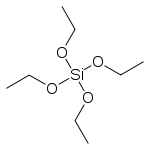
Allgemeines Name Tetraethylorthosilicat Andere Namen - Tetraethylorthosilikat
- Tetraethoxysilan
- Kieselsäuretetraethylester
- Ethylsilicat
- TEOS
Summenformel C8H20O4Si CAS-Nummer 78-10-4 PubChem 6517 Kurzbeschreibung farblose Flüssigkeit mit schwachem, angenehm fruchtigen Geruch Eigenschaften Molare Masse 208,32 g·mol−1 Aggregatzustand flüssig
Dichte 0,933 g·cm−3[1]
Schmelzpunkt Siedepunkt 168 °C [1]
Löslichkeit gut in Alkohol, nicht in Wasser
Sicherheitshinweise Gefahrstoffkennzeichnung aus RL 67/548/EWG, Anh. I [2] 
Gesundheits-
schädlich(Xn) R- und S-Sätze R: 10-20-36/37 S: (2) LD50 WGK 1 (schwach wassergefährdend) Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Tetraethylorthosilicat, auch Tetraethoxysilan, Kieselsäuretetraethylester oder Ethylsilicat, kurz TEOS genannt, ist ein Ethylester der Orthokieselsäure.
Inhaltsverzeichnis
Verwendung
Es wird in Sol-Gel-Prozessen als Siliciumdioxid-Prekursor zur Herstellung von kolloidalen Sol-Gel-Systemen benutzt. In Wasser ist die Verbindung weitgehend unlöslich. Als Reaktionsmedium wird daher meist ein Gemisch aus Ethanol und Wasser verwendet. Im Neutralen hydrolysiert TEOS in Wasser sehr langsam (mehrere Stunden) zu Orthokieselsäure und Ethanol:
wobei die gebildete Orthokieselsäure durch Ausbildung von Si–O–Si-Bindungen und Abgabe von Wasser weiter in Siliciumdioxid zerfällt:
Erheblich schneller erfolgt die Hydrolyse im Sauren oder Alkalischen, da beides die Reaktion erheblich katalysiert. Im Ammoniakalischen können aus einer TEOS/Ethanol-Mischung, die etwas Wasser enthält, monodisperse Siliciumdioxid-Partikel erhalten werden. Im sogenannten Stöber-Prozess[4] kann durch die Wahl der Konzentrationen, Temperaturen und Ammoniakmenge die Partikelgröße im Bereich von ca. 20–500 nm eingestellt werden. Das Verfahren wird beispielsweise zur Herstellung von photonischen Kristallen[5][6] und künstlichen Opalen[7] verwendet.
Herstellung
TEOS wird großtechnisch durch Alkoholyse von Siliciumtetrachlorid mit Ethanol hergestellt.
Quellen
- ↑ a b c www.chemdat.de: Tetraethylorthosilicat, Sicherheitsdatenblatt
- ↑ Eintrag zu CAS-Nr. 78-10-4 im European chemical Substances Information System ESIS
- ↑ Tetraethylorthosilicat bei ChemIDplus
- ↑ Werner Stöber, Arthur Fink, Ernst Bohn: Controlled growth of monodisperse silica spheres in the micron size range. In: J. Colloid Interface Sci., Nr. 26, 1968, Seiten 62–69
- ↑ Jian Li, Weihuan Huang, Zhe Wang, Yanchun Han: A reversibly tunable colloidal photonic crystal via the infiltrated solvent liquid–solid phase transition. In: Colloids and Surfaces A: Physicochemical and Engineering Aspects, Nr. 293, 2007, Seiten 130–134.
- ↑ Martyn E. Pemble, Maria Bardosova, Ian M. Povey, Richard H. Tredgold, Debra Whitehead : Novel photonic crystal thin films using the Langmuir–Blodgett approach, in Physica B: Condensed Matter, 394/2007, Seiten 233–237.
- ↑ L. Pallavidino, et al.: Synthesis, characterization and modelling of silicon based opals. In: Journal of Non-Crystalline Solids, Nr. 352, 2006, Seiten 1425–1429
Literatur
- K. Nozawa, et.al.: Smart control of monodisperse Stöber silica particles: effect of reactant addition rate on growth process. In: Langmuir, Nr. 21, 2005, Seiten 1516–1523.
- T. Suratwala, M. L. Hanna, P. Whitman: Effect of humidity during the coating of Stöber silica sols. In: Journal of Non-Crystalline Solids, Nr. 349, 2004, Seiten 368–376.
Siehe auch
Wikimedia Foundation.