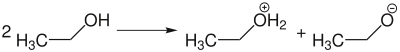- Ethanol
-
Strukturformel 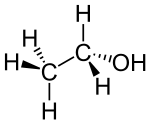
Keile zur Verdeutlichung der Geometrie Allgemeines Name Ethanol Andere Namen - Ethylalkohol
- Äthanol (standardsprachlich)
- Äthylalkohol (standardsprachlich)
- Weingeist
- Spiritus (vergällter Äthylalkohol)
- Alkohol (umgangssprachlich)
- ALCOHOL (INCI)
Summenformel C2H6O CAS-Nummer 64-17-5 PubChem 702 Kurzbeschreibung klare, farblose, würzig riechende und brennend schmeckende, leichtentzündliche, hygroskopische Flüssigkeit[1]
Eigenschaften Molare Masse 46,07 g·mol−1 Aggregatzustand flüssig
Dichte Schmelzpunkt Siedepunkt 78 °C[2]
Dampfdruck pKs-Wert 16[3]
Löslichkeit beliebig mit Wasser, Diethylether, Chloroform, Benzin und Benzol mischbar[1]
Brechungsindex 1,3638[1]
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung aus EU-Verordnung (EG) 1272/2008 (CLP) [4] 
Gefahr
H- und P-Sätze H: 225 EUH: keine EUH-Sätze P: 210 [2] EU-Gefahrstoffkennzeichnung aus EU-Verordnung (EG) 1272/2008 (CLP) [4] 
Leicht-
entzündlich(F) R- und S-Sätze R: 11 S: (2)-7-16 MAK 500 ml·m−3 bzw. 960 mg·m−3[2]
LD50 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C Ethanol, auch Äthanol, ist eine farblose, leicht entzündliche Flüssigkeit mit brennendem Geschmack und charakteristischem, würzigem Geruch,[11] die im allgemeinen Sprachgebrauch nur mit Alkohol, dem Namen seiner chemischen Substanzklasse, bezeichnet wird. Ältere Bezeichnungen sind Weingeist und Spiritus (lat. für Luft, Atem, Lebenshauch, Geist). In der Laborsprache wird Ethanol oft mit EtOH abgekürzt und in der Alltagsmedizin mündlich mit C2 bezeichnet (Verkürzung der Summenformel C2H6O bzw. der Halbstrukturformel C2H5OH). Eine wässrige Lösung mit 70 Vol% Ethanol wird in der Pharmazie Spiritus dilutus genannt.
Bekannt ist Ethanol vor allem als Trinkalkohol, der als Anteil in Genussmitteln (z. B. Wein, Bier, Likör) klassifiziert wird. Er ist allerdings zugleich ein Rauschmittel, dessen Konsum in den meisten Staaten erlaubt ist. Laut der Weltgesundheitsorganisation sterben jedes Jahr 2,5 Millionen Menschen an den Folgen des Alkoholkonsums.[12]
Ethanol ist ein wichtiges organisches Lösungsmittel, eine Grundchemikalie in der Industrie und ein Desinfektionsmittel. Eine der technischen Hauptverwendungen von Ethanol ist die Nutzung als Biokraftstoff, als so genanntes Bioethanol; beispielsweise enthält Ethanol-Kraftstoff E85 85 Vol.-% Ethanol.
Systematik
Ethanol (C2H5OH) gehört zu den n-Alkanolen. Es leitet sich von dem Alkan (gesättigten Kohlenwasserstoff) Ethan (C2H6) ab, in dem formal ein Wasserstoffatom durch die funktionelle Hydroxygruppe (–OH) ersetzt wurde. Zur Benennung wird dem Namen Ethan das Suffix -ol angehängt.
„Alkohol“ ist das umgangssprachliche Wort für „Ethanol“; die Fachbezeichnung „Alkohole“ hingegen steht für eine Gruppe organisch-chemischer Verbindungen, die neben dem Kohlenwasserstoffgerüst als zusätzliche Funktionelle Gruppe mindestens eine Hydroxygruppe besitzen, wobei sich an dem Kohlenstoffatom mit der Hydroxygruppe kein höherwertiger Substituent befindet.
Wortherkunft Alkohol
Im Arabischen stand الكحل / al-kuḥl ursprünglich für sehr feines Antimonpulver, das als Augenschminke benutzt wurde.[13] Im übertragenen Sinn war Alkohol die „geistige Essenz“, die für die „irdene Essenz“ als Lösungsmittel diente. (Im heutigen Arabisch bedeutet الكحول / al-kuḥūl jedoch, wie in den europäischen Sprachen, nur die Substanz Alkohol). Nach Europa gelangte dieser Begriff während der langen arabischen Herrschaft in Spanien.[14] Auch in der spanischen Sprache bedeutete alcohol ursprünglich feines, trockenes Pulver, was, als Bezeichnung für verschiedene Produkte von Sublimation und Destillation, in die Alchemistensprache Eingang fand. Erst Paracelsus benutzte alcool vini oder alcohol vini im heutigen, engeren Sinn für „Weingeist“, „Essenz des Weines“. Zuvor war für diesen Stoff der Name aqua ardens („brennendes Wasser“) oder aqua vitae („Lebenswasser“) gebräuchlich gewesen.
Kulturgeschichte des Alkohols
Ethanol entsteht auf natürlichem Wege bei der Vergärung zuckerhaltiger Früchte. Auf diese Weise wurden wohl unabhängig voneinander, schon in einem frühen Stadium der Geschichte, Menschen auf diese Substanz aufmerksam.[15] Laut Josef H. Reichholf (2008) geht der Ackerbau – und damit die Sesshaftwerdung – sogar in erster Linie aufs Bierbrauen zurück, da Met, ein „Honigwein“, nie ausreichend zur Verfügung stehen konnte. So finden sich in ägyptischen Schriftrollen der III. Dynastie[16] sowie auf alt-mesopotamischen Keilschrifttafeln[17] Hinweise auf die Herstellung alkoholischer Getränke. Auch in der Bibel wird der Alkohol erwähnt, etwa in Gen 9,18–29 LUT.
Biere, später auch Weine wurden mit Hilfe von Wildhefen erzeugt. Meist hatten solche Alltagsgetränke einen deutlich geringeren Alkoholgehalt als heute, da die Wildhefen ab einer bestimmten Alkoholkonzentration die Umwandlung von Zucker in Alkohol einstellen, weil sie sich ansonsten selbst vergiften würden. Durch jahrhundertelange Züchtung tolerieren heutige Kulturhefen (Saccharomyces cerevisiae) höhere Ethanolgehalte.
Auch in diesen alten Zeiten wurde Alkohol bereits aufgrund seiner berauschenden Wirkung getrunken. So heißt es in einem ägyptischen Text über das Verhalten junger Männer:
- „Du verlässt die Bücher und gehst von Schenke zu Schenke; der Biergenuss allabendlich, der Biergeruch verscheucht die Menschen von dir.“[16]
In der Antike wurde der Wein schließlich ein wesentlicher Bestandteil römischer und griechischer Kultur. Beide Kulturen bedachten ihn mit einer eigenen Gottheit: Bacchus bzw. Dionysos. Ebenso sahen die Germanen den Met, der ebenfalls zu den frühesten alkoholischen Getränken gehört, als Geschenk der Götter an.
Vermutlich wurde im Gebiet der heutigen Türkei um etwa 1000 n. Chr. die Destillation von Wein zur Herstellung hochprozentiger Branntweine entwickelt.[15] So war es möglich, den Spiritus vini (Geist des Weines) aus Wein herzustellen. In Ostasien wurden schon früh Weine aus Litschi und Pflaumen hergestellt sowie der Sake, ein warm genossener Reiswein, dessen Herstellungsprozess dem des Bieres ähnelt.
Während des Dreißigjährigen Krieges stieg in Mitteleuropa der Bedarf an berauschenden Getränken (Verarmung, Zerrüttung), während das Angebot stagnierte (Ernteausfälle, Rückgang des Weinbaus, Unsicherheit des Transportes). Mit Branntwein konnte dem am leichtesten begegnet werden. Der Handel, z.T. auch die Produktion der Spirituosen lagen damals in Osteuropa oft in den Händen von Juden,[18] während ihnen dies in Westeuropa teilweise verboten war.
Mitte des 18. Jahrhunderts vergrößerte sich mit der Neuen Welt die landwirtschaftlich nutzbare Fläche des Königreichs England um ein Vielfaches. Dies führte in der Folge zu sinkenden Getreidepreisen und einer damit verbundenen Verarmung der Unterschicht. Die Überproduktion an Getreide wurde zum Teil zur Herstellung von Gin genutzt, der in den Armenvierteln des Mutterlandes dankbare Abnehmer fand. Zeitweise kostete eine Kalorie Gin weniger als eine Kalorie Brot.[19] In der Folge entwickelte sich die Gin-Krise, welche die damalige Regierung erst durch eine Reihe von Gesetzen (hohe Steuern auf Gin, Erschwerung des Handels, Ausgabe von Lizenzen für Händler, etc.) beenden konnte. Erst aus dieser Zeit finden sich die ersten Schriften, die sich mit Alkoholabhängigkeit und deren Folgeerkrankungen beschäftigen. Ebenso wurde vor diesem Hintergrund Alkohol zum ersten Mal als Ursache für gesellschaftliche Probleme und Fehlentwicklungen verstanden.[19]
Während sich der Alkoholkonsum Mitte des 19. Jahrhunderts wieder verringerte, begann mit der Industrialisierung wiederum eine Zeit, in der sehr billiger Alkohol auf breite verarmte Bevölkerungsschichten traf. Die industrielle Produktion und die, vor allem nach dem Zweiten Weltkrieg einsetzende, massive Vermarktung der alkoholischen Getränke führten zu einem großen Überangebot in der 1. und 2. Welt. So wurden die Frauen und seit kurzem die Jugendlichen zu Zielgruppen der Nachfrage- und Absatzförderung. Inzwischen zählt man die alkoholbedingten Schäden zu den Zivilisationskrankheiten.
Vorkommen in Lebensmitteln und Getränken
Ethanol ist ein in reifen Früchten und Säften natürlich vorkommendes Produkt der alkoholischen Gärung. Wegen seiner stimulierenden und stimmungsaufhellenden Wirkung werden alkoholische Getränke gern und häufig konsumiert. Alkohol als Rauschmittel ist die am weitesten verbreitete Droge weltweit; regelmäßiger Konsum kann zu Alkoholismus führen.
Volumenanteile
Ethanolgehalte verschiedener Lebensmittel, Angabe in Volumenprozent:
- alkoholfreies Bier: bis 0,5 % Vol.
- Apfelsaft: bis 0,4 % Vol.
- Banane (reif): bis 1 % Vol. (durchschnittlich 3 ml)
- Brot: bis 0,3 % Vol.
- Kefir (reif): bis ca. 1 % Vol.
- Sauerkraut: 0,5 % Vol.
- Traubensaft: bis 0,6 % Vol.
Siehe auch Getränk#Ethanolgehalt alkoholischer Getränke
Kennzeichnung
In Zutatenlisten in der Europäischen Union muss Alkohol nicht eigens genannt sein. Wenn dort bei Marmelade oder Pralinen zum Beispiel „Armagnac“ oder „Knickebein“ steht, liegt es in der Verantwortung des Verbrauchers, zu wissen oder zu erkunden, dass das Produkt für Kinder oder trockene Alkoholiker ungeeignet sein kann. Es gibt kein einheitliches Symbol zur Kennzeichnung alkoholhaltiger Lebens- und Genussmittel.
Herstellung
Zum ersten Mal ist die Gewinnung von reinem Alkohol dem persischen Arzt, Naturwissenschaftler, Philosophen und Schriftsteller Abu Bakr Mohammad Ibn Zakariya al-Razi († 925) durch die Destillation aus Wein gelungen. Alkohol wird seit jeher fast ausschließlich aus Zucker- oder Stärke-haltigen Feldfrüchten oder traditionell aus Produkten des Gartenbaus (Wein, Obst) gewonnen.
Heute wird Ethanol hauptsächlich durch Gärung aus Biomasse gewonnen. Im Kontext der Erzeugung von Biokraftstoff spricht man dabei auch von Bioethanol. Agraralkohol ist Ethanol aus Agrarrohstoffen, das in weltweit, in Deutschland unter staatlicher Aufsicht in landwirtschaftlichen Brennereien erzeugt wird.
Die Synthese von Alkohol ist auch aus Mineralöl möglich, aber selbst in der Periode niedriger Rohölpreise (1900–1973) wurde Alkohol vorzugsweise aus nachwachsenden Rohstoffen erzeugt. Daher ist die Bezeichnung Bioalkohol lediglich ein Marketingaspekt, der für die weltweite Produktion unter den aktuellen Preisbedingungen (2010) belanglos bleibt.
Ethanol kann auch durch chemische Synthese aus Wasser und Ethen unter Zugabe von Katalysatoren wie Schwefelsäure[20] oder auf Silika aufgebrachte Phosphorsäure bei bis zu 300 °C und 70 bar Druck hergestellt werden.
Industriell wird synthetisches Ethanol mittels Phosphorsäurekatalyse hergestellt. Mittels der Radiokohlenstoffdatierung lässt sich synthetisches Ethanol aus fossilen Rohstoffen von Bio-Ethanol aus nachwachsenden Rohstoffen unterscheiden. Dieser Umstand lässt sich zum Nachweis des Panschen von Wein oder Spirituosen nutzen, wenn mit industriellem Ethanol anstelle von Bio-Ethanol gepanscht wird.
Produktionsmengen
Weltweit werden etwa 330 Millionen hl (33 Mrd. l) Ethanol hergestellt, wovon mit 42 Mio. hl etwa 13 % auf die europäischen Länder fallen. Größte europäische Erzeuger sind Russland und Frankreich. Deutschland erzeugt jährlich fast 4 Mio. hl zu gleichen Teilen als Getränkealkohol und als Alkohol für chemisch-technische Zwecke, was einer Eigenbedarfsdeckung von etwa 62 % entspricht. Neben der Produktion von Neutralalkohol für Getränke, Lebensmittel und technische Zwecke fallen weltweit etwa 65 % auf die Herstellung von Kraftstoffethanol.[21]
Weltweit erzeugten die USA und Brasilien 2005 zusammen über 90 % der Jahresproduktion von 365,67 Mio. hl (36,567 Mrd. l).[22] In den USA wird der Aufbau neuer Produktionsanlagen für Ethanol derzeit besonders forciert, vor allem durch das Gesetz „Energy Policy Act“ (EPACT) von 2005, das den Ausbau von erneuerbaren flüssigen Energieträgern fördern soll. In Brasilien werden gegenwärtig ca. 21 Mrd. Liter – nach 17,3 Mrd. l 2006 und 18,3 Mrd. l 2007[23] – Ethanol hergestellt. Im Jahre 2010 soll die Produktionsmenge bei ca. 30 Mrd. Liter liegen. In Brasilien wird Ethanol zu einem günstigen Preis von 16 ct/l aus Zuckerrohr hergestellt; in den USA müssen für Maisethanol 26 ct/l, in der EU für Ethanol auf Zuckerrübenbasis 45 ct/l aufgewendet werden.[23]
Produktionsverfahren
Die Produktion von Alkohol erfordert ein mehrschrittiges Verfahren. Zuerst wird Stärke in Zucker gespalten, dann der Zucker vergoren und schließlich der Alkohol fraktioniert. Je nach Einstellung der Gärung und der Fraktionierung entstehen verschiedene Alkohole Ethanol, Methanol und Nebenprodukte, insbesondere Fuselöle (Begleitalkohole). Ethanol ist stark hygroskopisch und hat daher immer azeotrop Wasser gebunden.
Herstellung durch Gärung und Synthese
Ethanol entsteht unter anderem bei der Vergärung von zucker- oder stärkehaltigen Materialien durch Hefe oder Bakterien. Daher wird dieser Prozess kontrolliert mit einer Reihe von Nahrungsmitteln durchgeführt, wodurch zum Beispiel Wein (aus Weintrauben) oder Bier (aus Malz und Hopfen) entstehen. Bei einer Ethanolkonzentration nahe 15 Prozent beginnen Hefezellen und Bakterien abzusterben, weswegen durch Gärung keine höhere Konzentration erreicht werden kann.
Durch Destillation kann das Ethanol konzentriert werden. Auf diese Art gewonnene Getränke bezeichnet man als Spirituosen (z. B. Whisky, Cognac, Schnaps, Wodka oder Rum). Sie enthalten noch Aromen der verdampften Ausgangslösung, die zumeist ein Wein war. Liköre sind Spirituosen, die mit zuckerhaltigen, aromatischen Flüssigkeiten gemischt werden und daher eine niedrigere Ethanolkonzentration besitzen. Branntwein darf nur beschränkt privat hergestellt werden (max. 0,5 l Maische), es sei denn der Branntwein wird versteuert. Durch intensivere Destillation kann man nahezu wasserfreies Ethanol für technische Anwendungen gewinnen (Azeotrop).
Destillation
Ethanol ist in jedem beliebigen Verhältnis mit Wasser mischbar. In der chemischen Synthese kann die Anwesenheit von Feuchtigkeit jedoch gravierende Nachteile haben. Großtechnisch erfolgt daher die Herstellung reinen Ethanols durch azeotrope Rektifikation. Die Anlage besteht hauptsächlich aus zwei Rektifikationskolonnen. In der Haupttrennsäule erfolgt die normale Rektifikation des Ethanol-Wasser-Gemischs bis in die Nähe des azeotropen Punkts. Das Sumpfprodukt ist Wasser.
Dem Kopfprodukt (95,6 % Ethanol und 4,4 % Wasser) wird der Hilfsstoff Cyclohexan beigemischt. Dieses Dreistoffgemisch gelangt in die Hilfsstoff-Trennsäule. Dort erfolgt eine Auftrennung in den im Sumpf anfallenden reinen Alkohol sowie in ein Cyclohexan-Wasser-Gemisch als Kopfprodukt. Cyclohexan und Wasser sind im flüssigen Zustand nicht mischbar und trennen sich nach der Kondensation in einem Abscheider (Dekanter). Der Hilfsstoff Cyclohexan wird am Einlauf der Hilfsstoff-Trennsäule wieder dem zuströmenden, azeotropen Ethanol-Wasser-Gemisch beigefügt. Er läuft im Kreislauf im oberen Bereich der Hilfsstoff-Trennsäule und wird deshalb auch als „kopflaufender Hilfsstoff“ bezeichnet.
Bei Temperaturen um −20 °C (Gefrierschrank) verdunstet Ethanol (96 %) kaum noch und zeigt eher zähflüssige Eigenschaften. Bei −70 °C wird es noch zähflüssiger (Kühlol).
Verwendung außerhalb der Genuss- und Nahrungsmittelindustrie
Die Hauptmenge des produzierten Ethanols wird in Form von alkoholischen Getränken für Genusszwecke verbraucht[1]. Es dient weiterhin als Lösungsmittel sowohl für Konsumprodukte unter anderem im Haushalt (Parfüm, Deodorant), als auch für medizinische Anwendungen (Lösungsmittel für Medikamente, Desinfektionsmittel) sowie in der Industrie selbst ebenfalls als Lösungsmittel und allgemein als Brennstoff. Für technische Anwendungen wie Kraftstoff, Lösungsmittel oder Brennspiritus werden Ethanol Vergällungsmittel beigemischt, wodurch diese ungenießbar werden und in Deutschland nicht mehr der Branntweinsteuer unterliegen.
 Lichtspektrum einer blau leuchtenden Spiritusflamme
Lichtspektrum einer blau leuchtenden Spiritusflamme
Haushalts- und Konsumprodukte
Ethanol findet u. a. als hervorragendes Lösungsmittel überall im Haushalt Verwendung, so als
- Träger für Geruchsstoffe (Parfüm, Deodorant, Duftspray)
- Reinigungsmittel (beispielsweise Glas, Chrom, Kunststoff, Scheibenwaschanlage, Fleckenentferner)
- Frostschutzmittel
- Lebensmittelzusatz (Portweinen und anderen Südweinen wird Ethanol zugegeben (Aufspritung), um zum gewünschten Zeitpunkt den Fermentationsprozess zu beenden;[24] auch kann Ethanol zur Haltbarmachung anderer Lebensmittel zugesetzt werden[25])
- Brennstoff (Campingkocher)
Medizin
- Die Wirksamkeit als Desinfektionsmittel oder Antiseptikum (etwa zur Händedesinfektion) hängt von der Konzentration des Ethanol-Wasser-Gemisches ab. Bei einem optimalen Alkoholgehalt zwischen 50 und 80 %[26] wird die Bakterienhülle zerstört und Ethanol wirkt damit tödlich. Alle Bakterien einschließlich der Tuberkelbakterien werden innerhalb einer Minute durch Denaturierung der Bakterienzellwand abgetötet (Bakterizidie). Daneben wirken Ethanol-Wasser-Mischungen auch durch ihren hohen Osmotischen Druck; 70-prozentiges Ethanol weist den höchsten osmotischen Druck von 250·106 Pascal der Mischungen mit Wasser auf.[11] Eingeschränkt wirksam ist er gegen Viren, nicht wirksam gegen Bakterien-Endosporen. Bei offenen Wunden sollte das Gemisch nicht eingesetzt werden (Brennen). Lösungen mit über 80 % Alkoholgehalt zeigen eine noch stärkere Wirkung, aber werden aufgrund der mangelnden Hautverträglichkeit nicht regelmäßig eingesetzt. Wasserfreies Ethanol härtet die Bakterienhülle, die Bakterien bleiben dadurch am Leben.[27] Das Trinken von Ethanol oder alkoholischen Getränken wirkt nicht antiseptisch. Getränke mit einem Ethanolgehalt von weniger als 20 % töten praktisch keine Keime ab. Durch Kombination mit Alkalien (etwa 1 %) oder Peroxycarbonsäuren (0,2 bis 0,5 %) wird die Wirksamkeit – auch gegen Viren und Sporen – stark verbessert.[26]
- 95-prozentiges Ethanol kann zur Verödung „heißer“ Schilddrüsenknoten und anderer umschriebener Tumore benutzt werden;[28] das Verfahren wird als Perkutane Ethanol-Injektionstherapie bezeichnet.[29]
- Flüssige Medikamente können Ethanol als Lösungsmittel oder Lösungsvermittler enthalten, wenn der Arzneistoff bzw. die die Arzneistoffe in Wasser schlecht oder unlöslich sind. Ethanol selbst ist mit Wasser beliebig mischbar. Es hat eine wichtige Funktion in der Konservierung und Stabilisierung flüssiger pflanzlicher Medikamente (Phytotherapeutika). Die Medikamente sind entsprechend der Arzneimittel-Warnhinweisverordnung (AMWarnV) zu kennzeichnen.
- Durch Einreiben der Haut mit hochprozentiger Ethanollösung (beispielsweise Franzbranntwein) wird die Durchblutung gefördert.
- Volksmedizinisch werden verdünnte ethanolische Lösungen zur Behandlung von Insektenstichen verwendet. Ein alkoholgetränktes Tuch wird dazu einige Zeit auf den frischen Stich gelegt. Die Schmerzlinderung geschieht aufgrund der kühlenden Wirkung der Ethanollösung; der Juckreiz wird unterdrückt. Eine chemische Veränderung oder Inaktivierung von Giften bewirkt Ethanol jedoch nicht.
- Bei einer Vergiftung mit Methanol wird als erste Maßnahme Ethanol intravenös gegeben, was die Umwandlung von Methanol über das Enzym Alkoholdehydrogenase in das giftige Methanal hemmt. Ethanol bindet etwa 25-mal stärker an Alkoholdehydrogenase als Methanol.[30]
- Bei einer schweren Alkoholsucht kann ein Alkoholprädelir mit Ethanol unterbrochen werden, um eine akute Zweiterkrankung ohne die sonst auftretenden Symptome behandeln zu können.
Ethanol als Kraftstoff
Ethanol findet als Ethanol-Kraftstoff in Form des biogenen Bioethanol Verwendung als Kraftstoff für Otto-Motoren, wobei vor allem Mischungen mit Benzin vorliegen. Dafür kann sowohl fossiles als auch aus regenerativer Biomasse hergestelltes Bioethanol verwendet werden, da es chemisch gesehen keinen Unterschied zwischen beiden Arten gibt. Aufgrund der Verfügbarkeit, der Herstellungskosten und politischer Fördermaßnahmen wird heute vor allem Bioethanol verwendet, das auf der Basis von fermentierbarem Zucker (Zuckerrohr und Zuckerrübe) und Stärke (vor allem Mais- und Weizenstärke) erzeugt wird. Die zukünftig mögliche Nutzung von Cellulose-Ethanol aus Holz wird diskutiert.
Ethanol wird vor allem als Beimischung zu herkömmlichem Kraftstoff genutzt, beispielsweise in einer Konzentration von 5 % Ethanol (E5 als Beimischung in gewöhnlichem Fahrzeugbenzin) oder 85 % Ethanol (als E85 für dafür geeignete Fahrzeuge). Im Zusammenhang mit dem Kyoto-Protokoll wird heute häufig über die Herstellung und den Einsatz biogener Treibstoffe (Biokraftstoffe) und die Reduzierung von Kohlenstoffdioxid-Emissionen pro gefahrenem Kilometer debattiert.
Ethanol wurde nach einer Entwicklung von Wernher von Braun zudem bis in die 1950er-Jahre als Treibstoff für die Raketen der Typen A1, A2, A3, A4, A4b und A5 verwendet. Im Unterschied zu Benzin kann durch Verdünnen mit Wasser für Testzwecke leicht der Heizwert heruntergesetzt werden, um bei Probeläufen von Triebwerken Explosionen zu verhindern, zum anderen war Ethanol während des Zweiten Weltkriegs leicht aus landwirtschaftlichen Produkten gewinnbar, im Gegensatz zum knappen Benzin.
Weitere Nutzung von Ethanol
Ethanol ist ein wichtiges Lösungsmittel und Zwischenprodukt in der Chemischen Industrie.
Besteuerung und Vergällung
Grundsätzlich unterliegt Ethanol in Deutschland der Branntweinsteuer. Diese beträgt derzeit 13,03 €/Liter reinem Alkohol und wird in Deutschland von der Zollverwaltung beim Inverkehrbringer (Spirituosenhersteller, berechtigter Empfänger, Branntweinlagerinhaber) zum Zeitpunkt des Lagerabganges erhoben. Ein Versand unter Steueraussetzung ist per BVD oder EVD möglich – beispielsweise zwischen Hersteller und Großhändler mit offenem Branntweinlager sowie bei Exportgeschäften.
Die Verwendung von Ethanol ist für technische Zwecke (Druckerei, Lackherstellung, Reinigungsmittelproduktion, Kosmetik und ähnliche) und als Brennspiritus steuerfrei möglich. Um zu verhindern, dass dieses Ethanol ohne Entrichtung der Steuer als Genussmittel getrunken oder solchen beigefügt wird, wird unversteuerter Alkohol unter Zollaufsicht vergällt. Vergällung bedeutet, dass Ethanol mit anderen Chemikalien, wie beispielsweise MEK (Methylethylketon = 2-Butanon, mit zwei weiteren branntweinsteuerrechtlich vorgeschriebenen Markierungskomponenten), Petrolether, Cyclohexan, Diethylphthalat oder ähnlichem versetzt wird, um es für den menschlichen Genuss unbrauchbar zu machen.
Bioethanol für die Beimischung zu Kraftstoff wird produktionsseitig mit ETBE oder Benzin vergällt. Gängige Vergällungsmittel wie sie etwa bei Spiritus oder Alkohol für kosmetische Zwecke beigemischt werden, beispielsweise MEK (Methylethylketon), dürfen in Kraftstoffen nach EN 228 nicht verwendet werden.
Bei dem in Form von Brennspiritus als Brennstoff verwendeten Ethanol, beispielsweise für Rechauds sowie Camping- und Expeditionskocher, wird dem Ethanol zusätzlich zum MEK noch das extrem bittere Denatoniumbenzoat (1 Gramm/100 Liter) beigemischt. Die früher übliche Verwendung von Pyridin als Vergällungsmittel für Brennspiritus ist branntweinsteuerrechtlich zwar immer noch erlaubt, dieses wird aber wegen seiner gesundheitlichen Bedenklichkeit seit ca. 1993 von deutschen Herstellern nicht mehr eingesetzt. Im Gegensatz zu Pyridin, das einen Siedepunkt von 115 °C aufweist, ist Denatoniumbenzoat ein Feststoff, der erst bei 163 bis 170 °C schmilzt. Es verdampft daher bei der Verwendung von Brennspiritus nicht, sondern reichert sich in den Dochten von Spiritusgeräten an, was zum Beispiel bei Spiritusglühlichtern und Spiritus-Vergaserkochern zu Betriebsstörungen führt.
Zu beobachten ist zudem, dass einige Spiritusabfüller, vermutlich aus Kostengründen, dem Ethanol diverse Fremdstoffe, Regenerate etc. beimischen. Abfüller, die in ihrem Produkt nur Ethanol verwenden, werden dies zumeist durch die Kennzeichnung „UN 1170“ auf der Flasche deutlich machen.
Die Vergällungsmittel haben meist ähnliche Siedepunkte wie Ethanol, so dass sie sich durch Destillieren nur schwierig entfernen lassen. Die Vergällungsmittel Diethylphthalat (Verwendung auch als Weichmacher) und MEK stellen ein Problem bei der Verwendung als Reinigungsmittel dar: Farben und Lacke, die an sich resistent gegen Ethanol sind, können erweichen oder angegriffen werden.
Brennspiritus ist nicht zu verwechseln mit sogenanntem Trockenspiritus, leicht entzündlichen weißen Würfeln, die meistens aus Urotropin (Hexamethylentetramin) oder dem Tetramer des Alkanals Ethanal, Metaldehyd, bestehen. Ein bekanntes Produkt ist der Trockenbrennstoff Esbit.
Physikalische und chemische Eigenschaften
Flammpunkt 12 °C[1] Zündtemperatur 425 °C[1] Explosionsgrenzen untere: 3,4 Vol.-%/obere: 15 Vol.-%[1] Schallgeschwindigkeit 1180 m·s−1 (20 °C)
Temp.-Abhängigkeit: −3,6 m·s−1·°C−1Dichte 0,79 g·cm−3 = 0,79 kg·dm−3 Energiedichte bzgl. der Masse 7,44 kWh·kg−1 = 26,78 MJ·kg−1[31] Energiedichte bzgl. des Volumens 5,87 kWh·l−1 = 21,14 MJ·l−1[31] dynamische Viskosität 1,2 · 10−3 Pa·s (20 °C) kinematische Viskosität 1,52 · 10−6 m2·s−1 (20 °C) Oberflächenspannung 0,02255 N·m−1 (20 °C) Brechungsindex 1,3638[1] Biologische Abbaubarkeit 94 % (OECD 301 E) UN-Nummer 1170 Gefahrennummer 30 + 33 Herausragendes Merkmal des Ethanols ist seine Hydroxygruppe. Da ein Sauerstoffatom Elektronen stärker anzieht als Wasserstoff und Kohlenstoff, resultiert eine asymmetrische Verteilung der Elektronendichte entlang dieser Bindung: Es bildet sich ein molekularer Dipol. Dieser verleiht Ethanol seine typischen Eigenschaften. Zum einen ziehen sich die Dipole auf molekularer Ebene gegenseitig an, so dass eine vergleichsweise hohe Siedetemperatur von 78 °C resultiert (Sp, Ethan = −88,6 °C), zum anderen ist Ethanol mit Flüssigkeiten mischbar, die ähnliche Dipoleigenschaften aufweisen (z. B. Wasser und Methanol), man spricht von Hydrophilie. Gleichzeitig besitzt das Molekül einen organischen Rest, der ihm eine begrenzte Mischbarkeit mit rein lipophilen Substanzen verleiht. Aus diesem Grund ist Ethanol in der Chemie ein wichtiges Lösungsmittel, so werden viele Pflanzenauszüge oder andere Medikamente als alkoholische Lösungen, sogenannte „Tinkturen“, angeboten.
Volumenkontraktion bei Mischung mit Wasser
Ethanol ist in jedem Verhältnis mit Wasser mischbar. Dabei kommt es in der Lösung durch eine Volumenkontraktion zu einer Abnahme des Gesamtvolumens, das theoretisch aus der Summe der Einzelvolumina entstehen müsste. Mischt man 50 ml Ethanol mit 50 ml Wasser erhält man nur 97 ml Ethanol-Wasser-Gemisch. Der Schmelzpunkt wässriger Ethanollösungen sinkt mit steigendem Ethanolgehalt, bis bei einem Gehalt von 93,5 Ma% ein Eutektikum mit einer Schmelztemperatur von −118 °C erreicht wird.[32]
-
Excess Volumina (Volumenkontraktion) bei der Mischung von Ethanol und Wasser
Säure-Base-Aktivität
Die OH-Gruppe des Ethanols ist mit einem pKs-Wert von 16[3] sehr schwach sauer, wodurch sie in der Lage ist, mit starken Basen (wie etwa den Alkalimetallen Natrium und Kalium) ein Proton (H+) abzuspalten. In der Chemie überführt man den Alkohol durch Umsetzen mit Alkalimetallen quantitativ in seine deprotonierte Form, das Ethanolat-Ion (CH3CH2O−). Die Reaktion verläuft unter Entwicklung von Wasserstoff:
Autoprotolyse
Ethanol kann sowohl als Brønsted-Säure als auch als Brønsted-Base reagieren und ist damit ein Ampholyt:
wobei die Autoprotolysekonstante pKau = 19,5 ist.
Nukleophile Substitution
In aprotischen Lösungsmitteln reagiert Ethanol mit Halogenwasserstoffen über eine nukleophile Substitution zu Ethylhalogeniden:

- Ethanol und Chlorwasserstoff reagieren zu Ethylchlorid und Wasser.
Ethanol und Bromwasserstoff reagieren zu Ethylbromid und Wasser.
Ethylhalogenide können auch spezifischer durch Halogenierungsreagenzien wie Thionylchlorid oder Phosphortribromid gebildet werden.
Veresterung
Säurekatalysiert reagiert Ethanol mit Carbonsäuren zu Ethylestern:
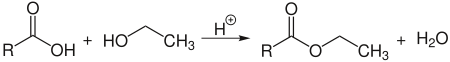
- Carbonsäuren reagieren mit Ethanol zu Ethylestern und Wasser.
Ethylester finden Verwendung als Zusätze für Kosmetika sowie Geruchs- und Geschmacksstoffe.
Dehydratation
Sehr starke Säuren, wie Schwefelsäure, katalysieren die Dehydratation des Ethanols. Es bilden sich Diethylether oder Ethen:

- Ethanol kondensiert unter Abspaltung von Wasser zu Diethylether.

- Ethanol spaltet in einer Eliminierungsreaktion Wasser unter Bildung einer Doppelbindung ab.
Welches Produkt sich bildet, hängt von den Reaktionsbedingungen wie Temperatur, Konzentrationen usw. ab. Bei der Dehydratation kann unter bestimmten Reaktionsbedingungen auch das hochgiftige Diethylsulfat gebildet werden.[33]
Oxidation
Ethanol kann bereits von Luftsauerstoff bei Raumtemperatur über Acetaldehyd bis hin zur Essigsäure oxidiert werden. Derartige Reaktionen werden beispielsweise in biologischen Systemen von Enzymen katalysiert. Im Labor dienen kräftige anorganische Oxidationsmittel wie Chromsäure oder Kaliumpermanganat zur Oxidation zu Essigsäure. Die teilweise Oxidation bis zum Acetaldehyd gelingt mit schwächeren Oxidationsmitteln, etwa mit Pyridiniumchlorochromat (PCC).
Verbrennung
Die Oxidation des Ethanols muss nicht auf der Stufe der Essigsäure stehenbleiben. Unter geeigneten Bedingungen, beispielsweise bei hohen Temperaturen, verbrennt Ethanol unter Flammenbildung bei vollständiger Oxidation mit einem Heizwert von etwa 30 MJ/kg zu Kohlendioxid und Wasser:
Physiologisches
Aufnahme und Abbau
Ethanol wird im gesamten Verdauungstrakt aufgenommen. Dies beginnt in geringem Umfang bereits in der Mundschleimhaut. Das dort resorbierte Ethanol geht direkt in das Blut über und wird damit über den gesamten Körper einschließlich des Gehirns verteilt. Etwa 20 % werden im Magen resorbiert; der Rest im Dünndarm.[34] Der in Magen und Darm aufgenommene Alkohol gelangt zunächst mit dem Blut in die Leber, wo er teilweise abgebaut wird. Die Ethanolaufnahme wird durch Faktoren, welche die Durchblutung steigern, erhöht, beispielsweise Wärme (Irish Coffee, Grog), Zucker (Likör) und Kohlenstoffdioxid (Sekt). Dagegen verlangsamt Fett die Aufnahme. Dies führt aber nicht zu einer niedrigeren Resorption des Alkohols insgesamt, sondern nur zu einer zeitlichen Streckung.[35]
Etwa 2–10 Prozent des aufgenommenen Ethanols werden unverändert über Urin, Schweiß und Atemluft wieder abgegeben.[36] Ein Teilabbau findet schon im Magen statt; eine dort gefundene sigma-Alkoholdehydrogenase zeigt eine etwa um den Faktor 200 höhere Aktivität als die in der Leber lokalisierten Isoenzyme. Der Anteil am gesamten Ethanolabbau beträgt aber lediglich ungefähr 5 %.[37]
In der Leber wird der Hauptteil des Alkohols – wie andere wasserlösliche Gifte – durch die Enzyme Alkoholdehydrogenase (ADH) und Katalase sowie das MEOS-System zu Ethanal (Acetaldehyd, H3C-CHO) abgebaut, um weiter durch Acetaldehyddehydrogenase zu Essigsäure oxidiert zu werden. Die Essigsäure wird über den Citratzyklus und die Atmungskette in allen Zellen des Körpers unter Energiegewinnung zu CO2 veratmet. Die Leber kann bei erheblich gesteigertem, regelmäßigem Konsum ihre Abbauaktivität in geringem Maße anpassen. Das Zwischenprodukt Ethanal ist auch für die so genannten „Kater“-Symptome wie Kopfschmerzen, Übelkeit und Erbrechen[38] mitverantwortlich. Der Abbau des Ethanals wird durch Zucker gehemmt, daher ist der Kater bei süßen alkoholischen Getränken, insbesondere Likör, Bowlen und manchen Sektsorten besonders intensiv.
Die Abbaurate durch die Alkoholdehydrogenase ist innerhalb gewisser Grenzen konstant. Sie beträgt bei Männern etwa 0,1 g pro Stunde und kg Körpergewicht, bei Frauen 0,085 g/h und kg/KG.[39][40] Die exakt gemessenen Abbauraten für Männer lagen dabei zwischen 0,088 und 0,146 g/h und kg Körpergewicht.[37] Eine 0,5-l-Flasche Bier mit 16 g Ethanol wird danach in ein bis zwei Stunden abgebaut. Bei Männern findet sich eine leicht erhöhte Aktivität der gastrischen Alkoholdehydrogenase im Magen, mit der Folge einer geringfügigen Beschleunigung des Alkoholabbaus. Hochdosierte Aufnahme von Fructose kann bei manchen Menschen durch Unterstützung des Katalase-Ethanolabbaus zu einer schnelleren Metabolisierung führen.[38] Bei höherer Alkoholkonzentration – ab etwa 50 g Ethanolaufnahme pro Tag[37] – oder bei chronischen Trinkern wird der Alkohol zusätzlich über das mikrosomale Ethanol oxidierende System (MEOS) abgebaut. Dabei wird Ethanol in den Mikrosomen der Leberzellen durch Cytochrom P450 (CYP2E1) unter Sauerstoffverbrauch ebenfalls zu Ethanal oxidiert. Dieser Effekt, gepaart mit einer Desensibilisierung des vegetativen Nervensystems, führt zu einer höheren Alkoholresistenz bei „trainierten Trinkern“ und „Spiegeltrinkern“. Diese Desensibilisierung durch Gewöhnung kann so weit gehen, dass Trinker mit zwei und mehr Promille keinerlei Verhaltensauffälligkeiten zeigen.
Andere Alkohole aus unsauber destillierten Spirituosen, die so genannten Fuselöle, werden ebenfalls durch die Alkoholdehydrogenase bzw. Acetaldehyddehydrogenase abgebaut. Dieser Abbau tritt damit zum Abbau des Ethanols in Konkurrenz, welcher deshalb langsamer abgebaut wird.
Genetische Unterschiede bei der Verträglichkeit von Alkohol
Die Ursache dafür liegt in den genetisch determinierten Abbausystemen von Ethanol und Ethanal; der Abbau geschieht im menschlichen Körper vorwiegend durch die Alkoholdehydrogenasen ADH-1, ADH-2 und ADH-3 sowie die Aldehyddehydrogenasen ALDH-1 und ALDH-2. Ist die Funktion eines oder mehrerer dieser Enzyme eingeschränkt oder fehlt völlig, so ist der Ethanolabbau im Körper nur vermindert möglich. Tritt das Defektallel ALDH-2x2 homozygot (reinerbig) auf, wird eine inaktive Form der Aldehyddehydrogenase 2 hergestellt. Träger dieses Defekts reagieren auf Ethanol mit starker Gesichtsrötung und Übelkeit, sowie deutlicher Alkoholaversion.[41] Reinerbige Träger kommen in Europa nahezu nicht vor, während in China 16 % und Japan 22 % der Bevölkerung betroffen sind. Bei Menschen mit diesem Gendefekt entwickelt sich so gut wie nie eine Alkoholabhängigkeit,[42][41] Mischerbigkeit (Heterozygotie) des Gens bewirkt eine vollständige Funktion des ALDH-2-Enzyms und damit eine normale Abbaurate. Die geringere Abbaurate führt aufgrund einer höheren Konzentration an giftigem Ethanal (Acetaldehyd) zum so genannten Kater mit dem Hauptsymptom Übelkeit.
Blut- und Atemalkohol
Ein objektives Maß für die alkoholische Beeinflussung stellt die Alkoholkonzentration im venösen Blutkreislauf und in der Atemluft dar, wobei nur begrenzte Aussagen über die physiologische Beeinträchtigung möglich sind, da diese stark von individuellen Einflüssen, insbesondere der Alkoholgewöhnung, abhängen.
Die Höhe der Blutalkoholkonzentration (BAK) bzw. der Atemalkoholkonzentration (AAK) ist mit einer statistischen Wahrscheinlichkeit mit dem Risiko von Ausfallerscheinungen oder Unfällen gegenüber dem nüchternen Zustand verbunden, welche die Grundlage der gesetzlichen Promillegrenzen darstellen.
Eine näherungsweise Auflistung der Blutalkoholkonzentration nach der Aufnahme verschiedener ethanolhaltiger Getränke und der entsprechenden Auswirkungen auf den Menschen liefert folgende Tabelle:
Blutalkoholkonzentration (BAK) nach der Aufnahme verschiedener ethanolhaltiger Getränke[43] Menge alkoholhaltiger Getränke Blutalkoholspiegel Wirkungen 1 Glas Bier (0,33 l) oder
0,2 l Weinab 0,3 ‰ enthemmende Wirkung mit Steigerung der Redseligkeit 2–3 Gläser Bier oder
0,5 l Wein0,5–1 ‰ „Schwips“ mit Enthemmung, Selbstüberschätzung, Nachlassen der Reaktionsfähigkeit 5–9 Gläser Bier oder
1–1,5 l Wein1–2 ‰ deutliche Angetrunkenheit, beginnende Ataxie (Störungen der Bewegungskoordination), verminderte Sehleistung, teils Aggressivität, Uneinsichtigkeit 11–16 Gläser Bier oder
2–3 l Wein2–3 ‰ Trunkenheit, Rausch, starke Ataxie, Denk- und Orientierungsstörungen, später teils Amnesie ab 3 ‰ schwerer Rausch, Benommenheit bis zur Bewusstlosigkeit, Verschlucken von Erbrochenem und Unterkühlung, Tod durch Atemlähmung bei Menschen, die nicht an regelmäßig größere Alkoholmengen gewöhnt sind 6–8 ‰ i. d. R. (auch für schwere Alkoholiker) tödlich Diese Angaben sind Durchschnittswerte und können sehr stark variieren.[43] Die erreichbare BAK ist von der aufgenommenen Getränkemenge, der Körpermasse und dem Geschlecht abhängig, aber auch von Faktoren wie Statur und Alter sowie Füllzustand des Magens. Zur Berechnung der (theoretisch) maximal erreichbaren BAK dienen die Widmarkformel (nach Widmark) oder die Methode nach Watson.[44] Als Maßeinheit dient das Massenverhältnis Milligramm Alkohol pro Gramm Blut (mg/g), besser bekannt als Promillewert. Die Berechnung der Blutalkoholkonzentration nach Watson erfolgt bei Männern mit folgender Formel:
- BAK = 0,8/(2,447 − 0,09516 × Alter in Jahren + 0,1074 × Größe in cm + 0,3362 × Masse in kg) × Alkohol in g
Die Atemalkoholkonzentration (AAK) kommt dadurch zustande, dass in den Lungenbläschen (Alveolen) ein Übergang des Alkohols aus dem arteriellen Blutkreislauf in die eingeatmete Luft erfolgt, womit beim Ausatmen Alkohol abgegeben wird. Als Maßeinheit dient die Alkoholmenge in Milligramm pro Liter Atemluft (mg/l). Eine direkte Umrechnung von AAK in BAK ist nicht exakt möglich, da sich das Verhältnis zeitlich verändert. Daher existieren in der Bundesrepublik Deutschland zwei separate Grenzwerte, die juristisch gleichgesetzt sind und auf dem mittleren Verteilungsfaktor von 1:2000 beruhen. Damit entsprechen 0,5 mg/g BAK 0,25 mg/l AAK. Umfangreiche grundlegende Forschungen zur Messung der Atemalkoholkonzentration wurden 1981 im damaligen Institut für Sozialmedizin und Epidemiologie des Bundesgesundheitsamtes durchgeführt.[45]
Unmittelbare physiologische Wirkung
Alkohol bewirkt situativ eine Betäubung, eine Stimulation oder auch einen Stimmungswandel.
Er führt auch zu einer Erweiterung insbesondere der peripheren Blutgefäße. Daraus ergibt sich ein Wärmegefühl beim Konsum alkoholhaltiger Getränke. Dabei wird die natürliche Regulierung des Wärmehaushalts bei niedrigen Temperaturen außer Kraft gesetzt. Zugleich wirkt Alkohol betäubend, so dass bedrohliche Kälte nicht mehr wahrgenommen wird. Daher können Erfrierungen bis hin zum Kältetod die Folge winterlichen Alkoholkonsums sein.
Problematisch ist auch die Kombination von Alkohol mit Medikamenten und anderen Drogen. Hier gibt es vielfältige Wechselwirkungen, die zu einer vorzeitigen und intensiveren Beeinträchtigung als bei reinem Alkoholkonsum führen können. Das beim Alkoholabbau gebildete Cytochrom P450 2E1 kann die Wirksamkeit von Medikamenten durch deren Abbau beeinträchtigen. Viele der „Drogentoten“ (insbesondere der Heroinopfer) starben an einem Mischkonsum mit Alkohol.
Toxikologie
Ethanol ist weder als giftig noch als gesundheitsschädlich eingestuft, wird aber von Pathologen zu den „obligat hepatotoxischen Stoffen“[46], also zu den Lebergiften, gezählt; es gilt auch ein „direkter toxischer Effekt des Alkohols auf die Erythropoiese“, die Bildung roter Blutzellen, als gesichert[47]; Pädiater nennen ihn eine „teratogene Noxe“[48], also ein die Leibesfrucht schädigendes Gift und auch die Pharmakologen/Toxikologen sprechen von „akuter Vergiftung“ ab einer bestimmten Schwellendosis sowie von einer „chronischen Vergiftung“ beim Alkoholismus[49]. So zeigen verdünnte Lösungen von Ethanol in Wasser schon bei Konzentrationen von wenigen Volumenprozenten physiologische Effekte. Die Aufnahme führt – ab etwa 0,5–1 Promille Alkoholkonzentration im Blut – zu typischen akuten Trunkenheitssymptomen wie Schwindel, Übelkeit, Orientierungsstörung, Redseligkeit und gesteigerter Aggressivität. Die Letale Dosis (LD) liegt etwa bei 3,0 bis 4,0 Promille für ungeübte Trinker. Es wurden jedoch schon Werte über 7 Promille gemessen.[50] Die LD50 beträgt für die Ratte 7.060 mg/kg bei oraler Applikation.[51] Bei einer akuten Ethanolvergiftung kann der noch im Magen befindliche Alkohol durch Herbeiführen von Erbrechen oder durch Auspumpen des Mageninhalts teilweise entfernt werden.
Bei regelmäßiger Einnahme, die zu einer Abhängigkeit (Alkoholkrankheit) führen kann, werden alle Zellen des Körpers geschädigt. Insbesondere leiden das Nervensystem und Gehirn sowie die Leber. Der Vitamin B1-Stoffwechsel wird durch langanhaltenden Alkoholkonsum geschädigt, diese Schädigung kann eine Polyneuritis auslösen. Epilepsie, Psychosen, soziale Vereinsamung und der verfrühte Tod können die Folge sein. Die Wernicke-Enzephalopathie findet sich bei etwa 15 % der verstorbenen Alkoholiker, und bildet zusammen mit dem Korsakow-Syndrom das Wernicke-Korsakow-Syndrom. Bekannt ist auch die Schädigung des Zentralnervensystems beim Delirium tremens. Diese Nervenerscheinung tritt beim Alkoholentzug des Körpers auf. In Deutschland sterben über 73.000 Menschen jährlich vorzeitig aufgrund von Alkoholmissbrauch.[52]
Wirkungen auf Nervensystem und Gehirn
Die akuten Wirkungen des Ethanols beruhen auf einer Schädigung von allen Körper- und vorwiegend Nervenzellen sowie auf einen Einfluss auf den Hirnstoffwechsel.[53] Die Beeinflussung beruht mit hoher Wahrscheinlichkeit auf der Einlagerung von Ethanol in Membranproteine, wodurch deren Funktion gestört wird. Besonders empfindlich für Ethanol sind verschiedene Ionenkanäle.[34] Es stimuliert dabei die GABA-Rezeptoren in Gehirn und Nervensystem und hemmt die NMDA-Rezeptoren.[54] Dies führt generell zu einer Hemmung der Reizübertragung im zentralen Nervensystem, aber gleichzeitig zu Sensitivitätssteigerung[55] und nachfolgend dosisabhängig zur Enthemmung, Beeinflussung des Gleichgewichtssinns und Sehvermögens (verengtes Blickfeld, Tunnelblick), der Muskelkontrolle und bis zu aggressivem Verhalten. Größere Mengen wirken akut betäubend und können zu Erinnerungslücken führen.[56] Weiterhin kann Ethanol den programmierten Zelltod von Gehirnzellen über eine komplexe Wirkungskette triggern.[57] Dies beginnt bei der Wirkung auf GABA- und NMDA-Rezeptoren, welche über eine Auflösung der Mitochondrien-Membran die Freisetzung von Cytochrom c und die Aktivierung verschiedener Caspasen verursachen kann.[58] Diese Peptidasen bewirken dann unter Anderem die Zerstörung des Zellkerns bzw. der DNA und damit den Tod der Zelle.[54][59]
Abhängig von der aufgenommenen Menge und damit der Konzentration im Blut bewirkt Ethanol auch eine Erhöhung der Durchlässigkeit der Blut-Hirn-Schranke.[60] Bei chronischem Alkoholkonsum ist eine Schädigung der Blut-Hirn-Schranke nachgewiesen,[61][62][63] was als wesentlicher Faktor für die Entstehung verschiedener neurodegenerativer Erkrankungen gilt.[64] Dies ist durch neuropathologische Untersuchungen von Alkoholabhängigen und auch durch Tierversuche belegt.[65]
In einer Studie mit etwa 2800 Personen, die jeweils mindestens 55 Jahre alt waren, wurden zunächst zwischen 1987 und 1989 die Daten der Personen erfasst. Von 1993 bis 1995 wurden dann bei noch rund 1900 der Versuchspersonen über eine Kernspintomographie die Schädigungen des Gehirns ermittelt. Bei der Datenaufnahme waren die Probanden je nach Alkoholkonsum in fünf verschiedene Gruppen eingeteilt worden. Dabei zeigte sich, dass auch bei geringer Alkoholaufnahme das Hirngewebe in geringem Maße schrumpfte. Dagegen war kein Zusammenhang zwischen der Menge des konsumierten Alkohols und der Anzahl von Hirn- oder Herzinfarkten nachweisbar. Das Herzinfarktrisiko sank sogar bei mäßigem Alkoholgenuss.[66][67]
Starker Alkoholkonsum führt zu einem als Trunkenheit bezeichneten Zustand. Dieser ist durch körperliche Veränderungen wie etwa psychisch durch erhöhte Emotionalität, und durch eine veränderte Bewusstseinswahrnehmung und verringerte geistige Leistungsfähigkeit gekennzeichnet. Dabei zeigen neue Studien, dass es dabei zu einer Verringerung der Aktivität der Gehirnregion kommt, die für das Erkennen von Gefahren benötigt wird.[68] Meistens führt erheblicher Alkoholkonsum zu Übelkeit und Erbrechen. Dabei wird allerdings nur der Teil des Alkohols ausgeschieden, der noch nicht in die Blutbahn gelangt ist.
In noch größeren Mengen setzt eine akute Alkoholvergiftung ein, die bis zum Koma oder dem direkten Tod führen kann. Besonders gefährlich ist der schnelle Konsum von hochprozentigen Spirituosen, da die Übelkeitsschwelle langsamer eintritt als ein lebensbedrohlicher Anstieg des Blutalkoholspiegels. Beim schnellen Trinken einer ganzen Flasche Schnaps, diese enthält 150–200 ml Ethanol, kann durch Lähmung des Hirnstammzentrums ein tödlicher Kollaps eintreten. Ferner kann eine zusätzliche Vergiftung drohen, wenn das Genussmittel mit größeren Mengen an Nebenprodukten verunreinigt ist wie Fuselalkoholen oder Methanol, die bei der Spirituosen zugrundeliegenden Destillation angereichert werden können.
Mangelsymptome durch Ethanol
Regelmäßiger Alkoholkonsum kann zu Mangelerscheinungen verschiedener Vitamine, Körperelektrolyte und Spurenelemente führen. So waren bei Patienten mit alkoholischer Lebererkrankung die fettlöslichen Vitamine Retinol (Vitamin A), Cholecalciferol (Vitamin D) und Tocopherol (Vitamin E) in Leber, Blut und gesamtem Organismus deutlich reduziert.[38] Retinol wird dabei in Anwesenheit von Ethanol verstärkt metabolisiert, wobei teils Karzinogene entstehen.[69][70] Der Vitamin-D-Mangel zeigt sich in verstärktem Auftreten von Frakturen und Osteoporose bei Alkoholkranken. Bei den E-Vitaminen, die aus verschiedenen Isomeren des Tocopherols bestehen, induziert Ethanol eine Verschiebung des Anteils vom α- zum sehr viel schwächer wirksamen γ-Isomer und damit Mangelsymptome. Auch alle wasserlöslichen Vitamine treten bei Alkoholismus vermindert auf, wobei vorwiegend Thiamin (Vitamin B1), Pyridoxin (Vitamin B6) und Folsäure betroffen sind. Alkoholaufnahme vermindert die Resorption von Vitamin B1 im Dünndarm und stört auch die Aktivierung des Thiamins durch Hemmung seiner Phosphorylierung. Dies kann – insbesondere bei gleichzeitiger Aufnahme von Diuretika – zu einem Herzversagen führen.[38] Ethanol blockiert die Bildung von Pyridoxal-5-Phosphat aus Vitamin B6, das im Organismus auch durch das aus Alkohol entstehende Ethanal zerstört wird. Folsäure wird ebenfalls vermindert resorbiert; ein Mangel bewirkt wiederum eine niedrigere Aufnahme von Thiamin im Darm. Der Folsäuremangel führt zu den stärksten akuten Symptomen bei Alkoholkranken wie Blutbildungsstörungen (makrozytäre Anämie), neurologischen Störungen (Vergesslichkeit und Schlafstörungen) sowie Fötusmissbildungen bei Schwangeren. Starker Alkoholkonsum kann ebenfalls einen Mangel wichtiger Elektrolyte und Spurenelemente, vorwiegend von Zink, Magnesium und Selen verursachen. Zinkmangel bedingt dabei eine Verstärkung der Giftigkeit des Ethanols, da das Enzym Alkoholdehydrogenase, welches Ethanol im Körper abbaut, abhängig von Zink ist.
Alkohol in der Schwangerschaft
Alkoholkonsum der Mutter während der Schwangerschaft kann zum sogenannten fetalen Alkoholsyndrom (FAS) führen. Dieses ist häufig durch eine Beeinträchtigung der geistigen Entwicklung des Kindes sowie körperliche Fehlbildungen (z. B. Herzfehler) gekennzeichnet. Jedes Jahr werden 10.000 alkoholgeschädigte Kinder in Deutschland geboren, davon 4.000 Kinder mit dem Vollbild des fetalen Alkoholsyndroms. Schädigungen bei Kindern alkoholabhängiger Mütter gehören damit zu den häufigsten der pränatal bedingten Gesundheitsschäden und sind häufiger als das Down-Syndrom. Generell ist in der Schwangerschaft jeglicher Alkoholkonsum zu vermeiden. Schon kleine Mengen können für das Kind fatale Folgen haben. Einer Studie der Berliner Charité zufolge konsumieren 58 Prozent aller Schwangeren gelegentlich alkoholische Getränke. Alkoholkonsum in der Schwangerschaft ist in Deutschland derzeit nicht strafbar (vgl. Kindesmisshandlung). [71][72][73]
Todesursache Alkoholmissbrauch
Alkohol kann eine sehr starke und körperliche und/oder psychische Abhängigkeit erzeugen, die körperliche Abhängigkeit ist verbunden mit heftigen Entzugserscheinungen. Bis zu 2 Millionen Menschen sind allein in Deutschland alkoholkrank, ca. 10 Millionen von Abhängigkeit bedroht.
In Deutschland starben im Jahr 2005 nach Angaben des Statistischen Bundesamts mehr als 16.000 Menschen durch Alkoholmissbrauch. Dies entspricht 2% aller Sterbefälle.[74]
Eine internationale Studie der WHO aus dem Jahr 2011 weist für 2004 sogar ein weltweite Sterbequote durch Alkoholmissbrauch von 3,1 % aus (6,6 % bei Männern und 1,1 % bei Frauen).[75]
Das Sterberisiko steigt innerhalb von 20 Jahren um 56 %, wenn man sich wenig bewegt, um 52 % durch Rauchen, um 31 % durch schlechte Ernährung und um 26 % durch viel Alkohol.[76]
Die häufigste alkoholbedingte Todesursache war die alkoholische Leberzirrhose mit 9.550 Toten.[77] Eine Krankheit, mit einer Mortalität (Todesrate) von über 50 Prozent, die insbesondere in Verbindung mit Alkohol und fettem Essen ausgelöst wird, ist die Pankreatitis (Bauchspeicheldrüsenentzündung).
Die damalige Drogenbeauftragte der Bundesregierung und Staatssekretärin im Bundesgesundheitsministerium, Marion Caspers-Merk, sprach für 2003 von 40.000 Todesfällen als Folge des Alkoholkonsums in Deutschland, wobei, im Vergleich, 1.477 Personen durch illegale Drogen verstorben sind und 110.000 als Folge des Tabakrauchens.[78]
Hilfe bieten Ärzte oder Selbsthilfegruppen wie die Anonymen Alkoholiker oder die Guttempler, ebenso Suchtberatungsstellen sowie verschiedene andere Selbsthilfegruppen.
Krebsrisiko
Übermäßiger Konsum von Alkohol kann neben teils unheilbaren Erkrankungen wie Leberzirrhose und Nervenerkrankungen auch viele Krebsarten (wie Magenkrebs und Speiseröhrenkrebs) erzeugen.
Die Internationale Agentur für Krebsforschung (IARC, „International Agency for Research on Cancer“) hat im Februar 2007 durch eine internationale Arbeitsgruppe eine Neubewertung der Folgen des Konsums alkoholischer Getränke vorgenommen und aus folgenden Gründen pauschal „Ethanol in alkoholischen Getränken“ als karzinogen für den Menschen (Gruppe 1) eingestuft: Das Vorkommen von malignen Tumoren von Mundhöhle, Rachenhöhle, Kehlkopf, Speiseröhre, Leber, weiblicher Brust und Colorectum steht in kausalem Zusammenhang mit dem Konsum alkoholischer Getränke, wie zahlreiche Studien zeigen. Gegenüber der früheren Bewertung im Jahre 1988 sah es die IARC-Arbeitsgruppe als gesichert an, dass Ethanol und nicht andere Bestandteile oder Kontaminanten für die Karzinogenität von alkoholischen Getränken verantwortlich ist. Das Krebsrisiko steigt generell mit der aufgenommenen Alkoholmenge. Ein Zusammenhang mit der Art des aufgenommenen Alkohols (Bier, Wein oder Spirituosen) konnte nicht hergestellt werden.[79]
Der World Cancer Research Fund und das American Institute for Cancer Research empfehlen, den täglichen Alkoholkonsum bei Frauen auf ein, bei Männern auf zwei Getränke zu begrenzen (10–15 g Ethanol pro Getränk; ca. 10 g sind in 30 ml Schnaps, 330 ml Bier oder 100 ml Wein enthalten). Die Bezugsgröße ist der Tag, da gelegentlicher Konsum (beispielsweise sieben Getränke am Wochenende und keines wochentags) gesundheitsschädlicher ist als ein gleichmäßiger verteilter Konsum derselben Menge (beispielsweise ein Getränk jeden Tag).[80]
Die karzinogene Wirkung entsteht durch das Ethanal, zu dem Ethanol in der Leber abgebaut wird. Das Ethanal wird durch Polyamine zu Crotonaldehyd umgewandelt, welches wiederum die DNA zerstört.[81]
Abhängigkeit
Verschiedene physiologische Auswirkungen des Ethanols – wie stimmungsaufhellende, stimulierende und angstlösende Effekte – können eine Abhängigkeit oder Alkoholsucht erzeugen. Diese Effekte beruhen vorwiegend auf der erhöhten Produktion von Dopamin und Endorphinen. Aber auch die starken Entzugssymptome begünstigen eine einmal vorhandene Abhängigkeit.[41]
Andere Auswirkungen und Schäden
Chronische Aufnahme von Alkohol steigert den Serumspiegel der toxischen Aminosäure Homocystein.[82][83] Dies wurde mit Alkohol-assoziierter Hirnatrophie,[84] mit Alkoholentzugsanfällen[85] und alkohol-assoziierten kognitiven Einbußen[86] in Verbindung gebracht.
Alkohol hat auch Auswirkungen auf Sexualität und Fruchtbarkeit. Ethanol erzeugt eine Erhöhung des Östrogenspiegels im Blut der Frau, was in Mengen ab 0,5–1 ‰ zu Fertilitätsstörungen führen kann. Beim Mann bewirkt dieselbe Menge Ethanol (zwei Gläser Wein oder eine Flasche Bier) eine Verringerung der Sperma-Menge und des Anteils von normalen Spermien um bis zu 34 %.[87] Dies wird durch die von Ethanol erzeugte Reduktion der Testosteronproduktion beim Mann begründet. Aufnahme größerer Mengen kann bis zur Hoden-Atrophie führen.[88] Alkoholkonsum führt zwar zu einer Enthemmung, speziell bei Männern auch zu einer Steigerung der Libido. Parallel dazu verringert sich ab ca. 0,4 ‰[89] die Erektionsfähigkeit bis hin zur völligen erektilen Dysfunktion.[43]
Mögliche positive gesundheitliche Wirkungen
Es ist unumstritten, dass die Wirkung alkoholischer Getränke eindeutig negativ ist, wenn sie in größeren Mengen und regelmäßig konsumiert werden. Beim Konsum geringerer Mengen Alkohol hingegen ist umstritten, ob die Wirkung eher positiv oder eher negativ ist. Viele vordergründig positive Wirkungen werden durch andere aufgehoben, etwa die leicht erhöhte Krebsgefahr beim regelmäßigen Konsum selbst geringer Mengen, die durch wissenschaftliche Studien bestätigt wurde, z. B. durch eine britische Studie aus dem Jahr 2006.[90] Mediziner warnen davor, einzelne Wirkungen aus dem Gesamtzusammenhang zu reißen. Die meisten positiven Wirkungen gehen nicht vom Alkohol selbst aus, sondern von anderen Pflanzenstoffen, die in Getränken wie Rotwein enthalten sind.
Aus einer Anzahl epidemiologischer Untersuchungen geht hervor, dass ein ausgesprochen mäßiger Konsum bestimmter alkoholhaltiger Getränke – insbesondere Rotwein – etwa ein bis zwei Gläser pro Tag über längere Zeiträume vor koronarer Herzerkrankung schützen soll. Außerdem wurde bei einem Alkohol-Konsum von 20–40 g bei Männern bzw. 10–20 g bei Frauen pro Tag eine höhere Lebenserwartung festgestellt. Dies entspricht etwa ¼ Liter Rotwein oder ½ Liter Bier. Die höhere Lebenserwartung ist allerdings nur ein statistischer Effekt, da unter den Antialkoholikern auch Personen sind, die gerade wegen einer Krankheit und damit verbundener niedriger Lebenserwartung keinen Alkohol trinken.[91][92]
Viele Studien wurden von der Alcohol Task Force der Stiftung International Life Sciences Institute finanziert, deren Mitglieder die Konzerne Moët & Chandon, Allied Domecq, Brasseries Kronenbourg, Heineken und Diageo sind. In Deutschland wurden viele Studien von der Deutschen Weinakademie (DWA) in Auftrag gegeben, die von den Weinerzeugern finanziert wird. Alleine für die Pressearbeit im Inland wurden 160.000 Euro ausgegeben. Die französische Sopexa gab 800.000 Euro für deutsche Medien aus.
Eine neue Metaanalyse von 54 internationalen Studien, die sich mit Alkohol und Herzschutz befassten – die älteste war von 1974, die jüngste von 2004 – wirft prinzipielle Zweifel an den immer wieder postulierten positiven gesundheitlichen Wirkungen von moderatem Alkoholkonsum auf.[93] Die Quintessenz dieser nun in Frage gestellten Untersuchungen lautet, dass mäßiger Alkoholkonsum langfristig die Rate von Herzinfarkten und Schlaganfällen senke. Trägt man die Sterblichkeit (Y-Achse) gegen den Alkoholkonsum (X-Achse) graphisch auf, ergibt sich gemäß der Interpretation dieser Studienergebnisse eine J-Kurve (so genannt, weil sie einem liegenden „J“ ähnelt), nach der die kardiovaskuläre und allgemeine Sterblichkeit bei einem leichten Alkoholkonsum am niedrigsten sei, dann aber rasch und sprunghaft ansteige. Menschen, die wenig Alkohol trinken, lebten demnach länger als abstinente Personen oder Vieltrinker.
Die 2006 veröffentlichte Metaanalyse kommt dagegen zu dem Schluss, dass 47 der 54 untersuchten Studien einen gravierenden Fehler aufweisen, infolgedessen die genannten Schlussfolgerungen an Glaubwürdigkeit verlören. So wurden in den meisten Studien ehemalige Alkoholkonsumenten – mit all ihren durch den bisherigen Alkoholkonsum kumulierten gesundheitlichen Problemen – der Gruppe der Abstinenzler zugerechnet. Diese „späten“ Abstinenzler, die das Trinken erst im fortgeschrittenen Alter aufgrund von – teils durch Alkoholkonsum verursachten – chronischen Krankheiten aufgegeben haben bzw. aufgeben mussten, werden mit den „echten“ Abstinenzlern, also denjenigen Personen, die schon viele Jahre lang Alkohol meiden oder nie welchen getrunken haben, in eine Gruppe zusammengefasst. Dieses Vorgehen setzt jedoch den durchschnittlichen Gesundheitszustand der Personen der Gruppe der „Abstinenzler“ generell herab – gemäß den Autoren der Metastudie ein erheblicher methodischer Fehler. Hierdurch entsteht der – falsche – Eindruck, in der Gruppe der (echten) Anti-Alkoholiker gäbe es eine höhere Zahl von Todesfällen als bei den moderaten Trinkern, so dass letztere wiederum als besonders gesund und langlebig erscheinen. Berücksichtigt man jedoch den „Abstinenzler-Fehler“, verringern sich die postulierten positiven Effekte von moderatem Alkoholgenuss bzw. sind diese gar nicht mehr vorhanden. Graphisch betrachtet ergibt sich bei zunehmendem Alkoholkonsum demnach gar keine (ausgeprägte) J-Kurve, sondern vielmehr ein stetiges Ansteigen der durch Alkohol verursachten Todes- und Krankheitsfälle.
Kaye Fillmore von der University of California in San Francisco, eine Autorin der Metaanalyse, weist darüber hinaus darauf hin, dass bei der Bewertung der gesundheitlichen Wirkung von moderatem Alkoholgenuss häufig der typische Fehler gemacht würde, Ursache und Wirkung zu verwechseln: „Wir wissen, dass ältere Menschen, die mäßig Alkohol trinken, gesünder sind als gleichaltrige Nichttrinker“, so Fillmore. „Das Trinken ist eine Folge ihres guten Allgemeinbefindens, nicht aber dessen Ursache. Viele Menschen meiden Alkohol im Alter aufgrund gesundheitlicher Probleme.“ Demzufolge sind diese Personen also nicht krank, weil sie nicht (moderat) trinken, sondern sie trinken nicht, weil sie krank sind.
Die Autoren der Metastudie kommen zu dem Schluss, dass die schützende, lebensverlängernde Wirkung von Alkohol aufgrund des beschriebenen „Abstinenzler-Fehlers“ in der Vergangenheit deutlich überbewertet wurde, wollen allerdings positive gesundheitliche Effekte von moderatem Trinken nicht prinzipiell ausschließen – für eine fundierte Aussage hierzu mangle es schlicht an fehlerfreien Studien.
Metastudien, also die zusammenfassende Analyse verschiedener Studien mit statistischen Mitteln, sind nach Ansicht ihrer Kritiker ein gewagtes Unterfangen, da dieser Ansatz eine Reihe methodischer Probleme mit sich bringen kann;[94] zweifelsfreie Schlussfolgerungen seien bei dieser Art der Analyse daher nicht zwangsläufig möglich. So lobte der Gerontologe John B. Standridge zwar die Arbeit der Forscher um Kaye Fillmore, zweifelt selbst aber weiterhin nicht daran, dass ein moderater Alkoholkonsum der Gesundheit zuträglich sei. Ursächlich für die möglichen positiven Wirkungen sei nicht der Alkohol selbst, sondern Begleitstoffe (sekundäre Pflanzenstoffe von roten Trauben und Inhaltsstoffe der Bierhefe), die im Wein und Bier zu finden seien und durch den Alkohol, der ein gutes Lösungsmittel ist, verfügbar gemacht würden (Lösungsmitteltheorie). Daher besäßen Schnäpse und die meisten Liköre auch keine vergleichbaren Wirkungen.
In anderen Kulturen sind jedoch andere alkoholische Getränke statistisch gesehen vorteilhafter, und es wurde kein signifikanter Unterschied zwischen einzelnen Getränkearten (Bier, Wein und Spirituosen) gefunden, so dass dies für die soziale Komponente als einzigen positiven Faktor spricht. Eine Studie an 38.000 Mitarbeitern des amerikanischen Gesundheitssystems zeigte, dass der Konsum von Bier und anderen Spirituosen – nicht aber von Wein – das Infarktrisiko senkte. Eine Studie aus Schanghai wiederum beschrieb für Reisweintrinker eine geringere koronare Mortalität.
Gesetzliche Beschränkungen
Die Einschränkung der Verfügbarkeit ist eine der wenigen wirksamen Maßnahmen, die ein Staat besitzt, um den Alkohol-Gesamtkonsum und damit die alkoholbedingten Schäden zu vermindern: zum Beispiel Einschränkung der Laden- und Ausschank-Öffnungszeiten, der Anzahl der Betriebe, die Alkohol verkaufen dürfen; die Erteilung von Bewilligungen für Alkoholverkauf an Bedingungen knüpfen (Lizenz, Gebühren, Wirteprüfung, etc.); gesetzliches Mindestalter; Erhöhung der Alkoholsteuer.
In einigen, vorzugsweise islamischen Ländern, ist Alkohol gesetzlich verboten. Getränke wie Absinth sind oder waren bis vor kurzer Zeit wegen ihres (angeblich) erhöhten Gefahrenpotentials auch in vielen europäischen Ländern verboten.
Während der amerikanischen Prohibitionszeit (1919–1932) war der Verkauf von Alkohol in den USA gesetzlich verboten. Dies führte zur massenhaften Entstehung von illegalen Kneipen (Speakeasies) und zum Aufblühen der organisierten Kriminalität. In den USA gibt es nach wie vor Gemeinden mit einem Verbot des Verkaufs, der Bewerbung und des öffentlichen Konsums von Alkohol (Gemeindeautonomie), zum Beispiel auch in Lynchburg in Tennessee, der Heimat des Whiskey Jack Daniel’s.
In Deutschland besteht ein Branntweinmonopol. Das deutsche Gaststättengesetz schreibt im § 6 vor, dass als preiswertestes Getränk – auf Grundlage des hochgerechneten Preises für einen Liter – ein nichtalkoholisches angeboten werden muss.
Jugendschutz
In Deutschland sowie in Österreich dürfen nach dem Jugendschutzgesetz alkoholische Getränke nicht an Personen unter 16 Jahren und Getränke, die Branntwein in mehr als nur geringfügigen Mengen enthalten, erst nach Vollendung des 18. Lebensjahres abgegeben werden (§ 9 Absatz 1 JuSchG). In Deutschland ist das öffentliche Konsumieren von nicht-branntweinhaltigen alkoholischen Getränken in Begleitung von Erziehungsberechtigten ab 14 Jahren gestattet, es gibt sonst keine Beschränkung.
In der Schweiz sind mangels eines eigentlichen Jugendschutzgesetzes die entsprechenden Regelungen in der eidgenössischen Lebensmittelverordnung oder in kantonalen Gewerbegesetzen enthalten. Die Altersgrenzen sind mit denen in Deutschland identisch.[95]
Österreich
In Österreich ist der Jugendschutz Ländersache und ebenfalls relativ komplex, da die Altersgrenze für Jugendliche sowie die Prozentgrenze zwischen hochprozentigen, gebrannten Alkoholika und niedrigprozentigen Alkoholischen Getränken auch vom Bundesland abhängt oder teils gar nicht fest definiert ist. Folgende Tabelle stellt die Bestimmungen jeweils spezifisch dar; die Jahresangaben gelten „ab dem vollendeten Lebensjahr“:[96]
Bundesland/
-länderAlkohol
erlaubt abVol-%-
grenzeGebrannter Alkohol
erlaubt abWien,
Niederösterreich,
Burgenland16 keine 16 Steiermark,
Oberösterreich16 14 Vol.-% 18 Kärnten 16 12 Vol.-% 18 Salzburg 16 n. def.[97] 18 Tirol 14 / 16[98] n. def.[97] 18 Vorarlberg 16 n. def.[99] 18 Quellen,[96] Vorarlberg,[100] Tirol[101] Andere Länder – beispielsweise die meisten Bundesstaaten der USA – sehen als Mindestalter zum öffentlichen sowie privaten Verzehr von Alkohol das vollendete 21. Lebensjahr vor.
Verkehr
Da Alkohol die Fahrtüchtigkeit einschränkt, ist im Straßenverkehr das Fahren unter Alkoholeinfluss in den meisten Ländern der Welt unter Strafe gestellt. In Deutschland gelten 1,1 ‰ als absolute Grenze der Fahruntüchtigkeit. Eine relative Fahruntüchtigkeit kann bereits ab 0,3 ‰ vorliegen, wenn Ausfallerscheinungen erkennbar sind oder ein Verkehrsunfall passiert ist. Ab 0,5 ‰ (bzw. 0,25 mg/l bei Atemalkoholproben) begeht der Fahrer eine Ordnungswidrigkeit, die mit Geldbuße und Fahrverbot geahndet wird. In Deutschland gilt bei Fahranfängern seit dem 1. August 2007 die 0,0-‰-Grenze.[102] In Österreich dürfen Probeführerscheinbesitzer maximal 0,1 ‰ Alkohol im Blut haben.
Für Fahrräder gilt in Deutschland ein Grenzwert von 1,6 ‰ Blutalkoholkonzentration nach §13c der Fahrerlaubnisverordnung. Bei Überschreitung des Grenzwertes ist ein medizinisch-psychologisches Gutachten zu erbringen, welches belegt, dass keine Einschränkung zur Fahrtüchtigkeit auf Kraftfahrzeugen besteht.[103]
Im Schiffsverkehr gilt im Gültigkeitsbereich der Seeschifffahrtsstraßen-Ordnung für den Führer eines Fahrzeuges und Personal mit Tätigkeit im Brücken-, Deck- oder Maschinendienst ein BAK-Grenzwert von 0,5 ‰. (SeeSchStrO §3(4))
Im Luftverkehr gibt es in Deutschland zumindest nach der Luftverkehrs-Ordnung keine geschriebene BAK-Grenze. In §1, Absatz 3 der Luftverkehrs-Ordnung heißt es „Wer infolge des Genusses alkoholischer Getränke oder anderer berauschender Mittel oder infolge geistiger oder körperlicher Mängel in der Wahrnehmung der Aufgaben als Führer eines Luftfahrzeugs oder sonst als Mitglied der Besatzung behindert ist, darf kein Luftfahrzeug führen und nicht als anderes Besatzungsmitglied tätig sein.“ (Luftverkehrs-Ordnung §1[104]). Im gewerblichen Luftverkehrs sind jedoch zusätzlich die Regeln nach JAR-OPS 1.085(d)[105] einzuhalten. Danach ist es nicht gestattet
- innerhalb von acht Stunden vor der festgelegten Meldezeit zu einem Flugdienst oder vor dem Beginn einer Bereitschaftszeit Alkohol zu sich zu nehmen
- eine Flugdienstzeit mit einem Blutalkoholspiegel von mehr als 0,2 ‰ anzutreten
- während einer Flugdienst- oder Bereitschaftszeit Alkohol zu sich zu nehmen
Auch in vielen Luftsportvereinen ist unter Anderem aus Haftungsgründen das Fliegen unter Alkoholeinfluss durch interne Regelungen untersagt.
Literatur
- Ekkehard Grundmann (Hg.): Spezielle Pathologie. Lehrbuch. bgr.v. Franz Büchner, 7., neu bearb. Aufl., München/Wien/Baltmimore 1986, ISBN 3-541-00467-3.
- Wolfgang Forth e.a. (Hgg.): Allgemeine und spezielle Pharmakologie und Toxikologie. Für Studenten der Medizin, Veterinärmedizin, Pharmazie, Chemie, Biologie sowie für Ärzte, Tierärzte und Apotheker. 6., völlig neu bearb. Aufl., Mannheim/Leipzig/Wien/Zürich 1992, ISBN 3-411-15026-2.
- Karl-Heinz Niessen (Hg.): Pädiatrie. 3., neubearbeitete Aufl., Weinheim/Basel/Cambridge/New York 1993, ISBN 3-527-15517-1.
- Hans Joachim Mallach, H. Hartmann und V. Schmidt: Alkoholwirkung beim Menschen – Pathophysiologie, Nachweis, Intoxikation, Wechselwirkungen. G. Thieme Verlag, Tübingen, New York (1987), ISBN 3-13-697101-9.
- Singer, Teyssen (Hrsg.): Alkohol und Alkoholfolgekrankheiten. 2. Auflage. Springer, Heidelberg 2005, ISBN 3-540-22552-8.
- Günter Schmidt: ALEX – Das Alkohollexikon. Books on Demand (BoD), Norderstedt 2002, ISBN 3-8311-3825-7.
- Bernhard van Treeck: Drogen- und Suchtlexikon. Lexikon-Imprint-Verlag, Berlin 2003, ISBN 3-89602-221-0.
- Bernhard van Treeck: Drogen. Schwarzkopf & Schwarzkopf, Berlin 2003, ISBN 3-89602-420-5.
- Arthur L. Klatsky: Alkohol fürs Herz. in: Spektrum der Wissenschaft. Spektrumverlag, Heidelberg 25.2003,10, ISSN 0170-2971, S. 62–68.
- J. Kauhanen u. a.: Beer binging and mortality, results from the Kuopio ischaemic heart desease risk factor study, a prospective population based study. in: British Medical Journal. London 315.1997, ISSN 0267-0623, S. 846.
- E. B. Rimm u. a.: Moderate alcohol intake and lower risk of coronary heart desease, meta-analysis on effects on lipids and haemostatic factors. in: British Medical Journal. London 319.1999, ISSN 0267-0623, S. 1523.
- K. Nanchal u. a.: Alcohol consumption, metabolic cardiovascular risk factors and hypertension in women. in: International Journal on Epidemiology. Oxford Univ. Press, Oxford 29.2000, ISSN 0300-5771, S. 57.
- C. Power u. a.: U-shaped relation for alcohol consumption and health in early adulthood and implications for mortality. in: The Lancet. Elsevier Science, New York 352.1988, ISSN 1474-547X, S. 877.
- Hans-Peter Beck-Bornholdt: Der Hund, der Eier legt. Erkennen von Fehlinformation durch Querdenken. Rowohlt, Reinbek bei Hamburg 2002, ISBN 3-499-61154-6.
- Knut Kröger: Lebenserwartung – Der Mythos vom Rotwein. in: Deutsches Ärzteblatt. Köln 100.2003,42 (17. Oktober), S. A-2706, B-2260, C-2120. ISSN 0012-1207.
Weblinks
 Commons: Ethanol – Sammlung von Bildern, Videos und Audiodateien
Commons: Ethanol – Sammlung von Bildern, Videos und Audiodateien Wiktionary: Alkohol – Bedeutungserklärungen, Wortherkunft, Synonyme, Übersetzungen
Wiktionary: Alkohol – Bedeutungserklärungen, Wortherkunft, Synonyme, Übersetzungen Wikinews: Alkohol – in den Nachrichten
Wikinews: Alkohol – in den Nachrichten Wikiquote: Alkohol – Zitate
Wikiquote: Alkohol – Zitate- Wie wirkt Alkohol im Gehirn?, Beitrag vom 10. Februar 2004 bei Quarks & Co
- „Alkohol“ Ethanol – ein Artikel zum Thema von Peter Bützer (PDF-Datei; 966 kB)
Hörspiel
Das folgende Hörspiel behandelt die zentralen Themen dieses Artikels in Dialogform.
Einzelnachweise
- ↑ a b c d e f g h Thieme Chemistry (Hrsg.): Eintrag zu Ethanol im Römpp Online. Version 3.14. Georg Thieme Verlag, Stuttgart 2011, abgerufen am 11. November 2011.
- ↑ a b c d e f Eintrag zu CAS-Nr. 64-17-5 in der GESTIS-Stoffdatenbank des IFA, abgerufen am 5. Januar 2008 (JavaScript erforderlich).
- ↑ a b c d e f g h Ethanol bei ChemIDplus.
- ↑ a b Eintrag zu CAS-Nr. 64-17-5 im European chemical Substances Information System ESIS (ergänzender Eintrag)
- ↑ Toxicology and Applied Pharmacology. Vol. 16, Pg. 718, 1970.
- ↑ Gigiena i Sanitariya. For English translation, see HYSAAV. Vol. 32(3), Pg. 31, 1967.
- ↑ Raw Material Data Handbook, Vol.1: Organic Solvents, 1974. Vol. 1, Pg. 44, 1974.
- ↑ Alcoholism: Clinical and Experimental Research. Vol. 7, Pg. 289, 1983.
- ↑ Neurobehavioral Toxicology and Teratology. Vol. 8, Pg. 77, 1986.
- ↑ Journal of UOEH. Vol. 9, Pg. 53, 1987.
- ↑ a b Gerhard Eisenbrand (Hrsg.), Peter Schreier (Hrsg.): RÖMPP Lexikon Lebensmittelchemie. 2. Auflage, Thieme Verlag, Stuttgart 2006, S. 322.
- ↑ http://www.who.int/gho/alcohol/en/index.html
- ↑ Wissenschaft-Online-Lexika: Alkohole im Lexikon der Biologie. abgerufen am 3. Januar 2011.
- ↑ Nabil Osman(Hrsg.): Kleines Lexikon deutscher Wörter arabischer Herkunft. Beck'sche Reihe, 8. Auflage, München 2010, C.H.Beck, ISBN 978-3-406-60155-2, S. 25.
- ↑ a b J. Westermeyer: Cross-cultural studies on alcoholism. In: H. W. Goedde: Alcoholism: Biomedical and genetic aspects. Pergamon Press, New York; S. 305–311.
- ↑ a b D. von Cranach: Drogen im Alten Ägypten. In: G. Völger, K. Welck: Rausch und Realität: Drogen im Kulturvergleich, Bd 2. Rowohlt, Reinbek, 1982; S. 480–487.
- ↑ W. Färber: Drogen im Alten Ägypten. In: G. Völger, K. Welck: Rausch und Realität: Drogen im Kulturvergleich, Bd 2; Rowohlt, Reinbek, 1982; S. 480–487.
- ↑ Heinrich Grüger: Das Trebnitzer Rechnungsbuch von 1523–1524 und andere Quellen zur mittelalterlichen und frühneuzeitlichen Besitzgeschichte eines schlesischen Zisterzienserinnenklosters. Band 1; Historische und landeskundliche Ostmitteleuropa-Studien; J.G. Herder-Institut, 1986, ISBN 978-3-87969-196-8, S. 166. Dietrich Beyrau, Rainer Lindner: Handbuch der Geschichte Weissrusslands. Vandenhoeck & Ruprecht, 2001, ISBN 978-3-525-36255-6; S. 385.
- ↑ a b Singer, Teyssen (Hrsg.): Alkohol und Alkoholfolgekrankheiten. 2. Auflage. Springer, Heidelberg 2005, ISBN 3-540-22552-8.
- ↑ Klaus Dehnert, Norbert Jäckel, Egon Petrak, Werner Rauh und Verlagsredaktion: Chemie heute – Nordrhein-Westfalen, 9/10 Schuljahr. Schroedel Schulbuchverlag, Hannover 1988, ISBN 3-507-86022-8.
- ↑ Evelyn Boos, Thomas Priermeier: Gewinnchance Klimawandel: Investitionsmöglichkeiten und Anlagestrategien. Linde Verlag, Wien 2008, ISBN 978-3-7093-0216-3, S. 81.
- ↑ C. Ford Runge, Benjamin Senauer: How Biofuels Could Starve the Poor, Council on Foreign Affairs, Mai/Juni 2007
- ↑ a b Franz-Lothar Altmann, Josef Braml: Weltverträgliche Energiesicherheitspolitik: Jahrbuch internationale Politik 2005/2006. Deutsche Gesellschaft für Auswärtige Politik, Oldenbourg Wissenschaftsverlag, 2008, ISBN 978-3-486-58342-7, S. 153.
- ↑ WIGL Lehrmittel: Südweine (doc)
- ↑ Nagl-Netzreport: Haltbarmachung von Lebensmitteln.
- ↑ a b H.-H. Frey, F. R. Althaus: Lehrbuch der Pharmakologie und Toxikologie für die Veterinärmedizin. S. 469, Georg Thieme Verlag, 2007, ISBN 978-3-8304-1070-6.
- ↑ Herbert Hof, Rüdiger Dörries: Medizinische Mikrobiologie, Georg Thieme Verlag, Stuttgart 2005, 3. Aufl. S.686
- ↑ Percutane Alkohol Injektion (PEI) der Schilddrüse bei www.madeasy.de
- ↑ Lothar-Andreas Hotze, Petra-Maria Schumm-Draeger: Schilddrüsenkrankheiten. Diagnose und Therapie. Berlin 2003, ISBN 3-88040-002-4.
- ↑ Alkohol-Dehydrogenase.
- ↑ a b Karl-Ludwig Haken: Grundlagen der Kraftfahrzeugtechnik. Hanser Verlag, 2007, ISBN 978-3-446-22812-2, S. 23.
- ↑ E.W. Flick: Industrial Solvents Handbook. Fifth Edition, Noyes Data Corporation (ndc), Westwood, NJ/USA 1998, ISBN 0-8155-1413-1, S. 252.
- ↑ Eintrag zu Diethylsulfat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 22. Juli 2008 (JavaScript erforderlich)
- ↑ a b H. Lüllmann, L. Hein, K. Mohr, M. Wehling: Pharmakologie und Toxikologie. 16. Auflage, Georg Thieme Verlag, 2006, ISBN 978-3-13-368516-0, S. 521.
- ↑ K. Roth: Die Chemie des Katers: Alkohol und seine Folgen. in: Chemie in Unserer Zeit 2007, 41, 46. doi:10.1002/ciuz.200700409.
- ↑ W. Gerok, C. Huber, T. Meinertz, H. Zeidler, Henning (Hrsg.): Die innere Medizin: Referenzwerk für den Facharzt. 11. Auflage, Schattauer Verlag, 2006, ISBN 978-3-7945-2222-4, S. 644–646.
- ↑ a b c Hans-Konrad Biesalski, Olaf Adam: Ernährungsmedizin: Nach dem Curriculum Ernährungsmedizin der Bundesärztekammer. 3. Auflage, Georg Thieme Verlag, 2004, ISBN 978-3-13-100293-8, S. 520–528.
- ↑ a b c d P. Schauder, G. Ollenschläger: Ernährungsmedizin: Prävention und Therapie. Elsevier Deutschland, 2006, ISBN 978-3-437-22921-3.
- ↑ Heinrich Kasper: Ernährungsmedizin und Diätetik. 10. Auflage, Elsevier, Urban & Fischer Verlag, 2004, ISBN 978-3-437-42011-5, S. 70.
- ↑ Eduard Burgis: Intensivkurs allgemeine und spezielle Pharmakologie. 4. Auflage, Elsevier, Urban & Fischer Verlag, 2008, ISBN 978-3-437-42613-1, S. 520.
- ↑ a b c Detlev Ganten, Klaus Ruckpaul: Erkrankungen des Zentralnervensystems. Springer, 1999, ISBN 978-3-540-64552-8, S. 180.
- ↑ H.-J. Möller, G. Laux, H.-P. Kapfhammer: Psychiatrie und Psychotherapie. 2. Auflage, Springer, 2005, ISBN 978-3-540-25074-6, S. 97.
- ↑ a b c H. Abdolvahab-Emminger, T. Kia: Exaplan: Das Kompendium der klinischen Medizin. 5. Auflage, S. 2402, Elsevier, Urban&FischerVerlag, 2007, ISBN 978-3-437-42462-5.
- ↑ Watson PE, Watson R, Batt RD: Total body water volumes for adult males and females estimated from simple anthropometric measurements. The American Journal of Clinical Nutrition 33: Januar 1980, S. 27–39; PMID 6986753.
- ↑ G. Schoknecht unter Mitarbeit von H.-U. Melchert u. W. Thefeld: Prüfung von elektronischen Atemalkoholtestverfahren – Eine Stellungnahme des Bundesgesundheitsamtes. SozEp-Berichte 1981/8, D. Reimer Verlag, Berlin, ISBN 3-496-02114-4.
- ↑ Grundmann, S. 258.
- ↑ Grundmann, S. 75.
- ↑ Niessen, S. 64.
- ↑ Forth e.a., S. 798.
- ↑ Mann mit knapp 7,7 Promille aufgefunden Tagesspiegel.de, abgerufen am 13. November 2008.
- ↑ Toxicology and Applied Pharmacology. Vol. 16, S. 718, 1970.
- ↑ Deutsche Hauptstelle für Suchtfragen (DHS): Jahresbericht 2004.
- ↑ Stiftung Warentest: Nervenschäden durch Alkohol, Meldung vom 15. Januar 2009.
- ↑ a b F.-J. Kretz, K. Becke: Anästhesie und Intensivmedizin bei Kindern. 2. Auflage, Georg Thieme Verlag, 2006, ISBN 978-3-13-110232-4, S. 23.
- ↑ Detlev Ganten, Klaus Ruckpaul: Erkrankungen des Zentralnervensystems. Springer, 1999, ISBN 978-3-540-64552-8.
- ↑ Deutsche Krebsgesellschaft: Gesundheitsgefahren durch Alkohol – Gehirn und Nervensystem
- ↑ Ikonomidou C, Bittigau P, Ishimaru MJ, Koch C, Genz K, Price MT, Stefovska V, Hörster F, Tenkova T, Dikranian K, Olney JW: Ethanol-induced apoptotic neurodegeneration and fetal alcohol syndrome. Science, 287:1056-1060, 2000.
- ↑ A. E. Kulozik, M. W. Hentze, C. R. Bartram, C. Hagemeier: Molekulare Medizin: Grundlagen, Pathomechanismen, Klinik. Walter de Gruyter, 2000, ISBN 978-3-11-015097-1, S. 154–157.
- ↑ Harvey Lodish et. al.: Molecular Cell Biology. 6th edition, Palgrave Macmillan, ISBN 1-4292-0314-5, S. 940.
- ↑ J. Kornhuber, C.H. Kaiserauer, A.W. Kornhuber, M.E. Kornhuber: Alcohol consumption and blood-cerebrospinal fluid barrier dysfunction in man. Neurosci. Lett. 79:218-222,1987. PMID 3670730
- ↑ E. M. Cornford u. a.: Comparison of lipid-mediated blood-brain-barrier penetrability in neonates and adults. In: Am J Physiol 243, 1982, S. 161C–168C. PMID 7114247.
- ↑ I. Elmas u. a.: Effects of profound hypothermia on the blood-brain barrier permeability in acute and chronically ethanol treated rats. In: Forensic Science International 119, 2001, S. 212–216. PMID 11376985.
- ↑ S. C. Phillips und B. G. Cragg: Weakening of the blood-brain barrier by alcohol-related stresses in the rat. In: J Neurol Sci 54, 1982, S. 271–278. PMID 7201507.
- ↑ A. K. Singh u. a.: Effects of chronic ethanol drinking on the blood brain barrier and ensuing neuronal toxicity in alcohol-preferring rats subjected to intraperitoneal LPS injection. In: Alcohol Alcohol 42, 2007, S. 385–399. PMID 17341516.
- ↑ J. Haorah u. a.: Alcohol-induced blood-brain barrier dysfunction is mediated via inositol 1,4,5-triphosphate receptor (IP3R)-gated intracellular calcium release. In: J Neurochem 100, 2007, S. 324–336. PMID 17241155.
- ↑ F. Rötzer: Schrumpfende Gehirne. Nach einer Studie führt auch mäßiger Alkoholkonsum bereits zu Gehirnatrophie. Artikel vom 7. Dezember 2003 in Telepolis.
- ↑ J. Ding, M. L. Eigenbrodt et. al.: Alcohol Intake and Cerebral Abnormalities on Magnetic Resonance Imaging in a Community-Based Population of Middle-Aged Adults. The Atherosclerosis Risk in Communities (ARIC) Study. In: Stroke, 4. Dezember 2003.
- ↑ Weshalb sich Menschen unter Alkoholeinfluss riskant verhalten
- ↑ X. D. Wang et. al.: Chronic alcohol intake reduces retinoic acid concentration and enhances AP-1 (c-Jun and c-Fos) expression in rat liver. Hepatology 1998;28:744–750.
- ↑ X. D. Wang: Alcohol, vitamin A and cancer. Alcohol 2005;35:251–258.
- ↑ Ärzteblatt: Studie: Jede zweite Schwangere trinkt Alkohol. 8. September 2008.
- ↑ Ärzteblatt: Kinderhilfe: Strikter gegen Alkoholkonsum Schwangerer vorgehen. 9. September 2008.
- ↑ ZDF heute.de: Auch ein Schluck Sekt ist tabu — Alkohol in der Schwangerschaft macht Kinder ein Leben lang krank. 9. September 2008.
- ↑ destatis.de: Alkoholmißbrauch kostete mehr als 16.000 Menschen das Leben, Zahl der Woche Nr.13 vom 27. März 2007, Zugriff am 30. August 2011.
- ↑ World Health Organization (Hrsg.): Global status report on alcohol and health. Genf Februar 2011, ISBN 978-92-4156415-1, 2.2.1, S. 24 (http://www.who.int/substance_abuse/publications/global_alcohol_report/msbgsruprofiles.pdf, abgerufen am 27. April 2011).
- ↑ Arch Intern Med 170, 2010, 711, zitiert nach Ärzte-Zeitung, 28. April 2010, S. 2.
- ↑ Statistisches Bundesamt
- ↑ Drogen- und Suchtbericht, 2004.
- ↑ Dirk Lachenmeier: „Warning Labels“ statt „Health Claims“? IARC Neubewertung von Ethanol in alkoholischen Getränken als „Gruppe-1-Karzinogen“. Conference presentation at the Deutscher Lebensmittelchemikertag 2007.
- ↑ WCRF/AICR Expert Report, Food, Nutrition, Physical Activity and the Prevention of Cancer: a Global Perspective. S. 384.
- ↑ wissenschaft.de: Was Kater und Krebs gemeinsam haben, 5. August 2005.
- ↑ S Bleich, K Bleich, S Kropp, HJ Bittermann, D Degner, W Sperling, E Rüther, J Kornhuber. Moderate alcohol consumption in social drinkers raises plasma homocysteine levels: a contradiction to the "french paradox"? Alcohol Alcohol. 36:189-192, 2001. PMID 11373253
- ↑ S Bleich, M Carl, K Bayerlein, U Reulbach, T Biermann, T Hillemacher, D Bönsch, J Kornhuber. Evidence of increased homocysteine levels in alcoholism: the Franconian Alcoholism Research Studies (FARS). Alcohol.Clin.Exp.Res. 29:334-336, 2005. PMID 15770107
- ↑ S Bleich, B Bandelow, K Javaheripour, A Müller, D Degner, J Wilhelm, U Havemann-Reinecke, W Sperling, E Rüther, J. Kornhuber. Hyperhomocysteinemia as a new risk factor for brain shrinkage in patients with alcoholism. Neurosci.Lett. 335:179-182, 2003. PMID 12531462
- ↑ S Bleich, D Degner, B Bandelow, N von Ahsen, E Rüther, J Kornhuber. Plasma homocysteine is a predictor for ethanol withdrawal seizures. NeuroReport 11:2749-2752, 2000. PMID 10976956
- ↑ J Wilhelm, K Bayerlein, T Hillemacher, U Reulbach, H Frieling, B Kromolan, D Degner, J Kornhuber, S Bleich. Short-term cognitive deficits during early alcohol withdrawal are associated with elevated plasma homocysteine levels in patients with alcoholism. J.Neural Transm. 113:357-363, 2006.PMID 15997414
- ↑ M. Croon, K. Arends-Kailer (Übers.): Schwanger werden. S. 45, Georg Thieme Verlag, 2005, ISBN 978-3-8304-3284-5.
- ↑ A. Feige, A. Rempen, W. Würfel, J. Jawny, A. Rohde: Frauenheilkunde: Fortpflanzungsmedizin, Geburtsmedizin, Onkologie, Psychosomatik. 3. Auflage, S. 776, Elsevier, Urban&FischerVerlag, 2006, ISBN 978-3-437-21871-2.
- ↑ B. Altinkilic, R. G. Bretzel, W.-B. Schill, W. Weidner, Schill-Bretzel-Weidner: Männermedizin: In der allgemeinmedizinischen und internistischen Praxis. S. 128, Elsevier, Urban&FischerVerlag, 2005, ISBN 978-3-437-23260-2.
- ↑ Studie zu Krebsrisiko durch Alkohol
- ↑ Naimi TS, Brown DW, Brewer RD, Giles WH, Mensah G, Serdula MK, Mokdad AH, Hungerford DW, Lando J, Naimi S, Stroup DF: Cardiovascular risk factors and confounders among nondrinking and moderate-drinking U.S. adults. Am J Prev Med 2005; 28: 36973; PMID 15831343.
- ↑ Fillmore KM, Kerr WC, Stockwell T, Chikritzhs T, Bostrom A: Moderate alcohol use and reduced mortality risk: Systematic error in prospective studies. Addiction Research and Theory 2006; 1–31.
- ↑ Kaye M. Fillmore u. a.: Does moderate drinking prevent heart disease? A meta-analysis and re-estimation of alcohol-caused mortality in Australia. Universität von Kalifornien, San Francisco. in: Addiction Research and Theory. Brunner-Routledge Health Sciences, London 2006,5 (Mai). ISSN 1606-6359
- ↑ Probleme der Metaanalyse Beitrag bei www.dgps.de
- ↑ Hermann Fahrenkrug, Matthias Meyer, Elke Richter, Anja Schmittpott: Jugendschutz und Alkohol. Ein Grundlagenpapier zu strukturellen Massnahmen in der Schweiz und ausgewählten Ländern Europas. Schweizerische Fachstelle für Alkohol- und andere Drogenprobleme, Lausanne, Stand Mai 2005.
- ↑ a b Bundesarbeitsgemeinschaft Kinder- und Jugendschutz (BAJ): Regelungen zum gesetzlichen Kinder- und Jugendschutz in Österreich
- ↑ a b Der Gesetzext nennt Branntwein und branntweinähnliche Getränke sowie Alkoholkonsum, der eine Beeinträchtigung des Bewusstseins zur Folge hat
- ↑ Der Gesetzestext erlaubt Alkohol ab dem 14. Lebensjahr, wobei allerdings Weitergabe und der Konsum in der Öffentlichkeit ab dem vollendeten 14. bis zum vollendeten 16. Lebensjahr verboten sind.
- ↑ Der Gesetzext nennt gebrannte alkoholische Getränke oder solche enthaltende Mischgetränke
- ↑ Rechtsinformationssystem des Bundes (RIS): Gesetz über die Förderung und den Schutz der Jugend, §17
- ↑ Land Tirol: Überblick Jugendschutzgesetz. Alkohol Abgerufen am 19. Januar 2010
- ↑ 0,0 ‰ Grenze für Fahranfänger
- ↑ § 13 Fahrerlaubnisverordnung
- ↑ Luftverkehrs-Ordnung §1
- ↑ JAR-OPS 1.085(d) Bekanntmachung der deutschen Übersetzung der Bestimmungen der Joint Aviation Authorities über die gewerbsmäßige Beförderung von Personen und Sachen in Flugzeugen (JAR-OPS 1), Fassung vom 1. März 1998

Bitte den Hinweis zu Gesundheitsthemen beachten! Kategorien:- Feuergefährlicher Stoff
- Wikipedia:Gesprochener Artikel
- Sedativum
- Alkohol
- Mykotoxin
- Pharmazeutischer Hilfsstoff
- Antidot
- Droge
- Delirantium
- Kosmetischer Inhaltsstoff
- Lebensmittelinhaltsstoff
- Arzneistoff
Wikimedia Foundation.