- Zeise-Salz
-
Strukturformel 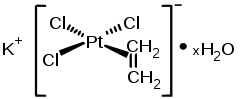
Allgemeines Name Zeise-Salz Andere Namen Kaliumtrichloridoethylenplatinat(II)-hydrat
Summenformel C2H4Cl3KPt CAS-Nummer 123334-22-5 Kurzbeschreibung gelber Feststoff[1]
Eigenschaften Molare Masse 368,61 g·mol−1 Aggregatzustand fest
Dichte 2,88 g·cm3−[1]
Schmelzpunkt Sicherheitshinweise GHS-Gefahrstoffkennzeichnung [1] 
Achtung
H- und P-Sätze H: 315-319-335 EUH: keine EUH-Sätze P: 261-305+351+338 [1] EU-Gefahrstoffkennzeichnung [1] 
Reizend (Xi) R- und S-Sätze R: 36/37/38 S: 26-37/39 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Bei dem Zeise-Salz handelt es sich um einen Platinkomplex mit der Summenformel K[PtCl3(C2H4)]·H2O. Er wurde von dem dänischen Chemiker William Christopher Zeise entdeckt und gilt als eine der ersten synthetisierten metallorganischen Verbindungen.
Inhaltsverzeichnis
Darstellung und Gewinnung
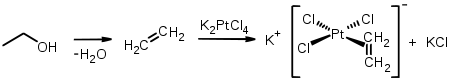
Zeise erhielt den Komplex durch Kochen von Kaliumtetrachloridoplatinat(II) (K2[PtCl4]) in Ethanol. Hierbei spaltet sich aus Ethanol Wasser ab unter der Bildung von Ethen. Dieses koordiniert dann an das Platinzentrum und bildet das Zeise-Salz.[2]
Zeise postulierte damals, dass das entstandene Salz Ethen enthielte. Dies konnte jedoch erst Jahrzehnte später bestätigt werden, als Kaliumtetrachloridoplatinat(II) mit Ethen zur Reaktion gebracht wurde und das gleiche Salz erhalten wurde.[3]
Struktur
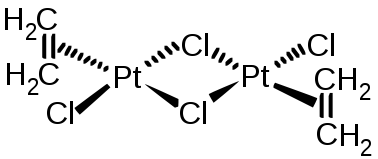
Im Zeise-Salz ist das zentrale Platinion quadratisch-planar koordiniert. Im Festkörper steht der Ethylenligand senkrecht zu dieser Ebene, in Lösung jedoch rotiert er um die σ-Bindung zum Metallion.[4] Durch Eliminierung von Kaliumchlorid kann das Dimer des Zeise-Salzes erhalten werden.
Einzelnachweise
- ↑ a b c d e f Datenblatt Potassium trichloro(ethylene)platinate(II) hydrate bei Sigma-Aldrich, abgerufen am 25. April 2011.
- ↑ W. C. Zeise: Annalen der Physik und Chemie 1831, 97, 497–541.
- ↑ K. Birnbaum: Annalen der Chemie und Pharmacie 1869, 152 (2), 137–147.
- ↑ Christoph Elschenbroich: Organometallchemie 2002 Teubner Verlag.
Siehe auch
Kategorien:- Reizender Stoff
- Kaliumverbindung
- Chlorverbindung
- Platinverbindung
- Metallorganische Verbindung
- Komplex
Wikimedia Foundation.