- Cyanogenes Glycosid
-
Cyanogene Glycoside sind weit verbreitete Pflanzengifte aus der Gruppe der Glycoside.
Inhaltsverzeichnis
Wirkung
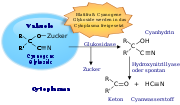
Cyanogene Glycoside selbst haben keinen toxischen Effekt, erst durch Spaltung des Moleküls kommt es zur Freisetzung der Blausäure (HCN), die den eigentlich giftigen Stoff darstellt. Der Abbau erfolgt zunächst enzymatisch. Durch eine mehr oder weniger spezifische β-Glucosidase wird der Zuckeranteil (meist Glucose) abgespalten. Es entsteht das freie Cyanhydrin. Dieses zerfällt spontan (oder enzymkatalysiert: Hydroxynitril Lyase) in ein Keton oder Aldehyd und HCN.
Entscheidend für diesen als Cyanogenese bezeichneten Vorgang ist die initiale Abspaltung des Zuckeranteils. Beispielsweise wird für die Spaltung des Glycosids Linamarin das Enzym Linamarase benötigt. Bei der intakten Pflanze liegen beide Stoffe in verschiedenen Organellen getrennt vor und das Glykosid bleibt erhalten (Kompartimentierung). Dies hat den Vorteil, dass die Toxine erst dann freigesetzt werden, wenn es zu einer Beschädigung der Pflanzenzellen (etwa durch Insektenfraß) kommt und so das Gift direkt produziert wird (Dekompartimentierung, Pflanzliche Abwehr von Herbivoren).
Auswirkungen auf den Organismus
Die von cyanogenen Glycosiden freigesetzte Blausäure ist für fast alle Tiere hochgiftig. Der Grund liegt darin, dass die Blausäure in den Stoffwechsel eingreift. Die Photosynthese der Pflanzen ist nicht betroffen. Der Energiestoffwechsel der Tiere hingegen wird innerhalb kürzester Zeit lahmgelegt.
HCN bindet an das zentrale Eisenion (Sauerstoff-Bindungsstelle) des Enzyms Cytochrom c Oxidase, welches eine grundlegende Redoxreaktion der Atmungskette ablaufen lässt. Dadurch wird das Enzym irreversibel inaktiviert. Wenn ein gewisser Anteil der Cytochrom c Oxidase durch HCN gebunden ist, fällt die Atmungskette aus, und der Organismus bekommt keine Energie mehr. Die Wirkung ist ähnlich wie bei Kohlenmonoxid (CO).
Polymorphismen beim Weißklee und Hornklee
Ein Polymorphismus von cyanogenen Glycosiden tritt in Europa bei verschiedenen Kleepopulationen auf. Durch Züchtungsexperiment lässt sich feststellen, dass zwei voneinander unabhängige Gene dafür verantwortlich sind.
Eines der Gene steuert die Synthese der cyanogenen Glycoside. Nur wenn dieses dominant ist, kann die Pflanze überhaupt diese Substanzen produzieren.
Das zweite Gen ist für das Enzym verantwortlich, das erforderlich ist, um die Glycoside zu spalten und damit gefährlich zu machen. Es gibt daher vier verschiedene Arten von Klee in Bezug auf ihre Toxizität durch cyanogene Glycoside. Nur wenn beide Gene dominant sind, kommt es zur toxischen Wirkung. Andernfalls können die Pflanzen zwar die Glycoside synthetisieren, lassen sie jedoch nicht entfalten. Oder es sind die Enzyme vorhanden, jedoch keine Glycoside, die gespalten werden könnten. Im vierten Fall sind weder Glycoside noch Enzyme vorhanden.
Welche Gene die Pflanze in sich trägt, lässt sich durch chemische Tests untersuchen: Man gibt frische Blätter in ein Teströhrchen, zerquetscht sie kurz mit einem Glasstab zusammen mit einem Tropfen Chloroform und verschließt das Röhrchen mit einem Stopfen, von dem ein Stück in Pikrinsäure-Lösung getauchtes Filterpapier herunterhängt. Eine Färbung innerhalb einer Stunde zeigt an, dass Blausäure vorhanden ist, und damit beide Gene dominant sind.
Literatur
Jeffrey B. Harborne: Ökologische Biochemie. Eine Einführung. ISBN 3-86025-245-3 (Schilderung der Wirkungen von Pflanzenstoffen auf Tiere.)
Wikimedia Foundation.