- Chloroform
-
Strukturformel 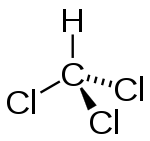
Allgemeines Name Chloroform Andere Namen - Trichlormethan (IUPAC)
- Chloretherid
- Methenylchlorür
- Methinchlorid
- TCM
Summenformel CHCl3 CAS-Nummer 67-66-3 PubChem 6212 Kurzbeschreibung farblose Flüssigkeit mit süßlichem Geruch[1]
Eigenschaften Molare Masse 119,38 g·mol−1 Aggregatzustand flüssig
Dichte 1,48 g·cm−3 (20 °C)[1]
Schmelzpunkt Siedepunkt 61 °C[1]
Dampfdruck Löslichkeit schlecht in Wasser (8,2 g·l−1 bei 20 °C)[1]
Brechungsindex 1,445 (nD20)[2]
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung aus EU-Verordnung (EG) 1272/2008 (CLP) [3] 

Achtung
H- und P-Sätze H: 302-315-351-373 EUH: keine EUH-Sätze P: 302+352-314 [1] EU-Gefahrstoffkennzeichnung aus EU-Verordnung (EG) 1272/2008 (CLP) [3] 
Gesundheits-
schädlich(Xn) R- und S-Sätze R: 22-38-40-48/20/22 S: (2)-36/37 MAK 0,5 ml·m−3[1]
Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C Chloroform (systematische Bezeichnung Trichlormethan) ist ein chlorierter Kohlenwasserstoff mit der Summenformel CHCl3.
Inhaltsverzeichnis
Geschichte
Chloroform wurde im Jahre 1831 unabhängig voneinander von Justus von Liebig und Eugène Soubeiran hergestellt. Nachdem seine narkotisierende Wirkung schon im Jahre 1842 durch den britischen Arzt Robert Mortimer Glover und 1847 durch den französischen Physiologen Marie Jean Pierre Flourens sowie den schottischen Geburtshelfer James Young Simpson erkannt worden war, war es das Verdienst des Letzteren, Chloroform ein Jahr darauf in die ärztliche Praxis einzuführen und unzähligen Patienten Operationsschmerzen zu ersparen.
Aufgrund der damaligen Operationsverfahren hatte die Verwendung dieses Narkotikums große Bedeutung für die ganze chirurgische Tätigkeit: So fürchteten die Kranken schon lange vor einer Operation die bevorstehenden Schmerzen und kamen dann vielfach bereits verunsichert auf den Operationstisch. Dort wurden sie nach bestimmten, für jede besondere Operation vorgezeichneten Methoden fixiert, damit sie während der schmerzhaften Prozedur nicht etwa durch störende Bewegungen die Ärzte behinderten. Bei dem Eingriff selbst war dann das wichtigste Erfordernis die Schnelligkeit, der oft die Exaktheit, Sauberkeit und Gründlichkeit zum Opfer fielen.
Herstellung
Industriell wird Chloroform durch Erhitzen von Chlor mit Methan oder Chlormethan auf 400–500 °C erzeugt. Bei dieser Temperatur wird schrittweise radikalisch substituiert bis hin zum Tetrachlormethan:
Dabei reagiert Methan mit Chlor unter Bildung von Chlorwasserstoff zunächst zu Chlormethan, dann weiter zu Dichlormethan, Trichlormethan und schließlich zu Tetrachlormethan. Das Ergebnis des Prozesses ist eine Mischung der vier Chlormethane, welche durch Destillation getrennt werden können. Industriell hergestelltes Chloroform technischer Reinheit enthält zudem Brom- und Ethanderivate (z.B. Bromchlormethan, Bromdichlormethan, 1,2-Dichlorethan) als Verunreinigung[4] sowie Ethanol (< 1 %) oder Pentene (< 0,1 %), die als Stabilisator künstlich zugefügt werden, um das beim Lagern an Luft und Licht entstehende Phosgen abzufangen.[5]
Eigenschaften
Trichlormethan ist eine farblose, nicht entflammbare, flüchtige Flüssigkeit von süßlichem Geruch. Der Schmelzpunkt liegt bei −63 °C. Der Siedepunkt unter Normaldruck bei 61 °C. Es hat eine größere Dichte als Wasser und ist nur wenig darin löslich.
Chloroform wird durch Sauerstoff unter Lichteinfluss photochemisch zersetzt, dabei entsteht Phosgen, Chlor und Chlorwasserstoff. Handelsübliches Chloroform enthält 0,5–1,0 % Ethanol als Stabilisator, um entstehendes Phosgen chemisch abzufangen.
Die Dämpfe von Chloroform verursachen Bewusstlosigkeit und heben die Schmerzempfindung auf. Wegen der toxischen Wirkung auf Herz, Leber und andere innere Organe wird Chloroform heute nicht mehr als Narkosemittel angewendet. Es steht außerdem unter Verdacht, krebserregend zu sein.
Verwendung
Chloroform wird in erster Linie als Lösungsmittel und zur Herstellung von Fluorchlorkohlenwasserstoffen (FCKW) verwendet.
In der chemischen Synthese wird es zur Herstellung von Dichlorcarben (in Gegenwart von Basen) verwendet. Durch Friedel-Crafts-Alkylierung mit Benzol erhält man Triphenylmethan.
Deuteriertes Chloroform (CDCl3), auch Deuterochloroform genannt, findet in der Kernresonanzspektroskopie (NMR) als Lösungsmittel Verwendung.
Bei der Bestimmung der mikrobiellen Biomasse in Bodenproben mittels Chloroform-Fumigation-Extraktion wird ausgenutzt, dass Chloroform Zelllyse verursacht.
Rechtsbestimmungen
Die Anwendung von Chloroform ist bei Lebensmittel liefernden Tieren gemäß der EU-Rückstandshöchstmengen-Verordnung für Lebensmittel tierischen Ursprungs in der Europäischen Union generell verboten.
Literatur
- Franz Hartmann: Beitrag zur Litteratur über die Wirkung des Chloroforms. Ferber, Giessen 1855 (Digitalisat der ULB Düsseldorf)
Einzelnachweise
- ↑ a b c d e f g h Eintrag zu Chloroform in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. Dezember 2007 (JavaScript erforderlich).
- ↑ Datenblatt Chloroform bei Sigma-Aldrich, abgerufen am 19. Juli 2010.
- ↑ a b Eintrag zu CAS-Nr. 67-66-3 im European chemical Substances Information System ESIS (ergänzender Eintrag)
- ↑ Schadstofflexikon.
- ↑ Sigma-Aldrich: Chloroform.
Weblinks
 Commons: Chloroform – Sammlung von Bildern, Videos und AudiodateienKategorien:
Commons: Chloroform – Sammlung von Bildern, Videos und AudiodateienKategorien:- Gesundheitsschädlicher Stoff
- Stoff mit Verdacht auf krebserzeugende Wirkung
- Digitalisierte Literatur der Universitäts- und Landesbibliothek Düsseldorf
- Chloralkan
- Anästhetikum
Wikimedia Foundation.





