- Gold(III)-oxid
-
Kristallstruktur 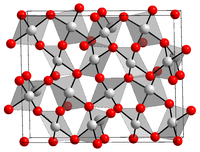
__ Au3+ __ O2− Allgemeines Name Gold(III)-oxid Verhältnisformel Au2O3 CAS-Nummer 1303-58-8 Kurzbeschreibung braunes Pulver[1]
Eigenschaften Molare Masse 441,93 g·mol−1 Aggregatzustand fest
Dichte 3,6 g·cm−3[2]
Schmelzpunkt Löslichkeit unlöslich in Wasser[2]
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung [3] 
Achtung
H- und P-Sätze H: 315-319 EUH: keine EUH-Sätze P: 305+351+338 [3] EU-Gefahrstoffkennzeichnung [2] keine Gefahrensymbole R- und S-Sätze R: keine R-Sätze S: keine S-Sätze Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Gold(III)-oxid (Au2O3) ist das stabilste bekannte Goldoxid. Es ist ein rotbrauner, kristalliner, lichtempfindlicher Feststoff. Die Verbindung ist thermisch instabil und zersetzt sich oberhalb von etwa 160 °C wieder in die Elemente. Au2O3 hat eine verzerrte quadratisch-planare Kristallstruktur, bestehend aus AuO4-Einheiten.
Inhaltsverzeichnis
Darstellung
Die Verbindung ist aufgrund des edlen Charakters des Elements nicht durch Verbrennung mit Sauerstoff herstellbar. Es ist allerdings durch die direkte Reaktion von Gold mit einem Sauerstoffplasma darstellbar. Chemisch geht man von in wässriger Lösung stabilem Trichlorogold-Hydrat AuCl3·H2O (eigentlich Hydrogentrichlorohydroxidoaurat(III) H[AuCl3(OH)]) oder der Tetrachloridogoldsäure H[AuCl4]·4 H2O aus, das, mit Natriumcarbonat versetzt, als ein brauner Niederschlag Au2O3·x H2O ausfällt. Nach dem Trocknen über Silicagel spaltet dieses Wasser ab und ergibt Au2O3·2-3 H2O. Dieses kann dann weiter beim vierwöchigem tempern bei 280°C und 3000 Bar Druck zu reinem polykristallinem und wasserfreiem Gold(III)-oxid Au2O3 umgewandelt werden.[4]
Verwendung
Goldoxid kann zum Färben von Gläsern (Goldrubinglas) verwendet werden, spezielle Anwendungen in der Optoelektronik sind auch möglich.
Einzelnachweise
- ↑ Arnold F. Holleman, Nils Wiberg: Lehrbuch der Anorganischen Chemie, 102. Auflage, de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1.
- ↑ a b c d Datenblatt Gold(III)-oxid bei AlfaAesar, abgerufen am 2. Februar 2010 (JavaScript erforderlich)..
- ↑ a b Datenblatt Gold(III) oxide hydrate bei Sigma-Aldrich, abgerufen am 3. April 2011.
- ↑ Georg Brauer: Handbuch der Präparativen Anorganischen Chemie Band II, Ferdinand Enke Verlag, Stuttgart 1978, ISBN 3-432-87813-3, S. 1090.
Weblinks
Kategorien:- Goldverbindung
- Oxid
Wikimedia Foundation.
