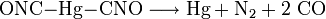- Hg(CNO)2
-
Strukturformel 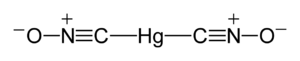
Allgemeines Name Knallquecksilber Andere Namen - Quecksilber(II)-fulminat
- Quecksilberfulminat
- Quecksilberdifulminat
Summenformel C2HgN2O2 CAS-Nummer 628-86-4 Kurzbeschreibung weiß-graues Pulver[1] Eigenschaften Molare Masse 284,62 g/mol Aggregatzustand fest
Dichte 4,42 g·cm–3[1]
Schmelzpunkt Löslichkeit wenig löslich in Wasser[1]
Sicherheitshinweise Gefahrstoffkennzeichnung aus RL 67/548/EWG, Anh. I [2] 


Explosions-
gefährlichGiftig Umwelt-
gefährlich(E) (T) (N) R- und S-Sätze R: 3-23/24/25-33-50/53 S: (1/2)-13-28-45-60-61 MAK 0,1 mg·m–3[1]
Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Knallquecksilber (chemisch: Quecksilber(II)-fulminat) ist das Quecksilbersalz der Knallsäure. Es bildet in reinster Form farblose Kristalle. Knallquecksilber ist giftig und zerfällt schon bei geringer mechanischer oder thermischer Belastung.
Inhaltsverzeichnis
Geschichte
Das Knallquecksilber wurde wahrscheinlich bereits Ende des 17. Jahrhunderts von Kunkel von Löwenstern und anderen Alchimisten erstmals isoliert. Die Herstellung aus Quecksilber, Ethanol und Salpetersäure wird erstmals 1799 von dem Engländer E. Howard beschrieben.
Knallquecksilber wurde früher in Zünd- und Sprengkapseln verwendet, ist allerdings inzwischen durch andere Stoffe ersetzt worden (z. B. Bleiazid). Alfred Nobel setzte Knallquecksilber in Sprengkapseln zur Zündung von Dynamit ein. Erst diese relativ sichere Zündmethode begründete den breiten Erfolgskurs von Dynamit-Sprengstoffen. Allein im deutschen Reich betrug die Jahresproduktion an Knallquecksilber Anfang des 20. Jahrhunderts etwa 100.000 kg.
Aufgrund seiner ausgeprägten Initiierfähigkeit war es bis zur Einführung des Bleiazids der am weitesten verbreitete Initialsprengstoff.
Gewinnung und Darstellung
Quecksilberfulminat wird durch Umsetzung von elementarem Quecksilber oder Quecksilber(II)-oxid mit konzentrierter Salpetersäure in Gegenwart von Ethanol hergestellt. Die Synthese größerer Mengen an Quecksilberfulminat erfordert strenge Sicherheitsvorkehrungen und darf nur durch ausgebildetes Fachpersonal erfolgen.
Zur Darstellung kleiner Mengen kann das 1901 von dem Italiener Angelico beschriebene Verfahren für Silberfulminat benutzt werden. Anstelle von Ethanol erfolgt die Umsetzung hier mit wässrigen Lösungen von Malonsäure und Natriumnitrit.
Verunreinigungen durch Nebenprodukte können durch ein oder mehrmaliges Umkristallisieren aus Ammoniak-Lösung beseitigt werden.
Eigenschaften
Physikalische Eigenschaften
Quecksilberfulminat ist in heißem Wasser, Ethanol und in Salpetersäure gut, in kaltem Wasser hingegen nur schlecht löslich.
Chemische Eigenschaften
Bereits bei geringer mechanischer oder thermischer Belastung zerfällt Quecksilberfulminat explosionsartig. Dabei entstehen elementares Quecksilber, Stickstoff und Kohlenstoffmonoxid:
Hierbei kann der Zerfall durch Verdämmen oder Zünden größerer Mengen leicht in eine Detonation (v = 5000 m/s) übergehen.
Da bei der Explosion eine Wolke von atomarem, giftigem Quecksilberdampf entsteht, wird es als Sprengstoff heute nicht mehr verwendet.
Kristallstruktur
Untersuchungen zum Kristallgitter des Knallquecksilber wurden bereits in der 1930er Jahren durchgeführt. Erst 2007 wurden signifikante Ergebnisse erzielt.[3] Knallquecksilber liegt demnach orthorhombisch vor. Die Hg-Atome und die zwei umgebenen C-Atomen sind − wie bereits vermutet − linear angeordnet, so dass die molekulare, gesteckte Anordnung von O-N-C-Hg-C-N-O bestätigt wird.
Sicherheitshinweise
Quecksilberfulminat ist ein Initialsprengstoff und daher besonders explosionsgefährlich. Es kann durch Zündquellen oder mechanische Einwirkung wie Reibung oder Stoß zur Explosion kommen, aber auch durch Aussetzung von Strahlung, durch Trocknen oder Kontakt mit anderen chemischen Verbindungen, wie beispielsweise Schwefelsäure.
Quecksilberfulminat ist giftig und umweltgefährlich; für Wasserorganismen stellt es ein besonders hohes Gefahrenpotential dar. Bei Umgang sind größte Vorsicht und Sorgfalt walten zu lassen und besondere Vorkehrungen zu treffen. Unter Wasser gelagert ist es nicht explosionsfähig und chemisch stabil.
Siehe auch
- Silberfulminat
- Kupferfulminat
Quellen
- ↑ a b c d e Eintrag zu Quecksilberfulminat in der GESTIS-Stoffdatenbank des BGIA, abgerufen am 20. Februar 2008 (JavaScript erforderlich)
- ↑ Eintrag zu CAS-Nr. 628-86-4 im European chemical Substances Information System ESIS
- ↑ Beck, Evers, Göbel, Oehlinger, Klapötke: The Crystal and Molecular Structure of Mercury Fulminate (Knallquecksilber). Z. anorg. allg. Chem. 2007, Bd. 633, Nr. 9, S. 1417–1422.
Literatur
- R. Knoll: Das Knallquecksilber und andere Sprengstoffe., Survival Press, Radolfz., November 2001, ISBN 3-831128766
- A. Stettbacher: Die Schieß- und Sprengstoffe. 2. Auflage, Leipzig, 1933.
Wikimedia Foundation.