- Nilotinib
-
Strukturformel 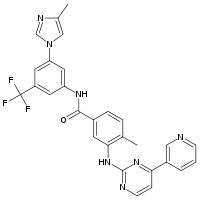
Allgemeines Freiname Nilotinib Andere Namen 4-Methyl-N-[3-(4-methylimidazol-1-yl)-5- (trifluormethyl)phenyl]-3-[(4-pyridin-3- ylpyrimidin-2-yl)amino]benzamid (IUPAC)
Summenformel C28H22F3N7O CAS-Nummer 641571-10-0 ATC-Code L01XE08
Arzneistoffangaben Wirkstoffklasse Eigenschaften Molare Masse 529,52 g·mol−1 Sicherheitshinweise Bitte beachten Sie die eingeschränkte Gültigkeit der Gefahrstoffkennzeichnung bei Arzneimitteln EU-Gefahrstoffkennzeichnung [1] Keine Einstufung verfügbarR- und S-Sätze R: siehe oben S: siehe oben Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Nilotinib, (Handelsname: Tasigna®, Hersteller: Novartis) wurde unter der Bezeichnung AMN107 entwickelt und ist ein spezifischer BCR-ABL-Tyrosinkinase-Inhibitor. Tasigna wurde erstmals Mitte 2007 in der Schweiz für die Behandlung der chronischen myeloischen Leukämie (CML) zugelassen, kurze Zeit später folgte die Zulassung in den USA und der EU. Seit dem 1. Januar 2008 ist das verschreibungspflichtige Arzneimittel in Deutschland zur Behandlung der CML erhältlich.
Die Zulassung erfolgte für Patienten, die eine Behandlung mit Imatinib nicht tolerieren oder nicht darauf ansprechen. Grundlage der Zulassung waren große Phase III-Therapiestudien, in denen Nilotinib auch bei Imatinib-resistenten CML-Patienten Wirksamkeit gezeigt hatte.[2]
Einzelnachweise
- ↑ In Bezug auf ihre Gefährlichkeit wurde die Substanz von der EU noch nicht eingestuft, eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ Kantarjian H et al.: Nilotinib in imatinib-resistant CML and Philadelphia chromosome-positive ALL. N Engl J Med 2006;354:2542-51. PMID 16775235
Weblinks
- [1] Nilotinib in der EU zugelassen, Leukämie-Online vom 28. November 2007
- Europäischer öffentlicher Beurteilungsbericht (EPAR) und Produktinformation zu Tasigna auf der Website der Europäischen Arzneimittelagentur

Bitte den Hinweis zu Gesundheitsthemen beachten!
Wikimedia Foundation.
