- 6-Hydroxyuracil
-
Strukturformel 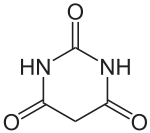
Allgemeines Name Barbitursäure Andere Namen - 2,4,6(1H,3H,5H)-Pyrimidintrion
- 2,4,6-Trihydroxypyrimidin
- 6-Hydroxyuracil
- N,N'-Malonylharnstoff
Summenformel C4H4N2O3 CAS-Nummer 67-52-7 Kurzbeschreibung farbloses, kristallines Pulver mit schwachem Geruch [1] Eigenschaften Molare Masse 128,09 g/mol Aggregatzustand fest
Schmelzpunkt Löslichkeit leicht löslich in Wasser (142 g·l−1 bei 20°C) [1]
Sicherheitshinweise Gefahrstoffkennzeichnung [1] keine Gefahrensymbole R- und S-Sätze R: keine R-Sätze S: keine S-Sätze LD50 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Barbitursäure ist Pyrimidin-Derivat, das als Ausgangssubstanz zur Herstellung der Barbiturate und in der Analytik Verwendung findet.
Inhaltsverzeichnis
Geschichte
Barbitursäure wurde erstmalig von Adolf von Baeyer im Jahre 1864 durch Kondensation von Harnstoff mit Malonsäure zum entsprechenden Dilactam synthetisiert. Er benannte seine Entdeckung nach seiner Geliebten Barbara.[3]
Verwendung
Barbitursäure ist selbst nicht sedativ-hypnotisch wirksam. Erst in Verbindung mit anderen Substanzen besitzt sie eine hypnotische Wirkung (siehe Barbiturat). Als erstes Barbiturat mit hypnotischer Wirkung wurde 1903 Diethylbarbiturat (Barbital) durch Fischer und von Mering dargestellt.
In der Trink- und Abwasseranalytik wird Barbitursäure als Reagenz zur kolorimetrischen Cyanidanalyse (CN–-Ion) verwendet.
Quellen
- ↑ a b c d Eintrag zu Barbitursäure in der GESTIS-Stoffdatenbank des BGIA, abgerufen am 21.06.2007 (JavaScript erforderlich)
- ↑ Barbitursäure bei ChemIDplus
- ↑ Werner E. Gerabek, Bernhard D. Haage, Gundolf Keil, Wolfgang Wegner: Enzyklopädie Medizingeschichte [1], De Gruyter Verlag, 1. Auflage 2004, S. 138, ISBN 3-110-15714-4
Weblinks
Wikimedia Foundation.
