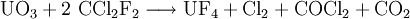- Urantetrafluorid
-
Kristallstruktur 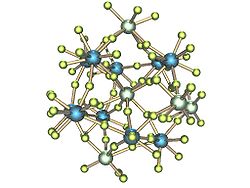
Kristallsystem monoklin Raumgruppe 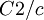
Gitterkonstanten a = pm
b = pm
c = pmAllgemeines Name Uran(IV)-fluorid Andere Namen Urantetrafluorid
Verhältnisformel UF4 CAS-Nummer 10049-14-6 PubChem 61461 Kurzbeschreibung grüne Kristalle[1] Eigenschaften Molare Masse 314,02 g/mol Aggregatzustand fest
Dichte 6,7 g/cm3[1]
Schmelzpunkt 1036 °C[1]
Siedepunkt 1417 °C[1]
Sicherheitshinweise Gefahrstoffkennzeichnung aus RL 67/548/EWG, Anh. I [2] 

Sehr giftig Umwelt-
gefährlich(T+) (N) R- und S-Sätze R: 26/28-33-51/53 S: (1/2)-20/21-45-61 Radioaktivität 
RadioaktivSoweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Uran(IV)-fluorid (UF4) ist ein grüner kristalliner Feststoff mit einem geringen Dampfdruck und einer guten Löslichkeit in Wasser. Uran spielt in seinem vierwertigen Zustand eine Rolle in verschiedenen technologischen Prozessen. Es ist als „green salt“ bekannt.
Inhaltsverzeichnis
Eigenschaften
UF4 ist in der Regel ein Zwischenprodukt bei der Umwandlung von Uranhexafluorid (UF6) sowohl zu den Uranoxiden (U3O8 oder UO2) als auch zum Uranmetall. Es wird gebildet durch Reaktion von UF6 mit Wasserstoffgas oder durch Einwirkung von HF auf Urandioxid (UO2). UF4 hydrolysiert allmählich bei Feuchtigkeit zu UO2 und HF. Aufgrund dieses Verhaltens und den korrosiven Eigenschaften des sich bildenden HF ist es für eine Langzeitaufbewahrung eher nicht geeignet.[3][4]
Synthese
Sehr reines Uran(IV)-fluorid kann durch Überleiten von trockenem Dichlordifluormethan (Freon 12) über 400 °C heißes Uran(VI)-oxid erhalten werden.[5]
Sicherheitshinweise
UF4 ist hochtoxisch beim Einatmen und Verschlucken. Außerdem besteht die Gefahr der Anreicherung im menschlichen Körper, was vor allem die Leber und die Nieren betrifft. Für Wasserorganismen ist es ebenfalls giftig und kann Langzeitschäden in der Wasserwelt verursachen. Wie alle Uranverbindungen ist es radioaktiv. Die Aktivität ist von der Isotopenzusammensetzung des Urans abhängig.
Einzelnachweise
- ↑ a b c d Uran(IV)-fluorid bei www.webelements.com.
- ↑ Nicht explizit in RL 67/548/EWG, Anh. I gelistet, fällt aber dort mit der angegebenen Kennzeichnung unter den Sammelbegriff „Uranverbindungen“; Eintrag in der GESTIS-Stoffdatenbank des BGIA, abgerufen am 30. März 2009 (JavaScript erforderlich)
- ↑ H. S. Booth, W. Krasny-Ergen, R. E. Heath: Uranium Tetrafluoride. In: Journal of the American Chemical Society. 68, 1946, S. 1969–1970. doi:10.1021/ja01214a028.
- ↑ S. Kern, J. Hayward, S. Roberts, J. W. Richardson, F. J. Rotella, L. Soderholm, B. Cort, M. Tinkle, M. West, D. Hoisington, G. H. Lander: Temperature variation of the structural parameters in actinide tetrafluorides. In: Journal of Chemical Physics. 101, 1994, S. 9333–9337. doi:10.1063/1.467963.
- ↑ G. Brauer (Hrsg.), Handbook of Preparative Inorganic Chemistry 2nd ed., vol. 1, Academic Press 1963, S. 261–262.
Literatur
- Arnold F. Holleman, Nils Wiberg: Lehrbuch der Anorganischen Chemie, 102. Auflage, de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1.
- Norman N. Greenwood, Alan Earnshaw: Chemie der Elemente, 1. Auflage, Wiley-VCH, Weinheim 1988, ISBN 3-527-26169-9.
Weblinks
Wikimedia Foundation.