- Uranylhydroxid
-
Kristallstruktur 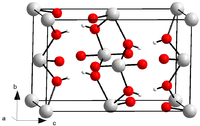
__ U6+ __ O2− Allgemeines Name Uranylhydroxid Verhältnisformel UO2(OH)2 CAS-Nummer 211573-15-8 Kurzbeschreibung grüngelber, fluoreszierender Feststoff
Eigenschaften Molare Masse 304,04 g·mol−1 Aggregatzustand fest
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung aus RL 67/548/EWG, Anh. I [1] 


Gefahr
H- und P-Sätze H: 330-300-373-411 EUH: keine EUH-Sätze P: ? EU-Gefahrstoffkennzeichnung aus RL 67/548/EWG, Anh. I [1] 

Sehr giftig Umwelt-
gefährlich(T+) (N) R- und S-Sätze R: 26/28-33-51/53 S: (1/2)-20/21-45-61 Radioaktivität 
RadioaktivSoweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Uranylhydroxid ist ein Hydroxid des Urans mit der chemischen Formel UO2(OH)2 in der monomeren und (UO2)2(OH)4 in der dimeren Form. Beide Isomere können im normalen wässrigen Medium existieren. Uranylhydroxidhydrat wird als ein gallertartiger Yellowcake aus oxidierten Uranlaugen bei etwa neutralem pH-Wert ausgefällt.
Inhaltsverzeichnis
Eigenschaften
Uranylhydroxid leitet sich wie die Uranate von der hypothetischen Uransäure ab, die sowohl als Base wie auch als Säure reagieren kann. Als Base werden die Uranyl-Verbindungen und als Säure die Uranate gebildet. Letztere sind jedoch nicht stabil und wandeln sich in die Di-uranate (U2O72−) um. Die entsprechenden Reaktionsgleichungen sind wie folgt:[2]
Auf Grund dieser Reaktionen können Uranate und Uranylsalze leicht in die jeweils andere Form umgewandelt werden.
Verwendung
Uranylhydroxid wurde früher in der Glas- und Keramikherstellung genutzt, um die Glasphasen einzufärben und Pigmente für das Hochtemperaturbrennen herzustellen. Durch Einleitung von alkalischen Diuranaten in Glas entsteht ein Gelbton im Glas und eine grüne Reflexion. Außerdem strahlt dieses Glas unter ultraviolettem Licht Kaltlicht ab und fluoresziert. Das Uranylhydroxid leitet Protonen, wenn es stetig stärker zusammengepresst wird und anschließend langsam wieder entspannt wird; und es findet Anwendung als Bauteil von Brennstoffzellen.[3]
Auswirkungen auf die Gesundheit
Uranylhydroxid schädigt das Erbgut, führt zu Fehlbildungen und ist radioaktiv; daher sollte es mit äußerster Vorsicht behandelt werden.
Einzelnachweise
- ↑ a b Nicht explizit in RL 67/548/EWG, Anh. I gelistet, fällt aber dort mit der angegebenen Kennzeichnung unter den Sammelbegriff „Uranverbindungen“; Eintrag in der GESTIS-Stoffdatenbank des IFA, abgerufen am 25. April 2011 (JavaScript erforderlich)
- ↑ Hollemann-Wiberg: Lehrbuch der anorganischen Chemie, 37–39. Auflage, Walter de Gruyter&Co, 1956, S. 519.
- ↑ United States Patent 4179491: Electrical device with separator as conductor for hydrogen cations.
Literatur
- Ingmar Grenthe, Janusz Drożdżynński, Takeo Fujino, Edgar C. Buck, Thomas E. Albrecht-Schmitt, Stephen F. Wolf: Uranium, in: Lester R. Morss, Norman M. Edelstein, Jean Fuger (Hrsg.): The Chemistry of the Actinide and Transactinide Elements, Springer, Dordrecht 2006; ISBN 1-4020-3555-1, S. 253–698; doi:10.1007/1-4020-3598-5_5.
- C. A. Alexander: „Volatilization of urania under strongly oxidizing conditions“, in: Journal of Nuclear Materials, 2005, 346, S. 312–318; doi:10.1016/j.jnucmat.2005.07.013.
Kategorien:- Giftiger Stoff
- Umweltgefährlicher Stoff
- Radioaktiver Stoff
- Hydroxid
- Uranylverbindung
Wikimedia Foundation.

