- Bootskonformation
-
Die Konformation eines organischen Moleküls beschreibt die räumliche Anordnung dessen drehbarer Bindungen an den Kohlenstoffatomen. Durch sie sind die dreidimensionalen Raumkoordinaten aller Atome des Moleküls vollständig beschrieben.
Die Konformation enthält damit auch die Information über die Stereochemie, also die Konfiguration, aller stereotopen Atome und über die Konstitution des Moleküls.
Moleküle mit gleicher Konfiguration, die sich jedoch in der spezifischen Anordnung der Atome unterscheiden, und in einem Energieminimum liegen bezeichnet man als Konformere. Synonym dazu ist auch die Bezeichnung Rotamer gebräuchlich.
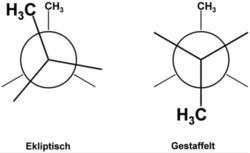
Als Beispiel seien zwei Konformere des Butans in der folgenden Newman-Projektion gezeigt. Der Winkel, den die beiden Methylgruppen miteinander ausbilden, wird als Diederwinkel bezeichnet.
Liegen verschiedene Konformere im Gleichgewicht miteinander vor, ist das Mengenverhältnis durch eine Boltzmann-Statistik gegeben.
Inhaltsverzeichnis
Konformationen bei cyclischen Molekülen
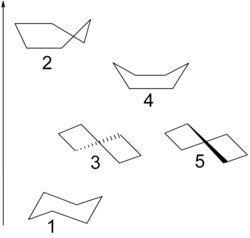
Cycloalkane können oft in unterschiedlichen Konformationen vorkommen, die durch eine signifikante Energiebarriere voneinander getrennt sind, so dass die Konformere nebeneinander nachweisbar sind.
Die Twist-, die Wannen- und die Sesselkonformation sind Konformationen von cyclischen Molekülen wie Cyclohexan. Im Vergleich zur Wannenkonformation oder auch Bootskonformation ist die Twistkonformation leicht verdreht. Dadurch werden die Wechselwirkungen zwischen den beiden H-Atomen, die an den beiden Wannenspitzen sitzen schwächer und die Pitzer-Spannung kleiner (die H-Atome stehen nicht genau ekliptisch). Die Baeyer-Spannung wird zwar durch das leichte Verdrehen des Rings geringfügig größer, doch gleicht dies die dafür wegfallende Van-der-Waals-Abstoßung zwischen den beiden an den Wannenspitzen sitzenden H-Atomen aus. Die Twistkonfomation ist darum um etwa 1,4 kcal/mol stabiler als die Wannenform und stellt wie die Sesselform ein Konformer dar. Da die Wannenform ebenfalls energiereicher ist als die Sesselkonformation, treten Verbindungen wie Cyclohexan fast ausschließlich in der nahezu spannungsfreien Sesselkonformation auf. Weil es möglich ist, das Molekül in zwei Richtungen zu verdrehen, gibt es zwei energetisch gleichwertige Twistkonformationen.
Ring-Flip
Der Ring-Flip ist ein Phänomen, bei dem durch Rotation um Einfachbindungen eine Umwandlung cyclischer Konformere gleicher Ringformen stattfindet. Die räumlichen Positionen der Substituenten müssen dabei nicht unbedingt gleich bleiben.
Cyclohexan ist die prominenteste Verbindung, bei der der Ring-Flip zu beobachten ist. Die Vorzugskonformation dieses sechsgliedrigen Ring-Alkans ist die Sesselkonformation. Entgegen den Erwartungen zeigt das 1H-NMR-Spektrum von Cyclohexan keine zwei Signale bei verschiedenen Resonanzfrequenzen für axiale und äquatoriale Wasserstoffatome, die sich in leicht unterschiedlichen chemischen Umgebungen befinden. Der ekliptische Übergangszustand, der bei der Konformationsumwandlung durchlaufen wird, ist energetisch wenig angehoben, sodass die Isomerisierung bei Raumtemperatur schnell stattfindet und nur ein Signal beobachtet werden kann. Dies ändert sich, wenn die Temperatur so stark erniedrigt wird, dass aufgrund der Energiebarriere der Isomerisierung die Umwandlung viel langsamer stattfindet. Beim Ring-Flip von Cyclohexan werden alle axialen Substituenten zu äquatorialen und alle äquatorialen zu axialen.
Der Ring-Flip von Cyclohexan beginnt mit dem Übergang von der Sessel- über die Halbsessel- zur Twist-Konformation, wobei das Energiemaximum bei der Halbsessel-Konformation liegt. Die Boot-Konfiguration wandelt sich die Twist-Konformation in die spiegelbildliche Twist-Konformation um, wobei die Boot-Konformation das Energiemaximum darstellt. Über einen weiteren Halbsessel wird die Sessel-Konformation nach Ring-Flip erreicht.
Verschiedene Substituenten verhindern das Auftreten des Ring-Flip, zum Beispiel ein zweiter angefügter Ring wie im trans-Decalin. Auch acyclische Substituenten können diesen Effekt haben. Die tert-Butylgruppe im tert-Butylcyclohexan lässt nur eine Konformation zu, man bezeichnet sie als Konformationsanker. Aufgrund ihres großen sterischen Anspruches verursacht sie in axialer Position weitaus größere 1,3-diaxiale Spannung als die drei Wasserstoff-Substituenten, wenn sie äquatorial steht. Die „Unterseite“ ändert sich beim Ring-Flip von tert-Butylcyclohexan nicht.
In der Biologie
Die Konformation in der Biologie beschreibt die Veränderung der Tertiärstruktur eines Proteins zum Transport eines Stoffes über eine Membran (Meistenteils entgegen einem Konzentrationsgefälle). Man unterscheidet diesen Transport in zwei Möglichkeiten: 1. Die Konformation des sogenannten "Carrierproteins" durch den zu transportierenden Stoff und 2. durch ein weiteres Molekül (vgl.: Membrantransport).
Quellen
- Clayden, J. Greeves, N. Warren, S. Wothers, P. (2001). Organic Chemistry. Oxford. ISBN 0-19-850346-6
- Conformations of Alkanes & Cycloalkanes
Siehe auch
Wikimedia Foundation.