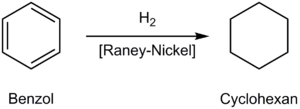
- Cyclohexan
-
Strukturformel 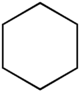
Allgemeines Name Cyclohexan Andere Namen - Hexahydrobenzol
- Hexamethylen
- Naphthen
Summenformel C6H12 CAS-Nummer 110-82-7 Kurzbeschreibung charakteristisch riechende, farblose Flüssigkeit[1]
Eigenschaften Molare Masse 84,16 g·mol−1 Aggregatzustand flüssig
Dichte 0,78 g·cm−3 [1]
Schmelzpunkt Siedepunkt 81 °C [1]
Dampfdruck Löslichkeit unlöslich in Wasser (50 mg·l−1 bei 20 °C)[1]
Brechungsindex 1,42623[2]
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung aus EU-Verordnung (EG) 1272/2008 (CLP) [3] 



Gefahr
H- und P-Sätze H: 225-304-315-336-410 EUH: keine EUH-Sätze P: 210-240-273-301+310-331-403+235 [1] EU-Gefahrstoffkennzeichnung aus RL 67/548/EWG, Anh. I [3] 


Leicht-
entzündlichGesundheits-
schädlichUmwelt-
gefährlich(F) (Xn) (N) R- und S-Sätze R: 11-38-65-67-50/53 S: (2)-9-16-25-33-51-60-61-62 MAK 200 ml·m−3, 700 mg·m−3 [1]
LD50 12705 mg·kg−1 (Ratte, oral) [4]
Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C Cyclohexan (auch Hexahydrobenzol, Hexamethylen, Naphthen) ist eine farblose Flüssigkeit. Es ist ein Cycloalkan mit der Summenformel C6H12, das im Erdöl vorkommt und als Lösungsmittel und Grundstoff in der Synthese genutzt wird.
Inhaltsverzeichnis
Gewinnung und Darstellung
Cyclohexan wird hauptsächlich durch Hydrierung von Benzol gewonnen, es kann aber auch aus Erdöl isoliert werden. Die USA sind Haupthersteller von Cyclohexan, jährlich werden in den USA etwa eine Million Tonnen Cyclohexan produziert, dies entspricht etwa 34 Prozent der weltweiten Produktion. Die Gesamtproduktion von Cyclohexan in Europa beträgt jährlich zwischen 835.000 und 925.000 Tonnen.
Eigenschaften
Cyclohexan schmilzt bei 6,5 °C und siedet unter Normaldruck bei 80,7 °C. Es riecht benzinartig, die Geruchsschwelle liegt bei 1,4 bis 88 mg·m−3, die Flüssigkeit ist leicht flüchtig. In Wasser ist Cyclohexan unlöslich, in organischen Stoffen, wie den Alkoholen, Kohlenwasserstoffen, Ethern oder Chlorkohlenwasserstoffen ist es gut löslich, Cyclohexan selbst ist ein Lösungsmittel für viele organische Stoffe. Die Oktanzahl des Cyclohexans ist 77. Cyclohexan ist leichtentzündlich und wassergefährdend.
Konformationen
Cyclohexan kann in drei Konformationen, der Sessel-, Twist- und Wannenkonformation vorliegen. Die energetisch günstigste Konformation ist die Sesselkonformation (1). Es existieren zwei Sesselkonformationen, die miteinander im Gleichgewicht stehen. Beim Wechsel von der einen Sesselkonformation zur anderen werden aus axialen, auf der Ringebene senkrecht stehenden Wasserstoffatomen, äquatoriale, das heißt zur Seite stehende Wasserstoffatome und umgekehrt. Die zwei Twistkonformationen (3, 5) sind jeweils die Übergangsformen von den Sessel- zur Wannenkonformation (4) und liegen energetisch zwischen Sessel- und Wannenkonformation. 99 Prozent der Cyclohexanmoleküle liegen in der Sesselkonformation vor, da diese energetisch am günstigsten ist, die Konformationen lassen sich aufgrund ihres nur geringen Energieunterschieds nicht voneinander trennen.
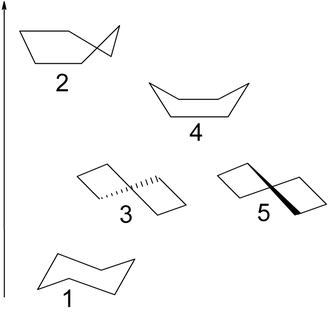 Konformationen des Cyclohexans
Konformationen des Cyclohexans
Thermodynamische Eigenschaften
Die Dampfdruckfunktion ergibt sich nach Antoine entsprechend log10(P) = A−(B/(T+C)) (P in bar, T in K) mit A = 3,99200, B = 1216,930 und C = −48.621 im Temperaturbereich von 303 K bis 343 K.[5]
Zusammenstellung der wichtigsten thermodynamischen Eigenschaften Eigenschaft Typ Wert [Einheit] Bemerkungen Standardbildungsenthalpie ΔfH0liquid
ΔfH0gas−156,2 kJ·mol−1[6]
−123,1 kJ·mol−1 [6]als Flüssigkeit
als GasVerbrennungsenthalpie ΔcH0liquid −3919,6 kJ·mol−1[7] als Flüssigkeit Wärmekapazität cp 156,9 J·mol−1·K−1 (25 °C)[8] als Flüssigkeit Kritische Temperatur Tc 553,8 K[9] Kritischer Druck pc 40,8 bar[9] Kritisches Volumen Vc 0,308 l·mol-1[9] Kritische Dichte ρc 3,24 mol·l-1[9] Azentrischer Faktor ωc 0,20805[10] Schmelzenthalpie ΔfH0 2,68 kJ·mol−1[11] beim Schmelzpunkt Verdampfungsenthalpie ΔVH0 29,97 kJ·mol−1[12] beim Normaldrucksiedepunkt Die Temperaturabhängigkeit der Verdampfungsenthalpie lässt sich entsprechend der Gleichung ΔVH0=Aexp(−αTr)(1−Tr)β (ΔVH0 in kJ/mol, Tr =(T/Tc) reduzierte Temperatur) mit A = 43,42 kJ/mol, α = −0,1437, β = 0,4512 und Tc = 553,4K im Temperaturbereich zwischen 298 K und 380 K beschreiben. [12]
-
Dampfdruckfunktion von Cyclohexan
-
Temperaturabhängigkeit der Verdampfungswärme von Cyclohexan
Sicherheitstechnische Kenngrößen
Cyclohexan bildet leicht entzündliche Dampf-Luft-Gemische. Die Verbindung hat einen Flammpunkt von −18 °C. Der Explosionsbereich liegt zwischen 1,0 Vol% (35 g/m3) als untere Explosionsgrenze (UEG) und 9,3 Vol% (326 g/m3) als obere Explosionsgrenze (OEG).[13] Die Explosionsgrenzen sind druckabhängig. Eine Erniedrigung des Druckes führt zu einer Verkleinerung des Explosionsbereiches. Die untere Explosionsgrenze ändert sich bis zu einem Druck von 100 mbar nur wenig und steigt erst bei Drücken kleiner als 100 mbar an. Die obere Explosionsgrenze verringert sich mit sinkendem Druck analog.[14]
Explosionsgrenzen unter reduziertem Druck (gemessen bei 100 °C)[14] Druck in mbar 1013 800 600 400 300 250 200 150 100 50 25 Untere Explosionsgrenze (UEG) in Vol% 0,9 0,9 0,9 1,0 1,0 1,1 1,1 1,1 1,3 1,7 3,3 in g·m−3 31 32 32 34 35 37 39 40 45 60 116 Obere Explosionsgrenze (OEG) in Vol% 9,3 8,8 8,4 8,0 7,8 7,6 7,5 7,5 7,4 6,2 4,0 in g·m−3 325 307 293 281 272 266 263 262 258 218 140 Der maximale Explosionsdruck sowie die Sauerstoffgrenzkonzentration sind druck- und temperaturabhängig.[14] Die Grenzspaltweite wurde mit 0,94 mm bestimmt.[13] Es resultiert damit eine Zuordnung in die Explosionsgruppe IIA.[13] Die Zündtemperatur beträgt 260 °C.[13] Der Stoff fällt somit in die Temperaturklasse T3. Die elektrische Leitfähigkeit ist mit 4,0·10-15 S·m-1 sehr gering.[15]
Sauerstoffgrenzkonzentration und maximaler Explosionsdruck unter reduziertem Druck (gemessen bei 20 °C und 100 °C)[14] Druck in mbar 1013 600 400 300 200 150 100 Sauerstoffgrenzkonzentration (SGK) in Vol % 20 °C 9,3 9,3 10,0 10,5 14,0 100 °C 8,5 8,4 9,0 9,4 10,5 Maximaler Explosionsdruck (pmax) in bar 20 °C 9,5 5,5 3,6 1,8 1,3 0,9 100 °C 7,6 4,6 3,1 1,5 0,8 Verwendung
Cyclohexan wird zur Produktion von Kunstfasern wie Nylon verwendet.[16] Außerdem wird es als Lösungsmittel eingesetzt. Cyclohexan kommt im Erdöl vor, es ist wichtiger Ausgangsstoff für organische Synthesen. Ungefähr 39 Prozent des hergestellten Cyclohexans werden in Europa verbraucht, Europa ist der größte Abnehmer für Cyclohexan.
Gesundheitsgefahren
Inhalation und Verschlucken der Flüssigkeit führen zu Kopfschmerzen, Übelkeit und Schwindel. Die Augen und die Haut werden gerötet und es kommt zu einer Reizung der Atemwege. Eine Langzeitexposition gegenüber Cyclohexan kann zu Dermatitis führen, einer entzündlichen Reaktion der Haut.
Einzelnachweise
- ↑ a b c d e f g h Eintrag zu CAS-Nr. 110-82-7 in der GESTIS-Stoffdatenbank des IFA, abgerufen am 18. Juni. 2008 (JavaScript erforderlich).
- ↑ CRC Handbook of Tables for Organic Compound Identification, Third Edition, 1984, ISBN 0-8493-0303-6.
- ↑ a b Eintrag zu CAS-Nr. 110-82-7 im European chemical Substances Information System ESIS (ergänzender Eintrag)
- ↑ Cyclohexan bei ChemIDplus.
- ↑ W. J. Gaw, F. L. Swinton: Thermodynamic Properties of Binary Systems Containing Hexafluorobenzene. Part 3. Excess Gibbs Free Energy of the System Hexafluorobenzene + Cyclohexane, in: Trans. Faraday Soc., 1968, 64, S. 637–647.
- ↑ a b Prosen, E.J.; Johnson, W.H.; Rossini, F.D.: Heats of formation and combustion of the normal alkylcyclopentanes and cyclohexanes and the increment per CH2 group for several homologous series of hydrocarbons in J. Res. NBS 37 (1946) 51-56.
- ↑ Moore, G.E.; Renquist, M.L.; Parks, G.S.: Thermal data on organic compounds. XX. Modern combustion data for two methylnonanes, methyl ethyl ketone, thiophene and six cycloparaffins in J. Am. Chem. Soc. 62 (1940) 1505-1507.
- ↑ Lainez, A.; Rodrigo, M.M.; Wilhelm, E.; Grolier, J.-P.E.: Excess volumes and excess heaat capacitiies of some mixtures with trans,trans,cis-1,5,9-cyclododecatriene at 298.15K in J. Chem. Eng. Data 34 (1989) 332-335.
- ↑ a b c d Daubert, T.E.: Vapor-Liquid Critical Properties of Elements and Compounds. 5. Branched Alkanes and Cycloalkanes in J. Chem. Eng. Data 41 (1996) 365-372.
- ↑ Schmidt, J.: Auslegung von Sicherheitsventilen für Mehrzweckanlagen nach ISO 4126-10 in Chem. Ing. Techn. 83 (2011) 796–812, doi:10.1002/cite.201000202.
- ↑ E. S. Domalski, E. D. Hearing: Heat Capacities and Entropies of Organic Compounds in the Condensed Phase. Volume III, in : J. Phys. Chem. Ref. Data, 1996, 25, S. 1–525; doi:10.1063/1.555985.
- ↑ a b Majer, V.; Svoboda, V., Enthalpies of Vaporization of Organic Compounds: A Critical Review and Data Compilation, Blackwell Scientific Publications, Oxford, 1985, S. 300.
- ↑ a b c d E. Brandes, W. Möller: Sicherheitstechnische Kenndaten – Band 1: Brennbare Flüssigkeiten und Gase, Wirtschaftsverlag NW – Verlag für neue Wissenschaft GmbH, Bremerhaven 2003.
- ↑ a b c d Pawel, D.; Brandes, E.: Abschlussbericht zum Forschungsvorhaben Abhängigkeit sicherheitstechnischer Kenngrößen vom Druck unterhalb des atmosphärischen Druckes, Physikalisch-Technische Bundesanstalt (PTB), Braunschweig, 1998. http://www.ptb.de/de/org/3/34/341/bericht_vakuum2.pdf
- ↑ Technische Regel für Betriebssicherheit - TRBS 2153, BG RCI Merkblatt T033 Vermeidung von Zündgefahren infolge elektrostatischer Aufladungen, Stand April 2009, Jedermann-Verlag Heidelberg.
- ↑ Bertram Philipp, Peter Stevens: Grundzüge der Industriellen Chemie, VCH Verlagsgesellschaft mbH, 1987, S. 179, ISBN 3-527-25991-0.
Weblinks
 Wiktionary: Cyclohexan – Bedeutungserklärungen, Wortherkunft, Synonyme, Übersetzungen
Wiktionary: Cyclohexan – Bedeutungserklärungen, Wortherkunft, Synonyme, Übersetzungen Commons: Cyclohexan – Sammlung von Bildern, Videos und AudiodateienKategorien:
Commons: Cyclohexan – Sammlung von Bildern, Videos und AudiodateienKategorien:- Feuergefährlicher Stoff
- Umweltgefährlicher Stoff
- Cyclohexan
Wikimedia Foundation.