- Cholesterinester-Transferprotein
-
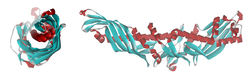
Cholesterinester-Transferprotein Bändermodell von CETP von zwei Seiten gesehen, nach PDB 2OBD Masse/Länge Primärstruktur 476 Aminosäuren Isoformen 2 Bezeichner Gen-Name CETP Externe IDs OMIM: 118470 UniProt: P11597 Transporter-Klassifikation TCDB 1.C.40.1.4 Bezeichnung BPIP-Familie Vorkommen Homologie-Familie BPI/LBP Übergeordnetes Taxon Wirbeltiere Das Cholesterinester-Transferprotein (CETP) ist eines von mehreren Proteinen, die in Wirbeltieren den Cholesterintransport zwischen unterschiedlichen Lipoprotein-Fraktionen bewerkstelligen.
Biochemisch gesehen ist CETP ein porenbildendes Protein. Beim Menschen wird es primär von der Leber gebildet und dort ins Blut abgegeben. Im Blut zirkuliert es hauptsächlich an HDL gebunden. Mutationen im CETP-Gen sind Ursache für eine seltene Erbkrankheit mit erhöhten HDL-Werten.[1][2]
Inhaltsverzeichnis
Wirkmechanismus von CETP
CETP ist ein Transferprotein, das Neutralfette (Triglyceride und Cholesterylester) von einem Donorpartikel aufnimmt, sie durch die wässrige Phase trägt und an Lipoprotein-Akzeptoren übergibt. Es ist beteiligt am reversen Cholesterintransport, also am Rücktransport von Cholesterin aus der Peripherie zur Leber. Konkret ist CETP in den sogenannten indirekten Cholesterintransport zur Leber involviert: Das CETP vermittelt hier die Übertragung der Cholesterinester von High Density Lipoproteinen (HDL) auf Low Density Lipoproteine (LDL) oder Very Low Density Lipoproteine (VLDL). Diese transportieren Cholesterin nicht nur in die Peripherie, sondern sie werden zu einem geringen Anteil auch von den Leberzellen aufgenommen, die das Cholesterin schließlich in Form von Gallensäure ausscheiden. Am direkten Transport des Cholesterins zur Leber ist CETP hingegen nicht beteiligt. Hier gibt HDL das Cholesterin direkt an die Hepatozyten ab.
Bei Normtriglyceridämie, also bei normalem Triglyceridspiegel im Blut, werden Cholesterylester im Austausch gegen Triglyceride von High Density Lipoproteinen (HDL) auf Low Density Lipoproteine (LDL) oder Very Low Density Lipoproteinen (VLDL) übertragen. CETP ist außerdem am Cholesterintransport zwischen unterschiedlichen HDL-Fraktionen beteiligt.[1][2][3][4]
CETP und Atherosklerose
Die Wechselwirkung zwischen CETP-Aktivität und der Entstehung atherosklerotischer Gefäßveränderungen ist komplex. Die Hauptfunktion von CETP im menschlichen Organismus ist der Cholesterintransport von den anti-atherogenen HDL in Richtung der pro-atherogenen LDL. Deshalb wirkt CETP tendenziell atherosklerosefördernd. Aus der Evolutionsperspektive betrachtet dürfte sich CETP als ein Werkzeug entwickelt haben, mit dem lebensnotwendiges Cholesterin im Körper zurückgehalten wird. Unter den veränderten Ernährungsbedingungen der Gegenwart steht jetzt der pro-atherogene Effekt im Vordergrund.
CETP-Hemmung
Das CETP kann pharmakologisch durch so genannte CETP-Inhibitoren gehemmt werden. Die CETP-Inhibition bewirkt unter anderem:
- eine Erhöhung der HDL-Konzentration[1][2]
- eine Erhöhung der Konzentration an Apolipoprotein A1[1][2] sowie des ApoA-1-Spiegels[5]
- eine Erhöhung der Gesamt-HDL-Partikelzahl[6]
- eine Erhöhung der HDL-Partikelgröße[1]
- eine Reduktion der LDL-Konzentration[2]
- eine Erhöhung der LDL-Partikelgröße[2]
- eine Reduktion des Cholesteringehalts von Chylomikronen und VLDL[1]
Insbesondere durch ihren Effekt auf die HDL-Fraktion mit Erhöhung von HDL-Partikelzahl und HDL-Konzentration hat die CETP-Inhibition ein anti-atherogenes Potenzial. Erhöhte HDL-C-Spiegel im Blut waren unter anderem in der Framingham-Studie[7] und in der TNT-Studie[8] mit einer niedrigeren kardiovaskulären Ereignisrate assoziiert. Bekannt ist außerdem, dass ein CETP-Mangel im Menschen mit einem deutlichen Anstieg des HDL-Cholesterins einhergeht.[2] Schließlich führte die CETP-Inhibition in Tiermodellen konsistent zu einer Hemmung der Atherosklerose.[2] Unter anderem aus diesen Gründen gilt die CETP-Inhibition als ein vielversprechender Ansatz zur Therapie bei Dyslipidämie beziehungsweise eine mögliche Behandlungsoption zur Verringerung des mit einer Fettstoffwechselstörung einhergehenden erhöhten kardiovaskulären Risikos.
CETP-Inhibitoren
CETP-Inhibitoren sind pharmakologische Substanzen, die das CETP hemmen. Es handelt sich um eine heterogene Substanzklasse, die Wirkstoffe unterschiedlicher biochemischer Struktur, unterschiedlicher physikochemischer Eigenschaften und mit unterschiedlichen Wirkmechanismen umfasst. In klinischer Entwicklung befanden oder befinden sich unter anderem die CETP-Inhibitoren Torcetrapib, Anacetrapib und Dalcetrapib. Während der ältere CETP-Inhibitor Torcetrapib die Erwartungen nicht erfüllen konnte, zeigten neuere CETP-Inhibitoren wie Anacetrapib und Dalcetrapib in Phase II-Studien neben einer günstigen Beeinflussung des Lipoproteinprofils ein günstiges Nebenwirkungsprofil.[9][10] Auf Grund der komplexen Zusammenhänge der CETP-Wirkung bzw. –Hemmung ist die Erhöhung des HDL-Cholesterins alleine noch kein ausreichender Marker für den klinischen Nutzen. Entscheidend im Hinblick auf einen möglichen therapeutischen Nutzen ist, ob die Substanzen in klinischen Studien eine Reduktion kardiovaskulärer Ereignisse nachweisen können.
Torcetrapib
Die Bindung von Torcetrapib an CETP führt zur Ausbildung eines hoch-affinen Komplexes aus Torcetrapib, CETP und HDL.[11][12] Der Effekt der Substanz auf kardiovaskuläre Ereignisse wurde in der Phase III-Studie ILLUMINATE bei Patienten mit Herz-Kreislauf-Erkrankungen untersucht. Es kam zu einem statistisch signifikanten Anstieg der HDL-C-Level um 72 Prozent. Trotzdem wurde die Studie abgebrochen, da die Behandlung mit Torcetrapib mit einem erhöhten Risiko von kardiovaskulären Ereignissen und mit einer erhöhten Sterblichkeit einher ging.[8] Als Grund für das unerwartete Resultat wird unter anderem ein Anstieg des Blutdrucks um 5,4 mmHg bei Behandlung mit Torcetrapib diskutiert. Ursache dieses Effekts könnte eine Erhöhung der Konzentration des Nebennierenrindenhormons Aldosteron gewesen sein. Ein weiterer Erklärungsansatz ist der spezifische Wirkmechanismus von Torcetrapib mit der genannten Komplexbildung, die ungünstige Effekte auf die Funktion der schützenden HDL-Partikel gehabt haben könnte.
Anacetrapib
Der CETP-Inhibitor Anacetrapib befindet sich derzeit in klinischen Studien. In einer Phase II-Studie bei Patienten mit Dyslipidämie zeigte sich ein Anstieg der HDL-C-Konzentration um 139 Prozent [13], die LDL-C-Konzentration sank gleichzeitig um knapp 40 %.[14] Die tatsächlichen klinischen Auswirkungen dieser veränderten Parameter sind, wie auch der genaue Wirkmechanismus von Anacetrapib, Gegenstand weiterer Untersuchungen. Hinweise auf einen Blutdruckanstieg unter Therapie mit Anacetrapib gab es nicht.
Dalcetrapib
Der CETP-Inhibitor Dalcetrapib befindet sich ebenfalls in klinischen Studien. Dalcetrapib bindet ausschließlich an CETP und führt nicht zu einer Ausbildung hoch-affiner Komplexe mit HDL. Stattdessen induziert es eine Konformationsänderung des CETP, wodurch eine Bindung an HDL verhindert wird.[15] Zudem wird das CETP nicht komplett blockiert, sondern in seiner Funktion moduliert.[16] Tierversuche am Hamster zeigen außerdem, dass sich bei der Therapie mit Dalcetrapib die Ausscheidung von Cholesterin-Abbauprodukten erhöhte, der reverse Cholesterintransport also verstärkt wird. Dies deutet ebenfalls darauf hin, dass HDL in seiner Funktion erhalten bleibt.[17] In klinischen Phase II-Studien führte Dalcetrapib zu einem Anstieg des HDL-C um 30 Prozent. Es kam nicht zu einem Blutdruckanstieg und auch nicht zu einer Induktion der Aldosteronsynthase.[9] In einer Phase IIb-Studie zeigte Dalcetrapib zudem ein der Behandlung mit Placebo vergleichbares Nebenwirkungsprofil.[10] Als Konsequenz aus den günstigen Phase II-Daten wird Dalcetrapib jetzt in dem großen Studienprogramm, dem dal-HEART-Programm, untersucht. Es umfasst vier Phase III-Studien bei Patienten mit koronarer Herzerkrankung.
Einzelnachweise
- ↑ a b c d e f Tall AR: Plasma cholesteryl ester transfer protein. (PDF) In: J. Lipid Res.. 34, Nr. 8, August 1993, S. 1255–74. PMID 8409761.
- ↑ a b c d e f g h Barter PJ, Brewer HB, Chapman MJ, Hennekens CH, Rader DJ, Tall AR: Cholesteryl ester transfer protein: a novel target for raising HDL and inhibiting atherosclerosis. In: Arterioscler. Thromb. Vasc. Biol.. 23, Nr. 2, Februar 2003, S. 160–7. PMID 12588754.
- ↑ Barter PJ, Hopkins GJ, Calvert GD: Transfers and exchanges of esterified cholesterol between plasma lipoproteins. In: Biochem. J.. 208, Nr. 1, Oktober 1982, S. 1–7. PMID 6760853. Volltext bei PMC: 1153921.
- ↑ von Eckardstein A, Nofer JR, Assmann G: High density lipoproteins and arteriosclerosis. Role of cholesterol efflux and reverse cholesterol transport. In: Arterioscler. Thromb. Vasc. Biol.. 21, Nr. 1, Januar 2001, S. 13–27. PMID 11145929.
- ↑ Matsuura F, Wang N, Chen W, Jiang XC, Tall AR: HDL from CETP-deficient subjects shows enhanced ability to promote cholesterol efflux from macrophages in an apoE- and ABCG1-dependent pathway. In: J. Clin. Invest.. 116, Nr. 5, Mai 2006, S. 1435–42. doi:10.1172/JCI27602. PMID 16670775. Volltext bei PMC: 1451209.
- ↑ Kontush, Chapman: Pharmacol Rev. 2006; Nr. 58: S. 342-374.
- ↑ Castelli et al.: Can J Cardiol. 1988; Nr. 4 (suppl. A): S. 5A-10A.
- ↑ a b Barter PJ, Caulfield M, Eriksson M, et al.: Effects of torcetrapib in patients at high risk for coronary events. (PDF) In: N. Engl. J. Med.. 357, Nr. 21, November 2007, S. 2109–22. doi:10.1056/NEJMoa0706628. PMID 17984165.
- ↑ a b Stein EA, Stroes ES, Steiner G, et al.: Safety and tolerability of dalcetrapib. In: Am. J. Cardiol.. 104, Nr. 1, Juli 2009, S. 82–91. doi:10.1016/j.amjcard.2009.02.061. PMID 19576325.
- ↑ a b Stein EA, Roth EM, Rhyne JM, Burgess T, Kallend D, Robinson JG: Safety and tolerability of dalcetrapib (RO4607381/JTT-705): results from a 48-week trial. In: Eur. Heart J.. 31, Nr. 4, Februar 2010, S. 480–8. doi:10.1093/eurheartj/ehp601. PMID 20097702. Volltext bei PMC: 2821630.
- ↑ Niesor et al.: Atherosclerosis. 2008; Nr. 199: S. 231.
- ↑ Clark RW, Ruggeri RB, Cunningham D, Bamberger MJ: Description of the torcetrapib series of cholesteryl ester transfer protein inhibitors, including mechanism of action. In: J. Lipid Res.. 47, Nr. 3, März 2006, S. 537–52. doi:10.1194/jlr.M500349-JLR200. PMID 16326978.
- ↑ Bloomfield et al.: Am Heart J. 2009; Nr. 157: S. 352-360.
- ↑ Ärzte Zeitung online, 19. November 2010: http://www.aerztezeitung.de/medizin/krankheiten/herzkreislauf/article/630166/hdl-cholesterin-neuem-medikament-dramatisch-erhoeht.html
- ↑ Scientific Sessions, Orlando, November 16, 2009, Poster 1092.
- ↑ Okamoto H, Yonemori F, Wakitani K, Minowa T, Maeda K, Shinkai H: A cholesteryl ester transfer protein inhibitor attenuates atherosclerosis in rabbits. In: Nature. 406, Nr. 6792, Juli 2000, S. 203–7. doi:10.1038/35018119. PMID 10910363.
- ↑ Scientific Sessions, Orlando, November 17, 2009, Presentation 1271.
Kategorien:- Porenbildendes Protein
- Krankheitsassoziiertes Protein
Wikimedia Foundation.